
科目: 来源: 题型:
【题目】同种物质中同一价态的元素部分被氧化,部分被还原的氧化还原反应是
A.SO2+2H2S═S+2H2O
B.2NaNO32NaNO2+O2↑
C.NH4NO3N2O↑+2H2O
D.3Cl2+6KOH═5KCl+KClO3+3H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】将V1 mL 1.00 mol·L-1 HCl溶液和V2 mL 未知浓度的NaOH溶液混合均匀后,测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL)。
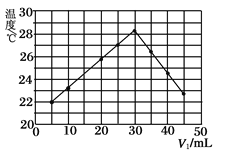
下列叙述正确的是
A.做该实验时环境温度为22 ℃
B.该实验表明化学能可以转化为热能
C.NaOH溶液的浓度约为1.00 mol·L-1
D.该实验表明有水生成的反应都是放热反应
查看答案和解析>>
科目: 来源: 题型:
【题目】吸入人体內的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体內的活性氧,由此推断Na2SeO3的作用是
A. 既作氧化剂又作还原剂
B. 既不作氧化剂又不作还原剂
C. 作还原剂
D. 作氧化剂
查看答案和解析>>
科目: 来源: 题型:
【题目】【2016湾里区模拟】在25℃、1.01×105 Pa下,反应2N2O5(g)═4NO2(g)+O2(g)△H=+56.7kJmol﹣1能自发进行的合理解释是( )
A.该反应是分解反应
B.该反应的熵增效应大于焓变效应
C.该反应是熵减反应
D.该反应是放热反应
查看答案和解析>>
科目: 来源: 题型:
【题目】W、X、Y、Z四种元素在周期表中的位置如图所示,下列说法不正确的是
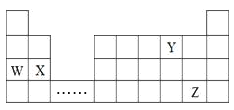
A. W、X、Y三种元素的原子半径依次减少
B. W元素的最高价氧化物的水化物的碱性比X的强
C. 可在省略号对应的族区域寻找各种优良的催化剂
D. Z元素与水反应得到HZO,HZO只有氧化性
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA表示为阿伏加德罗常数,下列叙述中,正确的是( )
A. 常温常压下,16 gSO2所含的分子数为0.25NA
B. 46 gNO2与N2O4的混合气体中所含的分子数是1NA
C. 0.1 molCl2完全反应,转移电子数目一定为0.2NA
D. 0.1 molH2与Cl2的混合气体充分反应后,体系中含有共价键总数为0.2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)实验中不能直接测出石墨和氢气生成甲烷反应的反应热,但可测出甲烷,石墨,氢气燃烧的反应热:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=-890.3kJ/mol
C(石墨)+O2(g)=CO2(g) ΔH2=―393.5kJ/mol
H2(g)+![]() O2(g)=H2O(l) ΔH3=―285.8kJ/mol,则由石墨生成甲烷的反应热:
O2(g)=H2O(l) ΔH3=―285.8kJ/mol,则由石墨生成甲烷的反应热:
C(石墨)+2H2(g)=CH4(g) ΔH 4= 。
(2)体积相同,pH均等于1的盐酸和CH3COOH溶液,分别加水稀释m倍、n倍,溶液的pH都变成3,则m________n(填>、<、= )
(3)取浓度相等的NaOH和HCl溶液,以3∶2体积比相混和,所得溶液的pH等于12,则原溶液的浓度为_________________
(4) 常温下,某一元酸HA的Ka=2×10-5,则0.05 mol/L该酸溶液的PH值=_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在某密闭恒容容器中发生反应:X(g) ![]() Y(g)+nZ(g) ΔH=+QkJ/mol(Q>0)。反应体系2min时达到 平衡后,各物质的浓度在不同条件下的变化如下图所示。(第10min到16min的X浓度变化曲线未标出),下列说法不正确的是
Y(g)+nZ(g) ΔH=+QkJ/mol(Q>0)。反应体系2min时达到 平衡后,各物质的浓度在不同条件下的变化如下图所示。(第10min到16min的X浓度变化曲线未标出),下列说法不正确的是

A. 反应方程式中n=1
B. 12min-14min内,用Y表示的评价速率为0.005mol/(L·min)
C. 在6min-10min内,反应吸收的热量为0.015Q kJ
D. 第12min时,Z曲线发生变化的原因是移走一部分Z
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com