
科目: 来源: 题型:
【题目】氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:
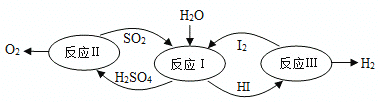
(1)反应Ⅰ的化学方程式是_______________________。
反应Ⅲ的化学方程式是____________________。
(2)SO2的排放是形成酸雨的原因之一,我们把pH小于_____的雨称为酸雨。
(3)反应Ⅰ得到的产物用I2进行分离。该产物的溶液在过量I2的存在下会分成两层,分别是含低浓度I2的H2SO4层和高浓度的I2的HI层。
①根据上述事实,下列说法正确的是____________(选填序号)。
a.两层溶液的密度存在差异
b.加I2前,H2SO4溶液和HI溶液不互溶
c.I2在HI溶液中比在H2SO4溶液中易溶
②分离两层液体用到的玻璃仪器主要有_____________________。
③辨别两层溶液的方法是____________。
④经检测,H2SO4层中c(H+):c(SO42-)=2.06:1。其比值大于2的原因是__________________________。
(4)反应Ⅱ:2H2SO4(l)→2SO2(g)+O2(g)+2H2O(g),已知生成9 g水蒸气吸收137.5 KJ的热量,写出该反应的热化学方程式_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】【2017孝义市模拟】下列储存药品的方法中,正确的是( )
A.液溴保存在带橡胶塞的玻璃瓶中
B.新制氯水保存在棕色广口瓶中
C.金属锂保存在石蜡油中
D.硅酸钠溶液保存在带磨口玻璃塞的玻璃瓶中
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.甲醇是重要的化学工业基础原料和清洁液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应 | 平衡 常数 | 温度/℃ | |
500 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 2.50 |
③3H2(g)+CO2(g) | K3 | ||
(1) 据反应①与②可推导出K1、K2与K3之间的关系,则K3=________(用K1、K2表示)。500 ℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol·L-1)分别为0.8、0.1、0.3、0.15,则此时v正__________v逆(填“>”、“=”或“<”)。
(2) 对于反应③,在相同温度和容积不变时,能说明该反应已达平衡状态的是
A.n(CO2)∶n(H2)∶n(CH3OH)∶n(H2O)=1∶3∶1∶1
B.容器内压强保持不变
C.H2的消耗速率与CH3OH的消耗速率之比为3∶1
D.容器内的密度保持不变
Ⅱ.超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)ΔH<0
2CO2(g)+N2(g)ΔH<0
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)(mol/L) | 1.00×10-3 | 4.50×10- 4 | 2.50×10- 4 | 1.50×10- 4 | 1.00×10- 4 | 1.00×10- 4 |
c(CO)(mol/L) | 3.60×10- 3 | 3.05×10- 3 | 2.85×10- 3 | 2.75×10- 3 | 2.70×10- 3 | 2.70×10- 3 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)前2s内的平均反应速率υ(N2)= ,CO的平衡转化率为____________。(结果均保留两位有效数字)
(2)写出该反应的平衡常数K的表达式________________。
(3)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是 。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(4)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。某同学设计了三组实验,实验条件已经填在下面实验设计表中。
实验 编号 | T(℃) | NO初始浓度 (mol/L) | CO初始浓度 (mol/L) | 催化剂的比表面积(m2/g) |
Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
Ⅱ | 280 | 1.20×10-3 | 5.80×10-3 | 124 |
Ⅲ | 350 | 1.20×10-3 | 5.80×10-3 | 124 |
①以上三组实验的实验目的是_______________________。
②请在给出的坐标图中,画出上表中的第三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图。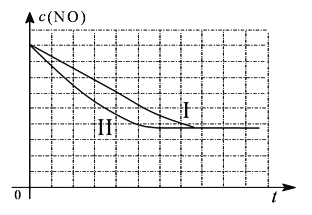
查看答案和解析>>
科目: 来源: 题型:
【题目】电镀废水中常含有剧毒的NaCN,可用两段氧化法处理:
①第一段:NaCN+NaClO→NaOCN+NaCl
②第二段:2NaOCN+3NaClO→Na2CO3+CO2↑+3NaCl+N2↑
完成下列填空:
(1)上述反应涉及的元素中,氮原子核外价电子数是______个;
O2—、Na+、Cl—中半径最小的是_____________。
(2)NaCN晶体中含有的化学键类型为_____________________________。
(3)第二段过程中,产物属于双原子分子的结构式是___________,该物质一般要比其他共价化合物如:NH3、H2S等都要稳定,其原因为:___________________;写出该物质的一种用途:____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】【2017届北京市昌平区高三上学期期末】下列说法不正确的是
N2(g)与H2(g)在铁催化剂表面经历如下过程生成NH3(g):
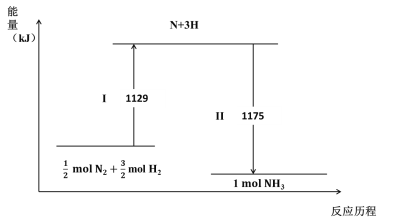
A.Ⅰ过程中破坏的均为非极性键
B.Ⅰ过程吸收能量,II过程放出能量
C. N2(g) + 3H2(g) ![]() 2NH3(g) ΔH = –44 kJ·mol-1
2NH3(g) ΔH = –44 kJ·mol-1
D.1mol N2(g)与3 mol H2(g)所具有的总能量比2 mol NH3(g) 所具有的总能量高
查看答案和解析>>
科目: 来源: 题型:
【题目】下列单质或化合物性质的描述正确的是
A.Na2CO3的溶解性比NaHCO3小
B.SiO2与酸、碱均能反应,属于两性氧化物
C.FeCl3溶液制作铜质印刷线路板的离子反应为2Fe3++Cu=2Fe2++Cu2+
D.Fe在足量Cl2中燃烧生成FeCl2和FeCl3
查看答案和解析>>
科目: 来源: 题型:
【题目】0.6mol锌粉跟过量盐酸反应,在一定温度下,为加快反应速率但又不影响生成氢气的总量,可向反应混合物中加入适量的( )
A.铜粉
B.醋酸锌溶液
C.氯化铜固体
D.二氧化锰
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com