
科目: 来源: 题型:
【题目】下列叙述正确的是
A.直径介于1nm~100nm之间的微粒称为胶体
B.电泳现象可以证明胶体粒子带电
C.丁达尔效应是溶液与胶体的本质区别
D.胶体粒子很小,可以透过滤纸和半透膜
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 mol·L-1 | K1=4.4×10-7 mol·L-1 K2=5.6×10-11 mol·L-1- | 3.0×10-8mol·L-1 |
请回答下列问题:
(1)同浓度的CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为________________。
(2)常温下0.1 mol·L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是________(填字母序号,下同)。
A.c(H+)
B.![]()
C.c(H+)·c(OH-)
D.![]()
E.![]()
若该溶液升高温度,上述5种表达式的数据增大的是___________。
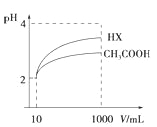
(3)体积为10mL pH=2的醋酸溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程pH变化如图:则HX的电离平衡常数__________(填“大于”、“等于”或“小于”)醋酸的平衡常数。稀释后,HX溶液中由水电离出来的c(H+) __________(填“大于”、“等于”或“小于”)醋酸的溶液中由水电离出来的c(H+),理由是______________________________。
(4)已知100℃时,水的离子积为1×10-12,该温度下测得某溶液pH=7,该溶液显__________(填“酸”、“碱”或“中”)性。将此温度下pH=1的H2SO4溶液aL与pH=11的NaOH溶液bL混合,若所得混合液pH=2,则a:b=__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有下列转化关系(反应条件略):

已知:① X 、Y 、Z 、W 均为氧化物。常态下,X 是红棕色气体;Y 能使澄清石灰水变浑浊但不能使品红溶液褪色。② 相对分子质量:甲﹤乙 。③ 将甲的浓溶液露置在空气中一段时间,质量减小浓度降低;将乙的浓溶液露置在空气中一段时间,质量增加浓度降低。请填写下列空白:
(1)Z的化学式: 。
(2)将乙的浓溶液露置在空气中一段时间,质量增加浓度降低,反映出乙的浓溶液具有 性。利用这种性质可以进行 项(填字母)实验操作。
a.钝化铁片 b.检验Ba2+离子 c.干燥氨气 d.干燥氯气
(3)在 X 和 Z 的反应中,被氧化的X 与被还原的X 的物质的量之比是: 。
(4)W可用于工业制溴过程中吸收潮湿空气中的Br2 ,写出该反应的离子方程式: 。
(5)写出M与甲的浓溶液在加热条件下反应的化学方程式: 。
查看答案和解析>>
科目: 来源: 题型:
【题目】向硫酸铜水溶液中逐滴加入氨水,先形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液,再向溶液中加入乙醇有深蓝色晶体(化学式为[Cu(NH3)4]SO4·H2O)析出。
(1)写出上述实验前两步反应的离子方程式__________,____________。
(2)铜元素基态原子的电子排布式为_________________,铜单质晶体中的原则堆积模型属于_________堆积(填堆积模型名称)。
(3)在上述深蓝色晶体所含的非金属元素中,电负性最大的是_________(填元素符号),第一电离能最大的是_________(填元素符号)。该晶体中的阴离子的立体构型是_________,阴离子的中心原子的杂化方式为_________。
(4)氨的沸点_________(填“高于”或“低于”)膦(PH2),原因是_____________。
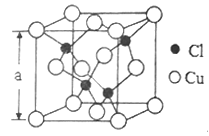
(5)Cu的一种氯化物晶胞结构如图所示,该氯化物的化学式是______________。若该晶体的密度为pg·cm-3,以NA表示阿伏伽德罗常数,则该晶胞的边长为a=_____________nm。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知可逆反应温度为T0时,在容积固定的密闭容器中发生X(g)+Y(g)![]() Z(g)(未配平)反应,各物质浓度随时间变化的关系如图a所示。其他条件相同,温度分别为T1、T2时发生反应;Z的浓度随时间变化的关系如图b所示。下列叙述正确的是
Z(g)(未配平)反应,各物质浓度随时间变化的关系如图a所示。其他条件相同,温度分别为T1、T2时发生反应;Z的浓度随时间变化的关系如图b所示。下列叙述正确的是

A.发生反应时,各物质的反应速率大小关系为v(X)=v(Y)=2v(Z)
B.图a中反应达到平衡时,Y的转化率为37.5%
C.T0时,该反应的平衡常数为33.3
D.该反应正反应的反应热ΔH<0
查看答案和解析>>
科目: 来源: 题型:
【题目】某探究性实验小组的同学将打磨过的镁条投入到滴有酚酞的饱和NaHCO3溶液中,发现反应迅速,产生大量气泡和白色不溶物,溶液的浅红色加深。该小组同学对白色不溶物的成分进行了探究和确定。
Ⅰ、提出假设:
(1)甲同学:可能只是MgCO3;
乙同学:可能只是 ;
丙同学:可能是xMgCO3·yMg(OH)2
(2)在探究沉淀成分前,须将沉淀从溶液中过滤、洗涤、低温干燥,洗涤沉淀的操作方法是 。
Ⅱ、定性实验探究:
(3)取沉淀物少许于试管中,加入稀盐酸时固体溶解,产生大量气泡,则 同学假设错误(选填“甲”、“乙”或“丙”)。
Ⅲ、定量实验探究:取一定量已干燥过的沉淀样品,利用下列装置测定其组成(部分固定夹持类装置未画出),经实验前后对比各装置的质量变化来分析沉淀的组成,得出丙同学的假设是正确的。请回答下列问题:
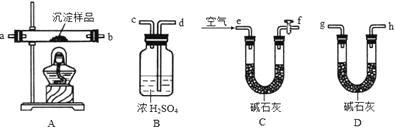
(4)实验中合理的连接顺序为:e→ → → → → → g→h(各装置只使用一次)。
(5)实验一段时间后,当B装置中 (填实验现象),停止加热,说明固体已分解完全;打开f处的活塞,缓缓通入空气数分钟的目的是 ,装置C中碱石灰的作用是 。
(6)指导老师认为在上述实验装置中末端还需再连接一个D装置,若无此装置,会使测出的x :y的值 (选填“偏大”、“偏小”或“无影响”)。
(7)若改进实验后,最终装置B质量增加m克,装置D质量增加了n克,则x :y= 。(用含m、n的代数式表示)
查看答案和解析>>
科目: 来源: 题型:
【题目】某小组的同学们利用下图装置,探究不同条件对铁与酸反应速率的影响。
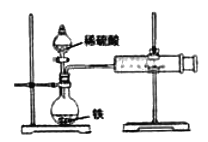
请回答下列问题。
(1)铁与稀硫酸反应的离子方程式是_______________________________________。
(2)适当升高烧瓶内液体的温度,产生气泡的速率将__________(填“加快、”“减慢”或“不变”),由此得出的结论是______________________________________________。
(3)将稀硫酸换为浓硫酸,可观察到_______________,原因是_________________。
(4)向烧瓶中滴入几滴CuSO4溶液,产生气泡的速率明显加快。这是什么原因?
甲同学:CuSO4溶液中的Cu2+对铁与稀硫酸的反应起了催化作用。
乙同学:CuSO4与Fe反应生成了Cu,从而Fe、Cu、稀硫酸构成了原电池,使反应速率加快。
你同意_______的观点,欲证明此观点,可另取一套上图装置,向烧瓶中直接加入少量_____,观察现象。
查看答案和解析>>
科目: 来源: 题型:
【题目】将一定量的SO2(g)和O2(g)分别通入体积为2L的恒容密闭容器中,在不同温度下进行反应:
2 SO2(g)+ O2(g)![]() 2SO3△H<0。得到如表中的两组数据:
2SO3△H<0。得到如表中的两组数据:
实验编号 | 温度/℃ | 平衡常数/mol-1·L | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
SO2 | O2 | SO2 | O2 | ||||
1 | T1 | K1 | 4 | 2 | x | 0.8 | 6 |
2 | T2 | K2 | 4 | 2 | 0.4 | y | t |
下列说法不正确的是
A.x= 1.6,y=0.2 ,t<6
B.T1、T2的关系:T1 > T2
C.K1、K2的关系:K2>K1
D.实验1在前6min的反应速率υ(SO2)=0.2 mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
【题目】 A、B、C、D、M均为中学化学常见物质,它们的转化关系如下图所示(部分生成物和反应条件略去)。A与水的反应在常温下进行。下列推断不正确的是( )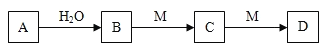
A. 若A为淡黄色固体,则D可能为CO
B. 若M为可溶性铝盐,则D可能为白色沉淀,且M(D)=M(A)
C. 若D为小苏打,C转化为D的反应是CO2+H2O+CO32-=2HCO3-,则A可能为氯气
D. 若C为CO2,则A一定为化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等有关。下列各组物质:①Cu与HNO3溶液;②MnO2与盐酸溶液;③Zn与H2SO4溶液;④Fe与HCl溶液。由于浓度不同而能发生不同氧化还原反应的是
A. ①③ B. ③④ C. ①②③ D. ①③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com