
科目: 来源: 题型:
【题目】如图,隔板K可左右移动,甲中充入2 mol A和1 mol B,乙中充入2mol C和1mol He,此时K 停在0处,发生反应2A(g)+B(g)![]() 2C(g),达到平衡后,恢复至温度。下列有关说法不正确的是( )
2C(g),达到平衡后,恢复至温度。下列有关说法不正确的是( )
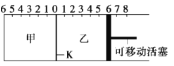
A.达平衡后,K最终停留在左侧刻度0~2之间
B.若平衡时K在左侧1处,则活塞停留在右侧6处
C.达到平衡时,甲容器中B的物质的量小于于乙容器中B的物质的量
D.根据隔板K滑动与否可判断左右两边的反应是否达到平衡
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应既是氧化还原反应,又是放热反应的是( )
A.氢氧化钠与稀硫酸反应
B.钠箔在Cl2中的燃烧
C.Ba(OH)28H2O与NH4Cl的反应
D.灼热的炭与水蒸气反应
查看答案和解析>>
科目: 来源: 题型:
【题目】下列广告语对应商品中含有的物质有误的是( )
A. “红梅味精,领先(鲜)一步”﹣﹣蛋白质
B. “衡水老白干,喝出男人味”﹣﹣乙醇
C. “吃了钙中钙,腰不疼了,腿不痛了,腰杆也直了”﹣﹣碳酸钙
D. “要想皮肤好,早晚用大宝”﹣﹣丙三醇
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容器中发生下列反应aA(g)cC(g)+dD(g),压缩容积到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
A.A的转化率变大 B.平衡向正反应方向移动
C.D的体积分数变大 D.a<c+d
查看答案和解析>>
科目: 来源: 题型:
【题目】标准状况下VL氨气溶解在1L水中(水的密度近似为1g/ml),所得溶液的密度ρg/ml,质量分数为W,物质的量浓度为c mol/L,则下列关系中不正确的是( )
A.ρ=(17V+22400)/(22.4+22.4V) B.W=17c/(1000ρ)
C.W=17V/(17V+22400) D.C=1000Vρ/(17V+22400)
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E是位于短周期的主族元素。已知:①热稳定性:HmD>HmC;②Cm-、E(m-1)-
具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题:
(1)HmDm的电子式__________。
(2)Cm-、E(m-1)-的还原性强弱顺序为__________(用离子符号表示),能证明其还原性强弱的离子方程式为____________________。
(3)写出B单质与A元素的最高价氧化物对应水化物的溶液反应的离子方程式___________________。
(4)用于判断C和D非金属性强弱的依据是__________
A.气态氢化物的稳定性 B.置换反应 C.与氢气化合难易程度
D.最高价含氧酸的酸性 E.得电子数目多少
F.两单质在自然界的存在形式
查看答案和解析>>
科目: 来源: 题型:
【题目】雾霾严重影响人们的生活, 雾霾的形成与汽车排放的 NOx等有毒气体有关。
(1)可以通过活性炭处理汽车尾气,原理为:C(s)+2NO(g)![]() N2(g)+CO2 (g) H<0。
N2(g)+CO2 (g) H<0。
①下列情况能说明该反应达到平衡状态的是( )
A.2ν正(NO) =ν逆(CO2)
B.在恒温、恒容的容器中,混合气体的压强保持不变
C.在绝热、恒容的容器中,反应的平衡常数不再变化
D.在恒温、恒压的容器中, 混合气体的密度保持不变
②在恒温、恒容条件下, 加入2 mol C(s)和2 mol NO(g)达平衡后,再在绝热、恒容条件下,加入1 mol NO重新达平衡后, N2的百分含量将____________(填“增大”、“减小”、“不变”)。
(2)臭氧是理想的烟气脱硝试剂,原理为:2NO2(g)+O3(g)![]() N2O5(g)+O2(g)。若在容积为10L的密闭容器中进行该反应,起始时充入0.4 molNO2、0.2 molO3,反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
N2O5(g)+O2(g)。若在容积为10L的密闭容器中进行该反应,起始时充入0.4 molNO2、0.2 molO3,反应在不同条件下进行,反应体系总压强随时间的变化如图所示。

①实验a从开始至平衡时的反应速率v(O3)=_________;实验c中NO2的平衡转化率为___________。
②与实验a相比,其他两组改变的实验条件分别是:b_________,c__________。
③M点的逆反应速率 v(逆)____________N点的正反应速率v(正)(填“>”、“<”或“=”)。
④若在N点时,维持温度和压强不变,t1时再加入0.4 molNO2、0.2 mol O3,请在图中画出逆反应速率在t1后随时间t的变化曲线图。

查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是
A. 1mol甲基中含有电子数为10NA
B. 常温下,1LpH=12的Na2CO3溶液中含有的OH-离子数为0.01 NA
C. 标准状况下,NO和O2各11.2L混合充分反应,所得气体的分子总数为0.75 NA
D. 50mL12mol·L-1盐酸和足量MnO2共热,转移的电子数为0.3 NA
查看答案和解析>>
科目: 来源: 题型:
【题目】下列溶液中离子浓度关系的表示正确的是( )
A.NaHCO3溶液中:c(H+)+c(Na+)=c(OH-)+c(CO![]() )+c(HCO
)+c(HCO![]() )
)
B.pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后的溶液中:c(OH-)>c(H+)+c(CH3COO-)
C.0.1 mol·L-1的NH4Cl溶液中:c(Cl-)>c(H+)>c(NH![]() )>c(OH-)
)>c(OH-)
D.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合后的溶液中:
2c(Na+)=c(CH3COOH)+c(CH3COO-)
查看答案和解析>>
科目: 来源: 题型:
【题目】右表是元素周期表的一部分,其中A、B、D、E、G、J为短周期元素,G元素的核电荷数为B元素的2倍。请回答下列问题:
A | B | ||
D | E | G | J |
L | M | Q |
(1)J的最高价氧化物对应水化物的化学式是___________________。
(2)G2J2常用作橡胶的低温硫化剂和黏结剂,其电子式为_______________________。写出一个能表示元素G、J非金属性强弱关系的化学方程式____________________________。
(3)G单质在空气中燃烧生成一种无色有刺激性气味的气体,该无色有刺激性气味的气体与含1molJ的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在—定条件下反应,可生成一种强酸和一种氧化物,且该反应中有NA个电子转移,则该反应的化学方程式是________________________。
(4)A的最简单氢化物是___________(填“极性”或“非极性”)分子,实验室制备该物质的化学方程式为__________________________________________。
(5)根据元素周期律,可以推测上表中长周期元素的单质具有半导体特性的是__________(填元素符号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com