
科目: 来源: 题型:
【题目】室温时,向20mL0.1000mol·L-1H2C2O4溶液中滴加0.1000mol·L-1NaOH溶液,混合溶液的pH随滴加NaOH溶液体积的变化如图所示。下列有关叙述错误的是

A. 忽略H2C2O4的第二步电离,由题给信息,可以计算出常温下H2C2O4的电离常数
B. A、B、C三点所对应的溶液中,水的电离程度最小的是A点
C. A、B、C三点所对应的溶液中,均有c(Na+)<c(OH-)+c(HC2O4-)+2c(C2O42-)
D. 在B点溶液中,生成的含钠化合物有两种,且n(HC2O4-)+n(C2O42-)=2.0×10-3mol
查看答案和解析>>
科目: 来源: 题型:
【题目】现有在室温的条件下,pH均为a的H2SO4溶液和NH4Cl溶液,回答下列问题:
(1)两溶液中c(H+)·c(OH)=________________。
(2)各取5 mL上述溶液,分别加水稀释至50 mL,pH较大的是___________溶液。
(3)各取5 mL上述溶液,分别加热到90℃,pH较小的是___________溶液。
(4)H2SO4溶液和NH4Cl溶液中由水电离出的c(H+)分别为_________、__________。
(5)取5 mL NH4Cl溶液,加水稀释至50 mL,c(H+)_________10(a+1)mol·L1(填“>”“<”或“=”),![]() ___________(填“增大”“减小”或“不变”)。
___________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据提供条件推断元素,并按要求填空:
(1)原子核外有3个电子层,其价电子数为7,最高价氧化物对应水化物化学式________,其单质与NaOH反应的化学方程式为_________________________。
(2) 已知X+、Y2+、Z—、W2—四种离子均具有相同的电子层结构,则X、Y、Z、W这四种元素的原子序数由大到小的顺序是_______________,原子半径由大到小的顺序是 。
(3)A+、B—、C、D 四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++B—![]() C+D↑,则标出A+、B—的电子式 , ;比较C和D的稳定性的强弱大小 (用化学式表示)
C+D↑,则标出A+、B—的电子式 , ;比较C和D的稳定性的强弱大小 (用化学式表示)
(4) ①NH4NO3②NaF ③CO2④K2O2⑤NaOH ⑥CH4
只含有极性键的是________,既有离子键又有非极性键的是______;既有离子键又有极性键的是______.
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组设计了一组实验验证元素周期律。
(Ⅰ)甲同学在a、b、c三只烧杯里分别加入50 mL水,再分别滴加几滴酚酞溶液,依次加入大小相近的锂、钠、钾块,观察现象。
甲同学设计实验的目的是 , 烧杯 (填字母)中的反应最剧烈。
(Ⅱ)乙同学设计实验验证非金属元素的非金属性越强,对应的最高价含氧酸的酸性就越强。他设计了下图装置以验证氮、碳、硅元素的非金属性强弱。

乙同学设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到有白色沉淀生成。
(1)写出所选用物质的化学式:A: ;B: ; C: 。
(2)写出烧杯中发生反应的离子方程式:
(3)该装置存在着某个缺陷,改进的方法是
查看答案和解析>>
科目: 来源: 题型:
【题目】30 mL 1 mol/L NaCl溶液和40 mL 0.5 mol/L CaCl2溶液混合之后(体积的变化忽略不计),混合液中Cl-的物质的量浓度为 ( )
A. 0.5 mol/L B. 0.6 mol/L C. 1 mol/L D. 2 mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】
铜是人类最早发现的金属,也是人类广泛使用的一种金属。铜及其化合物在工业、工程技术和工艺上有着广泛的应用。
(1)早期发现的天然准晶颗粒由Cu、Fe、Al三种金属元素组成。Fe元素位于元素周期表的____区。基态Al原子的L层电子排布图为___________。
(2)Cu2O为半导体材料,可由乙醛(CH3CHO)和新制氢氧化铜反应得到,同时可得到乙酸。乙醛中碳原子的杂化轨道类型为_________,1mol乙酸分子中含有的σ键的数目为____________。
(3)制造单晶硅太阳能电池片时,一般掺杂微量的铜、碳、硼、氮等。一价铜离子的电子排布式为____。碳、硼、氮元素的电负性由大到小的顺序是_____。(用元素符号表示)
(4)在络离子[Cu(NH3)4]2+中NH3的VSEPR模型为_________。
(5)铜银合金晶体具有面心立方最密堆积结构。在晶胞中,Cu原子位于面心,Ag原子位于顶点,若该晶胞边长为r pm,则合金的密度为____g·cm-3(设阿伏伽德罗常数的值为NA)。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知苯乙烯的结构为![]() 。有关该物质的下列说法正确的是
。有关该物质的下列说法正确的是
A. 该物质在一定条件下和氢气完全加成,加成产物的一溴取代物有6种
B. 该物质能使溴水和酸性高锰酸钾溶液褪色,褪色原理完全相同
C. 苯乙烯分子的所有原子不可能在同一平面上
D. 除去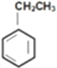 中的苯乙烯可以通入等量氢气反应
中的苯乙烯可以通入等量氢气反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com