
科目: 来源: 题型:
【题目】体积为1ml、浓度均为0.10mol/L的XOH和X2CO3溶液,分别加水稀释至体积V,pH随lgV的变化情况如图所示,下列叙述中正确的是

A.XOH是弱碱
B.pH=10的两种溶液中的c(X+):XOH大于X2CO3
C.已知H2CO3的电离平衡常数Ka1远远大于Ka2,则Ka2约为1.0×10-10.2
D.当lgV=2时,若X2CO3溶液升高温度,溶液碱性增强,则c(HCO3-)/c(CO32-)减小
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期金属元素甲—戊在元素周期表中的相对位置如右图所示,下面判断正确的是

A. 原子半径:戊<丁<丙 B. 金属性:甲>丙
C. 最高价氧化物水化物碱性:丙>丁>戊 D. 最外层电子数:甲>乙
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,下列叙述是可逆反应A(g)+2B(g)![]() 2C(g)在定容密闭容器中达到平衡的标志的是:
2C(g)在定容密闭容器中达到平衡的标志的是:
①C的生成速率与C的分解速率相等;
②单位时间内消耗amol A,同时生成2amolC;
③A、B、C的浓度不再变化;
④混合气体的总压强不再变化;
⑤混合气体的平均摩尔质量不再变化;
⑥用A、B、C的物质的量浓度变化表示的反应速率之比为1:3:2;
⑦A、B、C的分子数目比为1:3:2;
⑧混合气体的密度不再变化
A.②⑤ B.①③④⑤ C.②⑥⑦⑧ D.⑤⑥⑧
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中错误的是( )
A. CO燃烧是放热反应 B. H2SO4与NaOH反应是放热反应
C. CaO与H2O反应是吸热反应 D. CaCO3受热分解是吸热反应
查看答案和解析>>
科目: 来源: 题型:
【题目】称取两份铝粉,第一份加足量NaOH溶液,第二份加足量硫酸,如果要得到相同体积(同温同压)的氢气,两份铝粉的质量比是( )
A.1:1
B.1:3
C.3:2
D.1:2
查看答案和解析>>
科目: 来源: 题型:
【题目】“温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体,CO2的综合利用是解决温室及能源问题的有效途径。
(1)研究表明CO2和H2在催化剂存在下可发生反应生成CH3OH。己知部分反应的热化学方程式如下:
CH3OH(g)+![]() O2(g) = CO2(g)+2H2O(1) △H1=akJmol-1
O2(g) = CO2(g)+2H2O(1) △H1=akJmol-1
H2(g)+![]() O2(g) = H2O(1) △H2=bkJmol-1
O2(g) = H2O(1) △H2=bkJmol-1
H2O(g) = H2O(l) △H3=ckJmol-1
则 CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=__________kJmol-1
CH3OH(g)+H2O(g) △H=__________kJmol-1
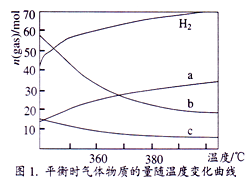
(2)CO2催化加氢也能合成低碳烯烃: 2CO2(g)+6H2(g)![]() C2H4(g)+4 H2O (g),不同温度下平衡时的四种气态物质的物质的量如图1所示,曲线b表示的物质为_______________ (写化学式)。
C2H4(g)+4 H2O (g),不同温度下平衡时的四种气态物质的物质的量如图1所示,曲线b表示的物质为_______________ (写化学式)。
(3)CO2和H2在催化剂Cu/ZnO作用下可发生两个平行反应,分别生成CH3OH和CO。
反应 A:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
反应B:CO2(g)+ H2(g)![]() CO(g)+H2O(g)
CO(g)+H2O(g)
控制CO2和H2初始投料比为1∶3时,温度对CO2平衡转化率及甲醇和CO产率的影响如图2所示。

① 由图2可知温度升高CO的产率上升,其主要原因可能是__________________。
② 由图2可知获取CH3OH最适宜的温度是________________,下列措施有利于提高CO2转化为CH3OH的平衡转化率的措施有__________________。
A.使用催化剂 B.增大体系压强
C.增大CO2和H2的初始投料比 D.投料比不变和容器体积不变,增加反应物的浓度
(4)在催化剂表面通过施加电压可将溶解在水中的二氧化碳直接转化为乙醇,则生成乙醇的电极反应式为______________________________________________________。
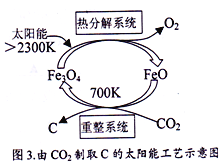
(5)由CO2制取C的太阳能工艺如图3所示。“热分解系统”发生的反应为:2Fe3O4![]() 6FeO+O2↑,每分解1mol Fe3O4转移电子的物质的量为_____________;“重整系统”发生反应的化学方程式为_____________________________________________。
6FeO+O2↑,每分解1mol Fe3O4转移电子的物质的量为_____________;“重整系统”发生反应的化学方程式为_____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一容积为2L的恒温恒容密闭容器中充入2mol SO2和1mol O2,发生反应2SO2(g)+O2(g) ![]() 2SO3(g) △H=-Q kJ·mol-l (Q>O),下列有关说法不正确的是
2SO3(g) △H=-Q kJ·mol-l (Q>O),下列有关说法不正确的是
A. 反应达到平衡时,放出热量为QkJ
B. 若容器的压强不再发生交化,则反应达到平衡
C. 反应过程中c(SO2)+ c(SO3)=1 mol·L-1恒成立
D. 平衡时,SO2、O2的转化率相等
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素A、B、C、D、E、F的原子序数逐渐增大,A和B同周期,A和F同族,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的简单阴离子与C、D、E的简单阳离子电子层结构相同。请回答下列有关问题:
(1)F在元素周期表中的位置是_____________。
(2)C2B2的电子式是_________;AB2的结构式是_______。
(3)B、C、D、E离子半径由大到小的顺序为______(用离子符号回答); C、D、E最高价氧化物对应水化物的碱性由强到弱的顺序为____________(用化学式表示,且用“>”符号连接回答)。
(4) C、E最高价氧化物对应水化物能够相互反应,则反应的离子方程式为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在容积为2L的密闭容器中进行如下反应:
A(g)+2B(g)![]() 3C(g)+nD(g),开始时A为4mol,B为6mol;5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。计算
3C(g)+nD(g),开始时A为4mol,B为6mol;5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。计算
(1)5min末A的物质的量浓度为__________ mol/L·
(2)前5min内用B表示的化学反应速率v(B)为___________ mol/(L·min)。
(3)化学方程式中n值为__________。
(4)此反应在四种不同情况下的反应速率分别为:
①v(A)=5mol/(L·min)
②v(B)=6mol/(L·min)
③v(C)=4.5mol/(L·min)
④v(D)=8mol/(L·min)
其中反应速率最快的是__________(填编号)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某校化学学习小组设计了两组实验来探究元素周期律。
Ⅰ.甲组同学为验证卤素单质氧化性的相对强弱,用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
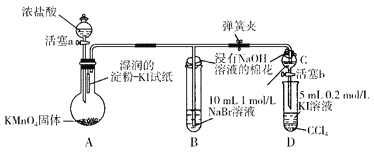
实验过程及现象:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡。静
置后CCl4层溶液变为紫红色。
请回答下列有关问题:
(1)验证氯气的氧化性强于碘的实验现象是______________________________。
(2)B和C仪器口盛放浸有NaOH溶液的棉花的作用_______________________。
(3)过程Ⅲ实验的目的是_____________________________。
(4)由此实验得出的结论:同主族元素从上到下,原子半径逐渐增大,得电子能力逐渐_____________ (填“减弱”或“增强”)。
Ⅱ.乙组同学设计了如图1装置来一次性完成验证C、Si、S非金属性强弱的实验研究。
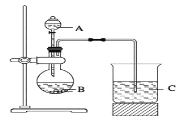
(1)A中所盛溶液的名称是__________。
(2)B仪器的名称是____________。
(3)烧杯C中发生反应的离子方程式为_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com