
科目: 来源: 题型:
【题目】(1)准确量取25.00mL高锰酸钾溶液,可选用的仪器是 .
(A)50mL 量筒 (B)10mL量筒 (C)50mL 酸式滴定管 (D)50mL碱式滴定管
(2) 进行中和滴定时,事先不应该用所盛溶液润洗的仪器是 .
(A)酸式滴定管 (B)碱式滴定管 (C)锥形瓶 (D)量筒
某烧碱样品中含有少量不与酸作用的杂质,为了测定其纯度,进行以下滴定操作:
(A)在托盘天平上准确称取烧碱样品Wg,在烧杯中用蒸馏水溶解;
(B)在250mL的容量瓶中定容配制250mL烧碱溶液;
(C)用移液管移取25mL烧碱溶液于锥形瓶中,并滴入几滴甲基橙作指示剂;
(D)将物质的量浓度为cmolL﹣1的标准硫酸溶液装入已润洗过的酸式滴定管中,调整液面并记下起始读数为V1mL;
(E)在锥形瓶下垫一张白纸,滴定至橙色为止,记下读数为V2mL.
就此完成下列问题:
(3)观察滴定管里液面的高度时应注意:滴定管垂直,液面不再变化时才可读数,视线与溶液凹液面最低点相平,读数精确到 ml
(4)E步骤的操作中在锥形瓶下垫一张白纸的作用是 .
(5)D步骤的操作中液面应调整到 ,尖嘴部分应该充满液体,不能有气泡。
(6)下列操作导致待测烧碱浓度偏高的( )
A. 滴定前仰视,滴定结束时俯视 B. 滴定前有气泡
C. 滴定结束有气泡 D. 未用标准液洗涤滴定管
(7) 该烧碱样品纯度是 .
(8)滴定终点的判定
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.强酸跟强碱的反应热一定是中和热
B.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6kJ/mol
2NH3(g) ΔH=-38.6kJ/mol
C.吸热反应的发生都需要加热,放热反应在常温下一定容易发生
D.表示中和热的离子方程式为H+(aq)+OH-(aq)![]() H2O(l) ΔH=-57.3kJ/mol
H2O(l) ΔH=-57.3kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】某学生用0.1mol/L KOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
(A)移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞;
(B)用标准溶液润洗滴定管2-3次;
(C)把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
(D)取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm;
(E)调节液面至0或0刻度以下,记下读数;
(F)把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度;
完成以下填空:
(1)正确操作的顺序是:(用序号字母填写)B、D、_______________.
(2)上述(B)操作的目的是_____________________。
(3)上述(A)操作之前,如先用待测液润洗锥形瓶,则对测定结果的影响是(填偏大、偏小、不变,下同)_________________。
(4)实验中用左手控制 (填仪器及部位),眼睛注视 ,直至滴定终点。判断到达终点的现象是 。
(5)若称取一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸,则对测定结果的影响是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200℃左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全。电池总反应为:C2H5OH +3O2=2CO2 +3H2O,电池示意图如下,下列说法中正确的是
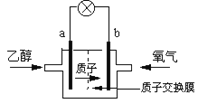
A.b极为电池的负极
B.电池工作时电子在内电路中由a极经溶液到b极
C.电池负极的电极反应为:C2H5OH+3H2O-12e-=2CO2+12H+
D.电池工作时,1mol乙醇被氧化时有6mol电子转移
查看答案和解析>>
科目: 来源: 题型:
【题目】有如下的可逆反应:X(g)+2Y(g)![]() 2Z(g) 现将X和Y以1︰2的体积比混合在密闭容器中,加压到3×107Pa,达到平衡后,已知平衡状态时反应物的总物质的量和生成物的总物质的量相等时,对应图中坐标上的温度是( )
2Z(g) 现将X和Y以1︰2的体积比混合在密闭容器中,加压到3×107Pa,达到平衡后,已知平衡状态时反应物的总物质的量和生成物的总物质的量相等时,对应图中坐标上的温度是( )
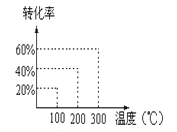
A. 100℃ B. 200℃ C. 300℃ D. 不能确定
查看答案和解析>>
科目: 来源: 题型:
【题目】【化学——物质结构与性质】
有A、B、C、D、E五种原子序数依次增大的元素(原子序数均小于30)。A的基态原子2p能级有3个电子;C的基态原子2p能级有1个电子;E原子最外层有1个单电子,其次外层有3个能级且均排满电子;D与E同周期,价电子数为2。则:
(1)写出基态E原子的价电子排布式________。基态A原子的第I电离能比B的大,其原因是____。
(2)B元素的氢化物的沸点是同族元素氢化物中最高的,原因是_________。
(3)A的最简单氢化物分子的空间构型为___________,其中A原子的杂化类型是_________。
(4)向E的硫酸盐溶液中通入A的气态氢化物至过量,产生蓝色沉淀,随后沉淀溶解得到深蓝色溶液,向溶液中加入适量乙醇,析出蓝色晶体。
①该蓝色晶体的化学式为_________,加入乙醇的目的是____________。
②写出该配合物中配离子的结构简式___________。
(5)C和D形成的化合物的晶胞结构如图所示,则D的配位数是_______,已知晶体的密度为ρg·cm-3,阿伏伽德罗常数为NA,求晶胞边长a=________cm(含用ρ、NA的计算式表示)。
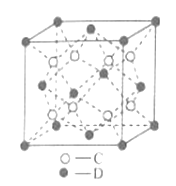
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的一部分,请回答有关问题:
主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为______。
(2)元素③、⑦、⑧中,原子半径从大到小的顺序是______(用元素符号表示)。
(3)元素④和⑥的最高价氧化物的水化物在水溶液中反应的离子方程式为______。
(4)元素⑤与元素⑧形成的化合物的电子式为________。
(5)①、②、⑦、⑧四种元素的最高价氧化物的水化物中酸性最强的是 ______。(填酸的化学式)。
(6)⑤⑥两元素相比较,金属性较强的是________ (填名称),可以验证该结论的实验是_____(填字母)。
A、将在空气中放置已久的这两种元素的块状单质分别放入热水中
B、将形状、大小相同的这两种元素的单质分别和同浓度的盐酸反应
C、将形状、大小相同这两种元素的单质分别和热水作用,并滴入酚酞溶液
D、比较这两种元素的气态氢化物的稳定性
查看答案和解析>>
科目: 来源: 题型:
【题目】将固体NH4I置于密闭容器中,在某温度下发生下列反应:
①NH4I(s)![]() NH3(g)+HI(g)
NH3(g)+HI(g)
②2HI(g)![]() H2(g)+I2(g)
H2(g)+I2(g)
当反应达到平衡时,cH2=0.5 mol / L,cHI=4 mol / L,则反应①的化学平衡常数为 ( )
A.10 B.15 C.20 D.25
查看答案和解析>>
科目: 来源: 题型:
【题目】将等物质的量的A、B、C、D四种物质混和,发生如下反应:
aA+bB![]() cC(s)+dD
cC(s)+dD
当反应进行一定时间后,测得A减少了n mol,B减少了n /2mol,C增加了3n /2mol,D增加了n mol,此时达到化学平衡:
(1) 该化学方程式中各物质的化学计量数为:
a= 、b= 、c= 、d= 。
(2) 若只改变压强,反应速度发生变化,但平衡不发生移动,该反应中各物质的聚集状态:
A B D
(3)若只升高温度,反应一段时间后,测知四种物质其物质的量又达到相等则该反应为 反应(填“放热”或“吸热”)
查看答案和解析>>
科目: 来源: 题型:
【题目】有关CaCO3的溶解平衡的说法中,不正确的是( )
A. CaCO3沉淀析出和沉淀溶解不断进行,但速率相等
B. CaCO3难溶于水,其饱和溶液几乎不导电,属于弱电解质溶液
C. 升高温度,CaCO3沉淀的溶解度增大
D. 向CaCO3沉淀中加入纯碱固体,CaCO3的溶解度降低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com