
科目: 来源: 题型:
【题目】Ⅰ.某同学为探究元素周期表中同周期元素性质的递变规律,设计了如下系列实验.
(1)将钠、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:________与盐酸反应最剧烈, ________与盐酸反应产生的气体最多.
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为__________.
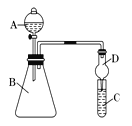
Ⅱ.利用右图装置可验证同主族元素非金属性的变化规律
(3)干燥管D的作用是 .
(4)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液 的现象, 即可证明.从环境保护的观点考虑,此装置缺少尾气处理装置,可用 溶液吸收尾气.
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液 的现象,即可证明。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有 溶液的洗气瓶.
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化亚铜(CuCl)广泛用于化工、印染、有机合成等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产氯化亚铜的工艺过程如下图所示。

回答下列问题:
(1)CuCl中Cu元素在周期表中的位置为___________。
(2)步骤①中N元素被还原为最低价,则Cu溶解的离子方程式为________。溶解温度应控制在60~70℃,原因是______________。
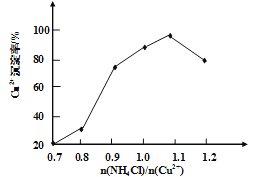
(3)写出步骤③中主要反应的离子方程式________。(NH4)2SO3要适当过量,目的有:保证Cu2+的还原速率,__________。已知NH4Cl、Cu2+的物质的量之比![]() 与Cu2+沉淀率的关系如图所示,当氯化铵用量增加到一定浓度后氯化亚铜的沉淀率减少,原因是________。
与Cu2+沉淀率的关系如图所示,当氯化铵用量增加到一定浓度后氯化亚铜的沉淀率减少,原因是________。
(4)步骤⑥加入乙醇洗涤的目的是__________。
(5)氯化亚铜的定量分析:
①称取样品0.250g和10mL过量的FeCl3溶液于250mL锥形瓶中,充分溶解;
②用0.100mol·L-1硫酸铈[Ce(SO4)2]标准溶液测定。已知:CuCl+FeCl3=CuCl2+FeCl2、Fe2++Ce4+=Fe3++Ce3+。
三次平衡实验结果如下表(平衡实验结果相差不能超过1%):
平衡实验次数 | 1 | 2 | 3 |
0.250g样品消耗硫酸铈标准溶液的体积(mL) | 24.35 | 24.05 | 23.95 |
则样品中CuCl的纯度为_______(结果保留3位有效数字)。
查看答案和解析>>
科目: 来源: 题型:
【题目】生物冶金技术越来越受到科学家的重视,这项技术的关键之一是寻找一些特殊的酶。下列有关叙述错误的是( )
A.酶是一种蛋白质
B.酶只有在强酸性或弱碱性条件下才能发挥作用
C.酶的催化具有高效性、选择性和专一性
D.发展生物冶金技术有利于节约能源和保护环境
查看答案和解析>>
科目: 来源: 题型:
【题目】PM2.5指大气中直径小于或等于2.5微米(1微米等于10-6m ) 的颗粒物,对空气质量和能见度有重要影响。若将直径为2.5微米颗粒物分散到水中,形成的分散系属于( )
A. 溶液 B. 胶体 C. 浊液 D. 不能确定
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D四种芳香族化合物的结构简式如下所示:

请回答下列问题:
(1)写出A中无氧官能团的名称 ,C中含氧官能团的名称为 .
(2)用A、B、C、D填空:能发生银镜反应的有 ,既能与FeCl3溶液发生显色反应又能与Na2CO3溶液反应放出气体的是 .
(3)按如图C经一步反应可生成E,E是B的同分异构体,
![]()
则反应①的反应类型为 ,写出反应②的化学方程式: .
查看答案和解析>>
科目: 来源: 题型:
【题目】元素是构成我们生活的世界中一切物质的“原材料”。
(1)自18世纪以来,科学家们不断探索元素之谜。通过从局部到系统的研究过程,逐渐发现了元素之间的内在联系。下面列出了几位杰出科学家的研究工作。
序号 | ||||
科学家 | 纽兰兹 | 道尔顿 | 德贝莱纳 | 尚古尔多 |
工作 | 发现“八音律”,指出从某一指定的元素起,第八个元素是第一个元素的某种重复 | 创立近代原子论,率先开始相对原子质量的测定工作 | 发现了5组性质相似的“三元素组”,中间元素的相对原子质量为前后两种元素相对原子质量的算术平均值 | 认为各元素组之间并非毫不相关,可以用相对原子质量把它们按从小到大的顺序串联 |
上述科学家的研究按照时间先后排序合理的是_________(填数字序号)。
(2)1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,如图所示。

①门捷列夫将已有元素按照相对原子质量排序,同一_________(填“横行”或“纵列”)元素性质相似。结合表中信息,猜想第4列方框中“?=70”的问号表达的含义是_________,第5列方框中“Te=128?” 的问号表达的含义是_________。
②到20世纪初,门捷列夫周期表中为未知元素留下的空位逐渐被填满。而且,随着原子结构的逐渐揭秘,科学家们发现了元素性质不是随着相对原子质量递增呈现周期性变化,而是随着原子序数(核电荷数)递增呈现周期性变化。其本质原因是_________(填字母序号)。
A.随着核电荷数递增,原子核外电子排布呈现周期性变化
B.随着核电荷数递增,原子半径呈现周期性变化
C.随着核电荷数递增,元素最高正化合价呈现周期性变化
(3)在现有的元素周期表中有A、B、D、E、X、Y、Z七种短周期元素。X与Y处于同一周期,Y的最高价氧化物的水化物与强酸、强碱均能反应。Z的单质常温下为气态,同条件下相对于氢气的密度比为35.5。其余信息如图所示:

①上述七种元素中,处于第二周期的有_________(用元素符号表示,下同),X在周期表中的位置是_________。
②E的原子结构示意图为_________,写出Z元素气态氢化物的电子式:_________。
③B单质与E的最高价氧化物的水化物在一定条件下发生反应的化学方程式为_________;Y单质与X的最高价氧化物的水化物溶液反应的离子方程式为_________。
④B和D的最高价氧化物的水化物的化学式分别为_________、_________,二者酸性前者_________(填“强于”或“弱于”)后者,原因是B和D的非金属性有差异,利用原子结构解释产生差异的原因: _________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用不仅可以提高综合效益,而且还能防止环境污染,生产流程如下:
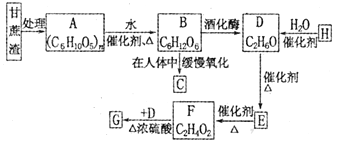
已知石油列解已成为生产H的重要方法,E的溶液能发生银镜反应,G是具有香味的液体,试填空。
(1)A的名称______;G的名称______。
(2)B的结构简式_______;H的结构简式____________。
(3)写出H发生加聚反应的方程式:_____________。
(4)D→E的化学方程式:_____________。
(5)E→F的化学方程式:_____________。
(6)F→G的化学方程式:_____________。
(7)写出G的同分异构体中与CH3COOH互为同系物的结构简式:____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某溶液中Cl-、Br-、I-的物质的量之比是2:3:4,要使溶液中的Cl-、Br-、I-的物质的量之比为4:3:2,则通入氯气的物质的量是原溶液I-的物质的量的( )
A. 1∕2 B. 1∕4 C. 1∕6 D. 1∕8
查看答案和解析>>
科目: 来源: 题型:
【题目】《化学与生活》
(1)合理膳食,保持营养均衡,是青少年学生健康成长的重要保证。
①蛋白质是人体必需的营养物质,它在人体内最终分解为( )。
A.葡萄糖 B.氨基酸 C.脂肪酸
②现有下列五种物质 A食盐 B食醋 C苹果汁 D葡萄糖 E青霉素,请按下列要求填空(填序号)。
富含维生素C的是 ;可直接进入血液,补充能量的是 ;应用最广泛的抗生素之一的是 ;即可作为调味剂,又可作为防腐剂的是 ;食用过多会引起血压升高、肾脏受损的 。
(2)材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
①居室装修所使的人造板材会释放出一种挥发性物质,长期接触会引起过敏性皮炎,免疫功能异常,该挥发性物质是( )。
A.酒精 B.蔗糖 C.甲醛
②一般情况下,合金比组成它的成分金属硬度 (填大、小)。
③常用来作半导体的物质是 (填化学式);用作食品保鲜膜的的高分子材料的结构简式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com