
科目: 来源: 题型:
【题目】反应N2O4(g) ![]() 2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )

A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.由状态B到状态A,可以用加热的方法
D.A、C两点气体的平均相对分子质量:A>C
查看答案和解析>>
科目: 来源: 题型:
【题目】已知298K时反应2SO2(g)+O2(g)═2SO3(g)△H=-197kJmol-1,在相同温度下向一密闭容器中加入2molSO2和1molO2,达化学平衡时放出热量为a1kJ;向另一容积相同的密闭容器中通入1molSO2和0.5molO2,达化学平衡时放出热量为a2kJ,则下列关系式中正确的是( )
A. 2a2>a1>197 B. 2a2<a1<197 C. 2a2=a1>197 D. 2a2=a1=197
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于合金的说法中错误的是
A. 铝合金中除Al外,还含有Cu、Mg、Si、Zn等
B. 生铁和钢都是铁碳合金
C. 我国在商代就已制造和使用的青铜器其成分主要是Cu-Zn合金
D. 金首饰中常加入一定量的Cu或Ag以增大硬度
查看答案和解析>>
科目: 来源: 题型:
【题目】2004年的诺贝尔化学奖授予以色列科学家阿龙·切哈诺夫、阿夫拉姆·赫什科和美国科学家欧文·罗斯,以表彰他们发现了泛素调节蛋白质水解。关于蛋白质的组成与性质的叙述正确的是
A. 蛋白质在酶的作用下水解的最终产物为氨基酸
B. 向蛋白质溶液中加入Na2SO4浓溶液,会使其变性
C. 天然蛋白质仅由碳、氢、氧、氮四种元素组成
D. 氨基酸和蛋白质都是只能和碱反应的酸性物质
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.烟道气中含有的CO和SO2是重要的污染物,可在催化剂作用下将它们转化为S(s)和CO2,此反应的热化学方程式为_____________________。
已知:CO(g) +1/2O2(g) = CO2(g) △H=-283.0kJ·mol-1;
S(s)+O2=SO2(g) △H=-296.0 kJ·mol-1
Ⅱ.氨的合成是最重要的化工生产之一。在2个恒压的密闭容器中,同温度下、使用相同催化剂分别进行反应:3H2(g)+N2(g)![]() 2NH3(g),按不同方式投入反应物,保持恒温,反应达到平衡时有关数据为:
2NH3(g),按不同方式投入反应物,保持恒温,反应达到平衡时有关数据为:
容 器 | 甲 | 乙 |
反应物投入量 | 3 mol H2、2 mol N2 | 6 mol H2、4mol N2 |
达到平衡的时间(min) | t | 5 |
平衡时N2的浓度(mol·L-1) | 3 | c |
(1)该反应的平衡常数表达式K=_______________。
(2)甲容器达到平衡所需要的时间t 5min(填“>”、“<” 或“=”);
Ⅲ.下表是不同温度下水的离子积数据:
温度/℃ | 25 | t1 | t2 |
Kw/ mol2·L-2 | 1×10-14 | a | 1×10-12 |
试回答以下几个问题:
(1)若25< t1< t2,则a________1×10-14(填“<”、“>”或“=”)。
(2)在25℃下,pH=10的NaOH溶液中,水电离产生的c(OH—)为:____________mol/L。
(3)在t2℃下,将pH=9的氢氧化钠溶液V1 L与pH=4的硫酸溶液V2 L混合(设混合后溶液体积为原两溶液体积之和)所得溶液的pH=7,则V1︰V2 = ___________
查看答案和解析>>
科目: 来源: 题型:
【题目】甲苯氧化法制备苯甲酸的反应原理如下:
![]() + 2KMnO4
+ 2KMnO4![]()
![]() +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O
![]() + HCl
+ HCl![]()
![]() +KCl
+KCl
实验时将一定量的甲苯和KMnO4溶液置于图1装置中,在100 ℃时, 反应一段时间,再停止反应,并按如下流程分离出苯甲酸和回收未反应的甲苯。


⑴实验室中实现操作Ⅰ所需的玻璃仪器有_____、烧杯;操作Ⅱ的名称为_____。
⑵如果滤液呈紫色,要先加亚硫酸氢钾,然后再加入浓盐酸酸化,若无此操作会出现的危害是_______________。
⑶在操作Ⅲ中,抽滤前需快速冷却溶液,其原因是__________;如图2所示抽滤完毕,应先断开_____之间的橡皮管。
⑷纯度测定:称取1.220 g产品,配成100 mL溶液,取其中25.00 mL溶液,进行滴定 ,消耗KOH物质的量为2.4×10-3mol。产品中苯甲酸质量分数为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】巧妙的实验设计有助于更好地解决问题。下列装置不能达到实验目的的是

A. 用装置甲验证HCl气体易溶于水
B. 用装置乙验证SO2具有漂白性
C. 用装置丙采集到的压强数据判断铁钉发生析氢腐蚀还是吸氧腐蚀
D. 用装置丁检验NH4Cl分解产生的气体
查看答案和解析>>
科目: 来源: 题型:
【题目】最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:
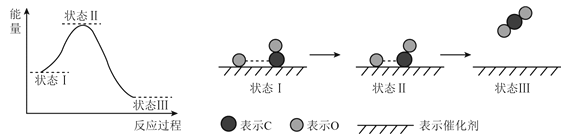
下列说法中正确的是
A.CO和O生成CO2是吸热反应
B.在该过程中,CO断键形成C和O
C.CO和O生成了具有极性共价键的CO2
D.状态Ⅰ→状态Ⅲ表示CO与O2反应的过程
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com