
科目: 来源: 题型:
【题目】下列物质的分类合理的是( )
A.氧化物:CO2、NO、SO2、H2O
B.碱:NaOH、KOH、Ba(OH)2、Na2CO3
C.铵盐:NH4Cl、NH4NO3、(NH4)2SO4、NH3H2O
D.碱性氧化物:Na2O、CaO、Mn2O7、Al2O3
查看答案和解析>>
科目: 来源: 题型:
【题目】[2015天津]下列有关“化学与生活”的叙述不正确的是
A.点燃爆竹后,硫燃烧生成SO3
B.中国古代利用明矾溶液的酸性清除铜镜表面的铜锈
C.服用阿司匹林出现水杨酸反应时,用NaHCO3溶液解毒
D.使用含钙离子浓度较大的地下水洗衣服,肥皂去污能力减弱
查看答案和解析>>
科目: 来源: 题型:
【题目】等温等压过程在低温下不能自发进行,而在高温下可自发进行的条件是
A. △H<0, △S<0 B. △H>0, △S<0 C. △H<0, △S>0 D. △H>0, △S>0
查看答案和解析>>
科目: 来源: 题型:
【题目】现有反应:①Ba(OH)2 8H2O+2NH4Cl═2NH3↑+BaCl2+10H2O,②Fe+H2SO4═FeSO4+ H2↑。试回答下列问题:
(1)两反应中属于吸热反应的是___________(填序号,下同〉,能设计成原电池的是_________。
(2)Fe-Cu原电池的装置如图所示。
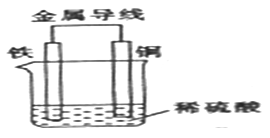
①铁作______(填“正极”或“负极”),溶液中H+向______ (填“铁”或“铜”)电极方向移动。
②正极的现象是___________,负极的电极反应式为____________。
③若反应过程中有0. 2 mol电子发生转移,则生成的氢气在标准状况下的体积为_______L。
查看答案和解析>>
科目: 来源: 题型:
【题目】(14分)工业上用闪锌矿(主要成分为ZnS,还含有Fe2O3等杂质)为原料生产ZnSO4·7H2O的工艺流程如下:
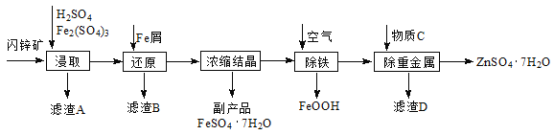
(1)滤渣A经CS2提取后可获得一种淡黄色副产品,其化学式为 。
(2)浸取过程中Fe2(SO4)3的作用是 。
(3)除铁过程控制溶液的pH在5.4左右,该反应的离子方程式为 。该过程在空气入口处设计了一个类似淋浴喷头的装置,其目的是 。
(4)置换法除重金属离子所用物质C为 。
(5)硫酸锌的溶解度与温度之间的关系如下表:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 41.8 | 54.1 | 70.4 | 74.8 | 67.2 | 60.5 |
从除重金属后的硫酸锌溶液中获得硫酸锌晶体的实验操作为 、 、过滤、干燥。
查看答案和解析>>
科目: 来源: 题型:
【题目】H2与O2、F2均能发生反应,下图为H2与F2发生反应生成HF过程中的能量变化示意图。请回答
下列问题:
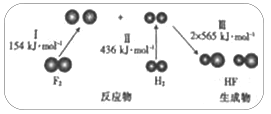
H2(g)与F2(g)反应生成HF(g)过程中的能量最变化
(1)完成转化I、II_________(填“吸收”或“放出”,下同)能量,完成转化Ⅲ_________能量。
(2)H2和F2反应的能量变化图可用___________(填“A”或“B”)表示。
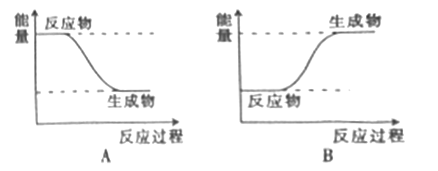
(3)H2在O2中燃烧的过程主要是__________能转化为_______能的过程。
查看答案和解析>>
科目: 来源: 题型:
【题目】某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见如图,电池总反应可表示为2H2+O2===2H2O,下列有关说法正确的是( )
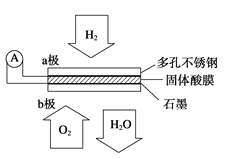
A.电子通过外电路从b极流向a极
B.b极上的电极反应式为O2+2H2O+4e-===4OH-
C.每转移0.1 mol电子,便消耗1.12 L的H2
D.H+由a极通过固体酸电解质传递到b极
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 在合成塔中加入3molH2与1molN2反应即可得到2molNH3
B. 工业上合成SO3时可加入过量空气以提高SO2的转化率
C. 利用Al、Mg、NaOH溶液、导线及电流计等可证明Al的金属活动性大于Mg的
D. 冰箱保存的食品不易变质,与化学反应速率无关
查看答案和解析>>
科目: 来源: 题型:
【题目】镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O![]() Cd(OH)2+2Ni(OH)2有关该电池的说法正确的是( )
Cd(OH)2+2Ni(OH)2有关该电池的说法正确的是( )
A.充电过程中镉元素被氧化
B.充电时阳极反应:Ni(OH)2-e—+ OH—=== NiOOH + H2O
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH—向正极移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com