
科目: 来源: 题型:
【题目】已知:25℃时,Ksp[Mg(OH)2]=2.0×10-11,Ksp[Mn(OH)2]=2.0×10-13。该温度下,关于含有Mg(OH)2和Mn(OH)2两种固体的悬浊液,下列说法正确的是
A. 溶液中的![]()
B. 若加入少量NaOH,Ksp[Mg(OH)2]和Ksp[Mn(OH)2]均减小
C. 若加入少量MgCl2,溶液中的c(Mg2+)和c(Mn2+)均增大
D. 若升高温度,Mg(OH)2和Mn(OH)2两种固体的质量均不变
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E为五种短周期元素,原子序数依次增大,原子半径按D、E、B、C、A的顺序逐渐减小。A、D位于同一主族,C、E位于同一主族;A、D的原子核内质子数之和为C、E的原子核内质子数之和的一半;B的氢化物与其最高价氧化物对应的水化物反应生成一种盐,D元素与其他四种元素均能形成离子化合物。试回答下列问题:
(1)E元素的离子结构示意图为_______;元素A、D形成的化合物的电子式为____________。
(2)比较元素C、E的氢化物沸点高低,HnC__ HnE (填“>”“<”)。解释原因(用化学式表示)__________________________________。
(3)B的氢化物与其最高价氧化物对应的水化物反应生成盐的化学方程式__________。
(4)由C、D、E中的两种元素组成的两种化合物发生的反应既属于化合反应又属于氧化还原反应,该反应的化学方程式为______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】被称为万能还原剂的NaBH4溶于水并和水反应:NaBH4+2H2O==NaBO2+4H2↑,下列说法中正确的是(NaBH4中H为-1价)
A. NaBH4既是氧化剂又是还原剂 B. NaBH4是氧化剂.H2O是还原剂
C. 硼元素被氯化,氢元素被还原 D. 被氧化的元素与被还原的元素质量之比为1:1
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室中需用2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是
A.950mL 111.2g B.500mL 117.0g
C.1000mL 117.0g D.1000mL 111.2g
查看答案和解析>>
科目: 来源: 题型:
【题目】将 4 molA气体和3molB气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)![]() 2C(g), 若经 2 s后测得 C的浓度为 0.6 molL-1,现有下列几种说法:
2C(g), 若经 2 s后测得 C的浓度为 0.6 molL-1,现有下列几种说法:
①用物质A 表示反应的平均速率为 0.3 molL-1s-1
②物质 B的体积分数是40%
③2 s 时物质 A 的转化率为30%
④2 s 时物质 B 的浓度为 1.0 molL-1
其中正确的是
A. ①④ B. ②③ C. ①③ D. ③④
查看答案和解析>>
科目: 来源: 题型:
【题目】熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是

A. 电池工作时,CO32-向电极B移动
B. 电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O
C. 电极B上发生的电极反应为:O2+2CO2+4e-=2CO32-
D. 反应CH4+H2O![]() 3H2+CO,每消耗1mol CH4转移12mol电子
3H2+CO,每消耗1mol CH4转移12mol电子
查看答案和解析>>
科目: 来源: 题型:
【题目】过氧化钙微溶于水,溶于酸,可作分析试剂、医用防腐剂、消毒剂。以下是一种制备过氧化钙的实验方法。回答下列问题:
(一)碳酸钙的制备
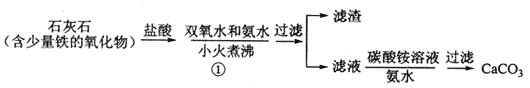
(1)步骤①加入氨水的目的是_______。小火煮沸的作用是使沉淀颗粒长大,有利于____。
(2)下图是某学生的过滤操作示意图,其操作不规范的是______(填标号)。
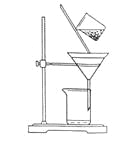
a.漏斗末端颈尖未紧靠烧杯壁
b.玻璃棒用作引流
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(二)过氧化钙的制备

(3)步骤②的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体,此时溶液呈____性(填“酸”、“碱”或“中”)。将溶液煮沸,趁热过滤。将溶液煮沸的作用是___________。
(4)步骤③中反应的化学方程式为________,该反应需要在冰浴下进行,原因是_________。
(5)将过滤得到的白色结晶依次使用蒸馏水、乙醇洗涤,使用乙醇洗涤的目的是_______。
(6)制备过氧化钙的另一种方法是:将石灰石煅烧后,直接加入双氧水反应,过滤后可得到过氧化钙产品。该工艺方法的优点是______,产品的缺点是_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在—定体积的密闭容器中,下列叙述能作为可逆反应A(S)+2B(g) ![]() C(g) +D (g)达到平衡状态标志的是
C(g) +D (g)达到平衡状态标志的是
A. 混合气题的平均分子量不再变化 B. 单位时间内消耗2a mol B,同时生成amol C
C. 2v正(B)=v逆(C) D. 混合气体的总压强不再变化
查看答案和解析>>
科目: 来源: 题型:
【题目】偶氮苯是橙红色晶体,溶于乙醇,微溶于水,广泛应用于染料制造和橡胶工业,以硝基苯、镁粉和甲醇为原料制备偶氮苯的实验步骤如下:
步骤1:在反应器中加入一定量的硝基苯、甲醇和一小粒碘,装上冷凝管,加入少量镁粉,立即发生反应。
步骤2:等大部分镁粉反应完全后,再加入镁粉,反应继续进行,等镁粉完全反应后,加热回流30 min。
步骤3:将所得液体趁热倒入冰水中,并不断搅拌,用冰醋酸小心中和至pH为4~5,析出橙红色固体,过滤,用少量冰水洗涤。
步骤4:用95%的乙醇重结晶。
(1)步骤1中反应不需要加热就能剧烈进行,原因是________________。镁粉分两次加入而不是一次性全部加入的原因是___________________ _____________________________________________________。
(2)步骤3中析出固体用冰水洗涤的原因是________________。若要回收甲醇,实验所需的玻璃仪器除冷凝管、酒精灯、牛角管(应接管)和锥形瓶外还应有________________________________________________________________。
(3)取0.1 g偶氮苯,溶于5 mL左右的苯中,将溶液分成两等份,分别装于两个试管中,其中一个试管用黑纸包好放在阴暗处,另一个则放在阳光下照射。用毛细管各取上述两试管中的溶液点在距离滤纸条末端1 cm处,再将滤纸条末端浸入装有1∶3的苯环己烷溶液的容器中,实验操作及现象如下图所示:
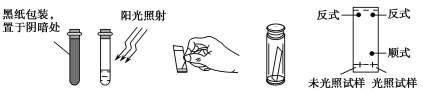
①实验中分离物质所采用的方法是________法。
②由实验结果可知:________________;利用该方法可以提纯反式偶氮苯。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com