
科目: 来源: 题型:
【题目】(1)有下列五种烃:①![]() ②
②![]() ③乙烷④正戊烷⑤
③乙烷④正戊烷⑤![]() ⑥
⑥![]() ,
,
其中互为同分异构体的是_________(填序号),② ③ ④ ⑤四种物质按它们的沸点由高到低的顺序排列正确的是______________(填序号),等质量的①③⑥三种物质,完全燃烧时消耗O2的物质的量由多到少的顺序为_________。
(2)按系统命名法, 化合物(CH3)2CHCH(CH3)C(C2H5)2C(CH3)3的名称是___________,该烃可由_______种烯烃加成而得到.
(3)分子式为C5H9C1O2的同分异构体甚多,其中能与NaHCO3发生反应产生CO2的同分异构体共有________种;
(4)有机物M分子式为C4H8O3,同温同压下,等质量的M分别与足量的金属钠、NaHCO3溶液反应,可得到等量的气体;在浓硫酸存在下,M还能生成一种分子式为C4H6O2的五元环状化合物N。根据上述性质,确定C4H8O3的结构简式为________________,写出M→N对应的化学方程式_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】燃料电池是利用燃料(如CO、H2、CH4等)与氧气反应,将反应产生的化学能转变为电能的装置,通常用氢氧化钾作为电解质溶液。完成下列关于甲烷(CH4)燃料电池的填空:
(1)甲烷与氧气反应的化学方程式为:
(2)已知燃料电池的总反应式为CH4+2O2+2KOH=K2CO3+3H2O,电池中有一极的电极反应为CH4+10OH--8e-= CO32-+7H2O,这个电极是燃料电池的 (填“正极”或“负极”),另一个电极上的电极反应式为:
(3)随着电池不断放电,电解质溶液的碱性 (填“增大”、“减小”或“不变”)
(4)通常情况下,甲烷燃料电池的能量利用率 (填“大于”、“小于”或“等于”)甲烷燃烧的能量利用率。
查看答案和解析>>
科目: 来源: 题型:
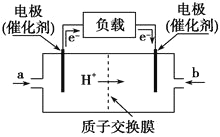
【题目】如图是甲醇燃料电池的构造示意图,该电池总反应式为:2CH3OH+3O2=2CO2+4H2O。下列有关该电池的说法不正确的是( )
A.等量的甲醇通过燃料电池释放的电能比其通过火力发电产生的电能多
B.左边的电极为电池的负极,a处通入的是甲醇
C.电池负极的反应式为:2CH3OH+2H2O-12e-=2CO2↑+12H+
D.若用池电池电解足量饱和食盐水(石墨电极),消耗1mol甲醇时,产生标况下44.8L氢气
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求回答下列问题:
(1)配制FeCl3溶液时,需将固体溶于较浓的盐酸后按需要进行稀释,用离子方程式解释其原因 。
(2)用离子方程式表示出泡沫灭火器的原理 。
(3)实验室中常用NaOH溶液来进行洗气和提纯,当100mL 3mol·L-1的NaOH溶液吸收标准状况下4.48LCO2时,所得溶液中离子浓度由大到小的顺序为 。
(4)常温下,浓度均为0.1mol/L的下列五种溶液的PH值如下表所示:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
①根据表中数据,将浓度均为0.01mol· L-1的下列四种酸的溶液分别稀释100倍,pH变化最小的是 。
A.HCN B.HClO C.H2CO3 D.CH3COOH
②根据以上数据,判断下列反应可以成立的是 。
A.CH3COOH+Na2CO3═NaHCO3+CH3COONa
B.CH3COOH+NaCN═CH3COONa+HCN
C.CO2+H2O+2NaClO═Na2CO3+2HClO
D.NaHCO3+HCN═NaCN+H2O+CO2
(5)已知在Cu2+、Mg2+、Fe2+浓度相同的溶液中,其开始沉淀时的pH如下:
离子 | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
若向该溶液中滴加NaOH溶液,则先沉淀的是 (填离子符号),
判断Ksp[Fe(OH)2] Ksp[Mg(OH)2](填“>”、“=”或“<”)。
已知Ksp[Cu(OH)2]=2.5×10-20,若向该溶液中加入生石灰调节其pH,当pH= 时,溶液中Cu2+沉淀完全。[已知1g2=0.3]
查看答案和解析>>
科目: 来源: 题型:
【题目】“文化自信”是我党提出的四大自信之一。古诗词是我国重要的文化遗产,下列诗句中加点字部分涉及氧化还原反应的是( )
A. 月波成露露成霜,借与南枝作淡妆 B. 春蚕到死丝方尽,蜡炬成灰泪始干
C. 粉身碎骨浑不怕,要留清白在人间 D. 莫道雪融便无迹,雪融成水水成冰
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极).下列分析正确的是

A. a 电极发生反应:H2NCH2CH2NH2+16e-+4H2O==2CO2↑+N2↑+16H+
B. 质子交换膜处H+由右向左移动
C. 该电池在微生物作用下将化学能转化为电能
D. 开始放电时b极附近pH不变
查看答案和解析>>
科目: 来源: 题型:
【题目】2016年10月17日我国神舟十一号载人飞船在酒泉卫星发射中心成功发射,为我们更好地掌握空间交会对接技术、开展地球观测活动奠定了基础。我国制造航天飞船的主要材料是铝,因而其也被称为会飞的金属,请根据其性质回答下列问题:
(1)现在工业冶炼铝的化学方程式为 。
(2)铝锂合金是今年来航空金属材料中发展最为迅速的一个领域,主要因为合金的某些性能优于各成分金属,其中包括 、 等方面。同时铝锂形成化合物LiAlH4既是金属储氢材料又是有机合成中的常用试剂,遇水能得到无色溶液并剧烈分解释放出H2,LiAlH4在化学反应中通常作
(填“氧化”或“还原”)剂。
(3)铝电池性能优越,在现代生产、生活中有广泛的应用。
①Al-Ag2O电池可用作水下动力电源,化学反应为2Al+3Ag2O+2NaOH=2NaAlO2+6Ag+H2O,则负极的电极反应式为 ,正极附近溶液的pH (填“变大”“不变”或“变小”),
②铝一空气电池以其环保、安全而受到越来越多的关注,其原理如下图所示。
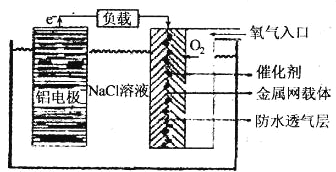
该电池的负极反应方程式为 ;正极反应方程式为 ;
电池中NaCl溶液的作用是 ;以该电池为电源,用惰性电极电解Na2SO4溶液,当Al电极质量减少1.8g时,电解池阴极生成的气体在标准状况下的体积为 L。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E均是短周期元素,其原子序数依次增大,A和B同周期,A和D同主族,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的阴离子与C的阳离子电子层结构相同,C的单质与B的单质在不同条件下反应,可生成C2B或C2B2,E是所在周期中原子半径最小的元素。请回答:
(1)D在元素周期表中的位置是 。
(2)C2B的电子式是 ;AB2的结构式是 。
(3)B、C、E的离子半径由大到小的顺序为 (用化学式回答,下同);A、D、E元素最高价氧化物对应水化物的酸性由强到弱为 。
(4)B的气态氢化物与H2S相比沸点高的是 (用化学式回答);原因是 。
(5)水中锰含量超标,容易使洁具和衣物染色,使水产生异味,EB2可以用来除去水中超标的Mn2+,生成黑色沉淀MnO2,当消耗13.50gEB2时,共转移了1mol电子,则反应的离子方程式: 。
查看答案和解析>>
科目: 来源: 题型:
【题目】向BaCl2溶液中依次通入过量的下列气体,第一次无沉淀,第二次有沉淀的组合是
选项 | A | B | C | D |
第一次 | CO2 | NO | NO2 | SO2 |
第二次 | SO2 | CO2 | CO2 | NO2 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com