
科目: 来源: 题型:
【题目】某化学小组对Na2SO3和AgNO3在不同pH下的反应及产物,进行了以下实验探究。
查阅资料:
Ⅰ.Ag2SO3:白色、难溶于水;
Ⅱ.Ag2O:棕黑色、难溶于水,易与酸溶液反应。
(1)根据资料:①通常情况Na2SO3溶液和AgNO3溶液反应产生的现象是________。
②若Ag2O与盐酸反应,其化学方程式应为___________。
(2)检测溶液pH:①0.1mol/LAgNO3溶液的pH=5,引发这一结果的微粒是________。
②0.1mol/LNa2SO3溶液的pH=10,其原因用离子方程式解释是________。
(3)实验探究:在不同pH条件下Na2SO3溶液与AgNO3溶液混合反应。
实验记录如下:

Ⅰ.实验a中沉淀溶解消失的原因,可能是___________。
Ⅱ.Ag2SO3在溶液中沉淀析出的大致pH范围是_________。
Ⅲ.将d中棕黑色絮状物X滤出、洗净、进行实验分析:
实验 | 操作 | 现象 |
ⅰ | 将其置于试管中加稀盐酸、观察 | 无明显现象 |
ⅱ | 将其置于试管中加足量浓硝酸、观察 | 立即产生红棕色气体 |
ⅲ | 在ⅱ反应所得溶液中,加Ba(NO3) 2溶液、观察,再加BaCl2、观察 | 前者无明显现象,后者出现白色沉淀 |
①由实验ⅰ得出的结论是_________。
②d中的棕黑色絮状物X是_________。
③实验ⅱ中的化学反应方程式是___________。
(4)小组认为在酸性条件下,SO32-的________性增强,生成X的化学方程式是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】选用一种试剂除去下列各物质中的杂质(括号内为杂质),把所选试剂的化学式填在横线上,并写出离子方程式。
(1)BaCl2(HCl)试剂 ;离子方程式为 ;
(2)CO(CO2)试剂 ;离子方程式为 ;
查看答案和解析>>
科目: 来源: 题型:
【题目】以Na2SO3溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性。
实验 | 试剂 | 现象 | |
滴管 | 试管 | ||
2 mL | 0.2 mol·L1 Na2SO3溶液 | 饱和Ag2SO4溶液 | Ⅰ.产生白色沉淀 |
0.2 mol·L1 CuSO4 | Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀 | ||
0.1 mol·L1 Al2(SO4)3溶液 | Ⅲ.开始无明显变化,继续滴加产生白色沉淀 | ||
(1)经检验,现象Ⅰ中的白色沉淀是Ag2SO3。用离子方程式解释现象Ⅰ:____________。
(2)经检验,现象Ⅱ的棕黄色沉淀中不含SO42,含有Cu+、Cu2+和SO32。
已知:Cu+![]() Cu +Cu2+,Cu2+
Cu +Cu2+,Cu2+![]() CuI↓(白色)+I2。
CuI↓(白色)+I2。
①用稀硫酸证实沉淀中含有Cu+的实验现象是_____________。
②通过下列实验证实,沉淀中含有Cu2+和SO32。
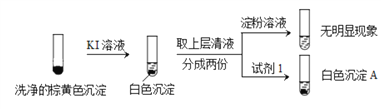
a.白色沉淀A是BaSO4,试剂1是____________。
b.证实沉淀中含有Cu+和SO32的理由是_______________。
(3)已知:Al2(SO3)3在水溶液中不存在。经检验,现象Ⅲ的白色沉淀中无SO42,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
①推测沉淀中含有亚硫酸根和____________。
②对于沉淀中亚硫酸根的存在形式提出两种假设:i. Al(OH)3所吸附;ii.存在于铝的碱式盐中。对假设ii设计了对比实验,证实了假设ii成立。
将对比实验方案补充完整。
步骤一:
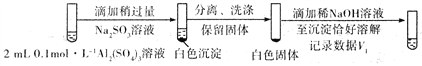
步骤二:

则V1___________V2(填>,<或=)。
(4)根据实验,亚硫酸盐的性质有___________。盐溶液间反应的多样性与__________有关。
查看答案和解析>>
科目: 来源: 题型:
【题目】胶体区别与其他分散系的本质特征是( )
A.能发生丁达尔现象
B.胶体粒子能通过滤纸空隙
C.胶体在一定条件下能稳定存在
D.胶体分散质粒子直径在1nm~100nm之间
查看答案和解析>>
科目: 来源: 题型:
【题目】有关氧化还原反应实质的说法中正确的是 ( )
A.是否有原子的重新组合 B.是否有元素的化合价的变化
C.是否有氧元素的参加 D.是否有元素原子的电子转移
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于细胞中元素和化合物的叙述,正确的是
A. 蛋白质和核酸都主要在细胞核中合成
B. 除核糖体和中心体外,其他各种细胞器均含磷脂成分
C. 内质网和高尔基体的各种成分的含量相同
D. 能源物质都是糖类,所有的糖类都是能源物质
查看答案和解析>>
科目: 来源: 题型:
【题目】将 4 mol A 气体和 2 mol B 气体在 2 L 的密闭容器中混合并在一定条件下发生如下反应2A(g)+B(g)![]() 2C(g);△H <0。4 s(秒)后反应达到平衡状态,此时测得 C 的浓度为0.6 mol·L-1。下列说法中正确的是
2C(g);△H <0。4 s(秒)后反应达到平衡状态,此时测得 C 的浓度为0.6 mol·L-1。下列说法中正确的是
A. 当A、B、C物质的量浓度之比为2:1:2时,反应即达到平衡状态
B. 4s内用物质B表示的反应速率为0.075mol·L-1·s-1
C. 达平衡后若通入一定量氦气,A的转化率降低
D. 达平衡后若升高温度,C的浓度将增大
查看答案和解析>>
科目: 来源: 题型:
【题目】某气态烃A 与 H2的相对密度为14,其产量可以用来衡量一个国家的石油化工发展水平。以该化合物为原枓合成化合物G、E和I的流程如下:
已知:Ⅰ.芳香族化合物F为C、H、O化合物,其相对分子质量为166,环上的一氯代物有一种,1 mol F与足量NaHCO3溶液反应能生成2 mol CO2,F与足量B反应生成G。
Ⅱ.H为二元醇,其蒸气密度折算成标准状况为2.77 g/L,H与足量D反应生成I。
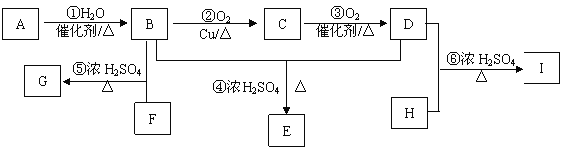
(1)A的电子式为____________________,E的结构简式____________________________________。
(2)G的分子式为______________,反应⑤的反应类型为________________。
(3)写出下列化学方程式:
②__________________________________________________________________;
⑥_______________________________________________________________;
查看答案和解析>>
科目: 来源: 题型:
【题目】研究发现:一节电池烂在地里,能够使一平方米的土地失去利用价值。废旧电池的危害上要集中在其中所含的少量重金属上。将废旧锌锰电池回收处理,既能减少它对环境的污染,又能实现废电池的资源化利用。
(1)回收填料中的二氧化锰和氯化铵。已知:废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水。回收物质的流程如图所示。

① 操作中先将电池填料研碎的目的是:________________。
② 操作l和操作2的名称都是___________,该操作中玻璃棒的作用是___________。
③ 灼烧滤渣l的目的是______________________。
(2)回收二氯化锰:将废旧锌锰电池处理,得到含锰混合物,向该混合物加入浓盐酸并加热。
①写出MnOOH与浓盐酸反应的化学方程式:________________。
② 锰回收新方法:向废旧锌锰电池内的混合物[主要成分MnOOH、Zn(OH)2]中加入一定量的稀硫酸和稀草酸(H2C2O4),并不断搅拌至无CO2产生为止,写出MnOOH参与反应的化学方程式______________。与使用浓盐酸回收锰相比,新方法的优点是___________(答l点即可)。
(3)用废电池的锌皮可用于回收制作ZnSO4·7H2O。过程中,需除去锌皮中的少量杂质铁,其方法是:常温下,加入稀H2SO4和H2O2,铁溶解变为Fe3+,加碱调节pH为4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中c(Fe3+)=_________。继续加碱调节pH为____时,锌开始沉淀(假定Zn2+浓度为0.1mol/L)。部分难溶的电解质溶度积常数(Ksp)如下表:
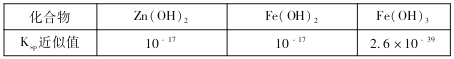
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com