
科目: 来源: 题型:
【题目】合金是一类非常重要的金属材料,在生产、生活、军事或高科技领域中都有广泛应用。铁铝合金是一种新型的高温结构材料。
(1)写出工业上生产铁和铝的化学方程式(只写最后得到金属单质的反应):________________________。
(2)高温条件下,Al和Fe2O3按一定比例混合反应可制得Fe3Al,写出该反应的化学方程式:_______________________________。
(3)如图表示室温时不同组分的Fe3Al在65%的浓硝酸中的腐蚀情况。由图可看出添加了________(填符号)元素的合金耐腐蚀性最差。
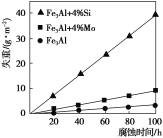
(4)某校兴趣小组欲测定另一种铁铝硅合金(FexAlySiz)粉末的组成。
①小明同学提出如下方案:准确称取1.46 g该合金粉末,再加入足量NaOH溶液(Si+2NaOH+H2O===Na2SiO3+2H2↑),充分反应后过滤,通过测定剩余固体质量及收集到气体的体积,可计算出此合金的组成。写出Al与NaOH溶液反应的离子方程式:______________________________。
②小军同学认为小明同学的方案难以测定标准状况下气体的体积,操作不简便。于是他设计了第二种方案:准确称取1.46 g该合金粉末,加入过量盐酸溶液充分反应后过滤,测定剩余固体质量0.07 g。向滤液中滴加足量浓NaOH溶液,充分搅拌、过滤、洗涤得固体。再将所得固体充分加热、灼烧得红棕色粉末1.60 g。试通过计算确定此合金的组成。
查看答案和解析>>
科目: 来源: 题型:
【题目】己知水在25℃和95℃时,其电离平衡曲线如图所示。
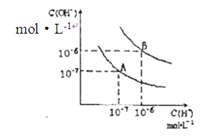
(1)则95℃时水的电离平衡曲线应为_____(填“A”或“B”),理由是_____。
(2)曲线A对应温度下,pH=2的HCl溶液和pH=12的某BOH溶液中,若水的电离程度分别用a1、a2表示,则a1________ a2 (填“大于”、“小于”、“等于”或“无法确定”,下同),若将二者等体积混合,则混合溶液的PH ______7。
(3)在曲线B所对应的温度下,将0.02mol·L-1的Ba (OH)2溶液与等物质的量浓度的NaHSO4 溶液等体积混合,所得混合液的PH=_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:

(1)写出下列元素的名称⑩________。
(2)在①~⑩元素中,金属性最强的元素是_______(填元素符号)。
(3)甲、乙是上述元素形成的两种气态氢化物,且甲、乙分子含有相同数目的电子,二者相互反应生成化合物丙,丙是离子化合物,且其阴、阳两种离子所含电子数都与甲、乙分子相同。若甲的相对分子质量比乙的小,则甲的气态氢化物与其最高价氧化物对应的水化物反应的化学方程式_____________________________________________ ,丙中所含有的化学键类型有__________________________。
(4)元素⑤、⑥、⑨的最高价氧化物的对应水化物中,两两间能发生反应的有关离子方程式分别为_____________________________、 _____________________________ 。
(5)下列事实中,能够判断元素⑥、⑦的非金属性强弱的是_________。
a.元素⑥单质的熔点比元素⑦单质的熔点高
b.元素⑦的氢化物比元素⑥的氢化物稳定
c.元素⑥与⑨形成的化合物能与元素⑦的氢化物的水溶液反应,生成元素⑥的氢化物
d.一定条件下元素⑥和元素⑦的单质分别与Fe反应时,产物中铁元素的价态不同
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。
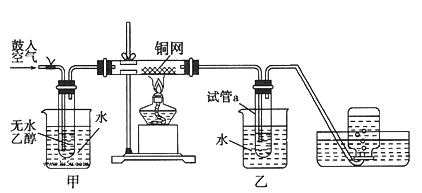
(1)实验过程中铜网出现黑色和红色交替的现象,请写出相应的化学方程式:
________________________,_____________________________ 。
在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是_____反应。
(2)甲和乙两个水浴作用不相同。甲的作用是___________;乙的作用是____________。
(3)反应进行一段时间后,试管a中能收集到不同的物质,它们是____________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有_____(填写名称)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(10分)Ⅰ.1100 ℃时,体积为2L的恒容容器中发生如下反应:Na2SO4(s)+4H2 (g)![]() Na2S(s)+4H2O(g)
Na2S(s)+4H2O(g)
(1)下列能判断反应达到平衡状态的是________。
A.容器内气体压强不再变化
B.H2的体积分数不再变化
C.1 mol H-H键断裂同时2 mol H-O键形成
D.Na2S的质量不再变化
E.υ(正)=υ(逆)
F.容器内气体密度不再变化
(2)若2 min时反应达平衡,此时气体质量增加8 g,则用H2表示该反应的反应速率为: 。
Ⅱ.丙烷燃料电池,以KOH溶液为电解质溶液。
(3)通入丙烷的电极为_____(填“正极”或“负极”),正极的电极反应式为 。
(4)燃料电池的优点________。
(5)若开始时电解质溶液中含KOH的物质的量为0.25 mol,当溶液中K2CO3的物质的量为0.1 mol时,消耗标准状况下丙烷的体积为 mL(保留一位小数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】铵明矾是一种广泛应用于医药、食品、污水处理等多个行业的重要化工产品。以高岭土(含SiO2、Al2O3、少量Fe2O3等)为原料制备硫酸铝晶体[Al2(SO4)3·18H2O]和铵明矾[NH4Al(SO4)2·12H2O]的工艺流程如下图所示。
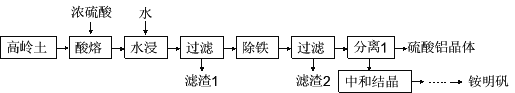
请回答下列问题:
(1)高岭土首先需要灼烧,实验室灼烧高岭土所需的实验仪器有 (填字母)。
a.蒸发皿 b.泥三角 c.漏斗 d.酒精灯 e.三脚架 f.坩埚 g.烧杯 h.试管
(2)研究发现,随着酸熔温度升高,氧化铝的溶出率增大,但若酸熔时温度过高(超过240℃),SiO2不仅会消耗硫酸,导致氧化铝溶出率下降,还会同时产生高温的腐蚀性气体,该副反应的化学方程式为 。
(3)要检验除铁后的滤液中是否含有Fe3+,应采取的实验方法为 ;滤渣2的主要成分为 (填化学式)。
(4)“分离1”操作包含的实验步骤有 、 、 、洗涤、干燥。
(5)中和结晶操作是将过滤出硫酸铝晶体后的滤液,先用硫酸调节酸铝比(溶液中游离硫酸和硫酸铝的物质的量之比),再用氨水中和至一定的pH值即可析出铵明矾晶体,写出该过程中的总反应方程式 。
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机物分子式为C4H8,据此推侧其结构和性质不可能的是( )
A.它与乙烯可能是同系物
B.一氯代物可能只有一种
C.分子结构中甲基的数目可能是0、1、2
D.等质量CH4和C4H8分别在氧气中完全燃烧,CH4的耗氧量小于C4H8
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于乙炔制取的说法不正确的是
A. 反应后溶液呈碱性
B. 此反应是放热反应
C. 为了除去杂质气体,可用硫酸铜溶液
D. 为了加快反应速率可用饱和食盐水代替水反应
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学反应属于氧化还原反应且水既不作氧化剂又不作还原剂的是( )
A. CaO+H2O=Ca(OH)2
B. NaH+H2O=NaOH+H2↑
C. 3NO2+H2O=2HNO3+NO
D. 2H2O+2F2=4HF+O2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com