
科目: 来源: 题型:
【题目】下列有关海水综合利用的说法正确的是( )
A.电解熔融的氯化镁可制备镁单质和氯气
B.从海水制食盐主要是通过化学变化完成
C.电解氯化铝可以制得铝单质和氯气
D.从海水中提取钠单质只发生物理变化
查看答案和解析>>
科目: 来源: 题型:
【题目】在无色透明的强酸性溶液中,能大量共存的离子组是( )
A.K+、SO42-、CO32-、Na+ B.Ca2+、NO3-、Al3+、Cl-
C.Fe3+、Cu2+、K+、OH- D.MnO4-、K+、SO42-、Na+
查看答案和解析>>
科目: 来源: 题型:
【题目】中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。CO2可转化成有机物实现碳循环。在体积为1L的密闭容器中,充入 1mol CO2和3mol H2,一定条件下反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如下图所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如下图所示。

(1)从3 min到9 min,υ(H2)=________mol·L-1·min-1。
(2)能说明上述反应达到平衡状态的是____________(填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1∶1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)平衡时CO2的转化率为______________。
(4)平衡时混合气体中CH3OH(g)的体积分数是__________________。
(5)一定温度下,第9分钟时υ逆(CH3OH) _______(填“大于”、“小于”或“等于”)第3分钟时υ正(CH3OH)。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是一个化学过程的示意图。

(1)图中甲池是________装置(填“电解池”或“原电池”),其中OH-移向________极(填“CH3OH”或“O2”)。
(2)写出通入CH3OH的电极的电极反应式:____________________。
(3)向乙池两电极附近分别滴加适量紫色石蕊试液,附近变红的电极为________极(填“A”或“B”),并写出此电极的反应式:________________。
(4)乙池中总反应的离子方程式:________________________。
(5)常温下,当乙池中B(Ag)极的质量增加5.40 g时,乙池的pH是________(若此时乙池中溶液的体积为500 mL);此时丙池某电极析出1.60 g某金属,则丙中的某盐溶液可能是________(填序号)。
a.MgSO4 B.CuSO4
c.NaCl D.AgNO3
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示的装置中,若通入直流电5 min时,铜电极质量增加2.16 g。
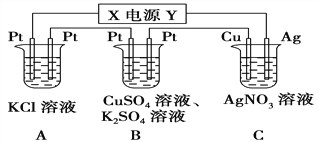
(1)电源电极X的名称为________。
(2)pH变化:A_______,B_______,C_______。(填“增大”“减小”或“不变”)
(3)通电5 min后,B中共收集224 mL气体(标准状况),溶液体积为200 mL,则通电前CuSO4溶液的物质的量浓度为______________(设电解前后溶液体积无变化)。
(4)若A中KCl溶液的体积也是200 mL,电解后,溶液的pH为_______(设电解前后溶液体积无变化)
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)铅蓄电池放电时的电池反应为PbO2+Pb+H2SO4=2PbSO4+2H2O,请写出铅蓄电池正极的电极反应式_____________________________________;
(2)汽车尾气分析仪对CO的分析以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质中自由移动。下列说法错误的是_________。

A.负极的电极反应式为:CO+O2-―2e—=CO2
B.工作时电极b作正极,O2-由电极a流向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,尾气中CO的含量越高
(3)某新型铝—空气燃料电池,以铝为负极,在正极通入空气,若以NaCl溶液或NaOH溶液为电解质溶液,放电时正极反应都为O2+2H2O+4e-=4OH-。那么若以NaOH溶液为电解质溶液,电池负极反应为____________________________________________;若以NaCl溶液为电解质溶液,则总反应为:________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一密闭容器中进行反应:2SO2(g)+O2(g) ![]() 2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,当反应达到平衡时,可能存在的数据是
2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,当反应达到平衡时,可能存在的数据是
A.SO2为0.4 mol·L-1,O2为0.2 mol·L-1 B.SO2为0.25 mol·L-1
C.SO2、SO3均为0.15 mol·L-1 D.SO3为0.4 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】决定物质性质的重要因素是物质结构。请回答下列问题:
(1)某Cr的配合物K[Cr(C2O4)2(H2O)2]中,配体有____种,配位原子是______;与C2O42-互为等电子体的分子是_______(填化学式);
(2)CaO晶胞如图所示,CaO晶体和NaCl晶体的晶格能分别为:CaO:3401kJ/mol、NaCl:786kJ/mol。导致两者品格能差异的主要原因____________。
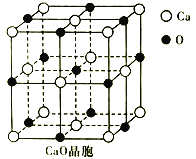
(3)汽车安全气囊的产生药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质,在NaN3固体中,阴离子的立体构型为________。
(4)从不同角度观察MoS2的晶体结构(见下图)。已知:①MoS2结构和石墨相似,具有层状结构;② Mo元素基态原子的价电子排布式为4d55s1。
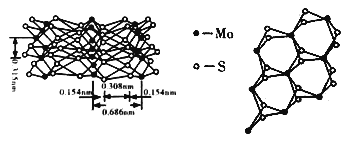
① 下列说法正确的是__ ;
A.晶体硅中硅原子的轨道杂化类型为sp2
B.电负性:S
C.晶体硅和C60比较,熔点较高的是C60
D.Mo位于第五周期ⅥB族E. MoS2的晶体中每个Mo原子周围距离最近的S原子数目为4
F. MoS2的晶体中Mo-S之间的化学键为极性键、配位键和范德华力
② 根据MoS2的晶体结构回答:MoS2纳米粒子具有优异的润滑性能,其原因是________。
(5)砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是普通灯泡的100倍,而耗能只有其10%,推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措。已知砷化稼的晶胞结构如图,晶胞参数a=565 pm。则砷化镓的晶胞密度____g/cm3(列式表示,不需计算结果), n位置Ga原子与m位置As原子之间的距离为____pm(列式表示)。

查看答案和解析>>
科目: 来源: 题型:
【题目】下列事实不能用元素周期律解释的是( )
A.酸性:HClO4>H2SO4
B.Na、Mg与水反应,Na更剧烈
C.气态氢化物的稳定性:HF>HCl
D.向Na2SO3溶液中加盐酸,有气泡产生
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.BaSO4难溶于水,所以BaSO4不是电解质[
B.SO2溶于水所得溶液可以导电,所以SO2是电解质
C.分散系一定是混合物
D.电解质的电离需要通电才能进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com