
科目: 来源: 题型:
【题目】下表列出了周期表中前20号元素中的十种元素的相关数据:
元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
原子半径(10-10m) | 1.52 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
最高价态 | +1 | +1 | — | +3 | +4 | +5 | +7 | +1 | +5 | — |
最低价态 | — | — | -2 | — | -4 | -3 | -1 | — | -3 | -1 |
试回答下列问题:
(1)以上10种元素的原子中,最容易失去电子的是________(填元素符号),与H2最容易化合的非金属单质是________(写物质名称)。
(2)若⑨形成的简单氢化物为A,⑥形成的简单氢化物为B,则二者的沸点A______B(填“大于”或“小于”)
(3)写出元素③形成的一种具有强氧化性的氢化物的电子式______________。
(4)写出上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的一种物质的分子式______________;⑤的最高价氧化物的结构式为__________。
(5)写出④的最高价氧化物的水化物与⑦的最高价氧化物的水化物反应的化学反应方程式:________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】铝是一种重要的金属,在生产、生活中具有许多重要的用途,如图是从铝土矿中制备铝的工艺流程:

已知:(1)铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
(2)溶液中的硅酸钠与偏铝酸钠反应,能生成硅铝酸盐沉淀,化学反应方程式为2Na2SiO3+2NaAlO2+2H2O=Na2A12Si2O8↓+4NaOH。请回答下列问题:
(1)铝土矿中Al2O3与氢氧化钠溶液反应的离子方程式为_________________________________。
(2)在工艺流程中“酸化”时,加入的最佳物质B是________,理由是_______________________,写出酸化过程发生反应的化学方程式:________________________________。
(3)工业上用Al2O3与C、Cl2在高温条件下反应制取AlCl3,理论上每消耗6.0 g碳单质,转移1 mol电子,则反应的化学方程式为__________________________________。
(4)某同学推测铝与氧化铁发生铝热反应得到的熔融物中还含有Fe2O3,设计了如下方案来验证:取一块该熔融物投入少量稀硫酸中,反应一段时间后,向反应后的混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有Fe2O3。
则物质甲是_________(填化学式),请判断该同学设计的实验方案的合理性_________(填“合理”或“不合理”)。原因是_______________________________________(若合理,则不用填写)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是( )
A.126C和146C互为同位素
B.金刚石和石墨互为同素异形体
C.CH3COOCH2CH3和CH3CH2CH2COOH互为同分异构体
D.CH4和CH3Cl互为同系物
查看答案和解析>>
科目: 来源: 题型:
【题目】外围电子排布式为4f75d16s2的元素在周期表中的位置应是
A. 第四周期第ⅦB族 B. 第五周期第ⅢB族 C. 第六周期第ⅦB族 D. 第六周期第ⅢB族
查看答案和解析>>
科目: 来源: 题型:
【题目】FeBr2是一种黄绿色固体,某学习小组制备并探究它的还原性。
I.实验室制备FeBr2
实验室用下图所示装置制取溴化亚铁。其中A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管。e是两只耐高温的瓷皿,其中盛有细铁粉。
实验开始时先将铁粉加热至600℃~700℃,然后将干燥、纯净的CO2气流通入D中,E管中反应开始,不断将d中液溴滴入约120℃的D中,经过几小时的连续反应,在E管的一端沉积有黄绿色鳞片状溴化亚铁。
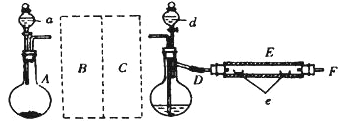
请回答:
(1)仪器D的名称是__。给D加热最好选择下列加热器中的__。

(2)若在A中烧瓶中盛固体CaCO3,a中盛6mol·L-1盐酸,为使导入D中的CO2为干燥纯净的气体,则图中B、C处的装置所装的试剂是:B为_______,C为_______。为防止污染空气,实验时应在F处连接盛有__ 溶液的尾气吸收装置。
(3)实验时,装置D和E的橡胶管用铝箔包住,且连接D、E之间的橡胶管可能短的原因是______。
(4)①E管反应前先通入一段时间CO2,其主要作用是________;
②反应过程中要继续通入CO2,其主要作用是________。
II.探究FeBr2的还原性
某课外小组学生对Cl2与 FeBr2溶液反应进行实验探究。
操作 | 现象 |
取0.1mol/L的FeBr2溶液100mL,测溶液的pH | pH试纸变红(约为4) |
| i. 开始通入100mLCl2(折合标班状况),溶液由浅绿色逐渐变黄; ii.稍后,继续通入Cl2,溶液黄色加深,变为棕黄色; iii.稍后,溶液由棕黄色变浅,最终变为黄色 |
(5)现象i中溶液由浅绿色逐渐变黄。某学生猜测可能原因:①Cl2将Fe2+氧化为Fe3+、使溶液呈黄色;②Cl2将Br-氧化为Br2,使溶液呈黄色。
请设计实验证明现象i中溶液由浅绿色变黄色的原因是原因①还是原因②:___________。
(6)若向上述FeBr2溶液中通入168mLCl2(标准状况),则反应的离子方程式为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,将3 mol A和1 mol B两种气体混合于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g)。2 min末该反应达到平衡,测得生成0.8 mol D, 0.4 mol C。下列判断不正确的是
xC(g)+2D(g)。2 min末该反应达到平衡,测得生成0.8 mol D, 0.4 mol C。下列判断不正确的是
A. x =1
B. 2 min时,A的浓度为0.9mol·L-1
C. 2 min内A的反应速率为0.3 mol·L-1·min-1
D. B的转化率为60%
查看答案和解析>>
科目: 来源: 题型:
【题目】I. 用![]() 表示原子:
表示原子:
(1)中性原子的中子数N=_______________。
(2)AXn+共有x个电子,则该阳离子的中子数N=___________。
(3)AXn-共有x个电子,则该阴离子的中子数 N=___________。
(4)12C16O2分子中的中子数N=______________。
II. 将Zn棒和Cu棒用导线连接后,放入硫酸铜溶液中,构成如图所示装置。回答下列问题:
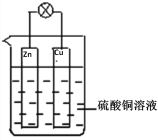
(1)Zn棒为原电池的_____极,其电极反应式为________________________;
(2)Cu棒为原电池的_____极,电极反应式为________________________;
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,水溶液中H+和OH-的浓度变化曲线如图,下列说法正确的是

A. 升高温度,可能引起由c向b的变化
B. 该温度下,水的离子积常数为1.0×10-13
C. 该温度下,加入FeCl3可能引起由b向a的变化
D. 该温度下,稀释溶液可能引起由c向d的变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com