
科目: 来源: 题型:
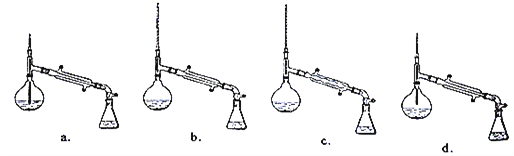
【题目】乙酸异戊酯是组成蜜蜂信息素质的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应装置示意图和有关数据如下:

实验步骤:
在A中加入4.4 g的异戊醇,6.0 g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50分钟,反应液冷却至室温后,倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,分出的产物加入少量无水硫酸镁固体,静置片刻,过滤除去硫酸镁固体,进行蒸馏纯化,收集140℃~143 ℃馏分,得乙酸异戊酯3.9 g。回答下列问题:
(1)装置B的名称是____________________ ,进水口为__________(填“C”或“D”)。
(2)在洗涤操作中,第一次水洗的主要目的是________________; 第二次水洗的主要目的是________________________。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后________(填标号),
A.直接将乙酸异戊酯从分液漏斗上口倒出
B.直接将乙酸异戊酯从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(4)实验中加入少量无水硫酸镁的目的是_______________________
(5)在蒸馏操作中,仪器选择及安装都正确的是____________________(填标号)
(6)本实验的产率是:_________
A.30℅ B.40℅ C.50℅ D.60℅
(7)在进行蒸馏操作时,若从130 ℃开始收集馏分,产率偏_______(填“高”或者“低”),原因是__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是( )
A. Li在氧气中燃烧主要生成Li2O2
B. 将SO3通入BaCl2溶液可生成BaSO3沉淀
C. 水晶项链、光导纤维、玻璃、瓷器等都是硅酸盐制品
D. 将CO2通入次氯酸钙溶液可生成次氯酸
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中,正确的是
A. 自发反应一定是熵增大,非自发反应一定是熵减小或不变
B. 自发反应在恰当条件下才能实现
C. 自发反应在任何条件下均能实现
D. 同一物质的固、液、气三种状态的熵值相同
查看答案和解析>>
科目: 来源: 题型:
【题目】在硫酸铁溶液中,加入ag铜完全溶解后再加入bg铁,充分反应后得到cg残余固体,且a>c,则下列说法中正确的是( )
A.残余固体可能为铁和铜的混合物
B.最后得到的溶液可能含有Fe3+
C.残余固体是铁,溶液中一定不含Cu2+
D.残余固体一定全部是铜
查看答案和解析>>
科目: 来源: 题型:
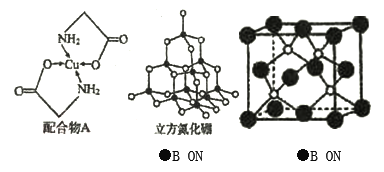
【题目】已知铜的配合物A(结构如图)。请回答下列问题:
(1)Cu的简化电子排布式为___________________。
(2)A中配位原子是_________,配位原子的第一电离能由大到小顺序为_________,杂化轨道类型均为_______________。
(3)配体氨基乙酸根(H2NCH2COO-)受热分解可产生CO2和N2,N2中α键和π键数目之比是_________;N2O与CO2互为等电子体,且N2O分子中0只与一个N相连,则N2O的电子式为_________。
(4)在Cu催化下,甲醇可被氧化为甲醛(HCHO),甲醛分子中H—C—O的键角_________(选填“大于”、“小于”或“等于”)120。甲醇沸点_________甲醛(选填“大于”、“小于”或“等于”),原因是_________。
(5)立方氮化硼与金刚石结构相似,是超硬材料。立方氮化硼的晶胞如图所示,N填充在由B组成的四面体空隙中,则N原子半径RN最大为_________(用B原子半径RB和晶体边长a表示),立方氮化硼晶体内B—N键数与硼原子数之比为_________。结构化学上用原子坐标参数表示晶胞内部各原子的相对位置,下图(右)立方氮化硼的晶胞中,B原子的坐标参数分别有:B(0,0,0);B(l/2,0,l/2);B(l/2,l/2,0)等。则距离上述三个B原子最近且等距的N原子的坐标参数为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ、火箭升空需要高能的燃料,通常用肼(N2H4)作为燃料,N2O4做氧化剂。
(1)已知:N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534.0kJ·mol-1
2NO2(g)![]() N2O4(g) △H=-52.7kJ·mol-1
N2O4(g) △H=-52.7kJ·mol-1
试写出气态肼在四氧化二氮气体中燃烧生成氮气和气态水的热化学方程式:______________________。
(2)工业上可用次氯酸钠与过量的氨反应制备肼,该反应的氧化剂和还原剂的物质的量之比为__________________。
(3)工业上常用氨水调节溶液pH除去金属离子,常温下Cr(OH)3的溶度积Ksp=10-32,要使Cr3+浓度降至10-5mol/L,溶液pH应调至____________________
II、在130℃和180℃时,分别将0.50molCH4和a mol NO2充入1L的密闭容器中发生反应:CH4(g)+2NO2(g) ![]() N2(g)+CO2(g)+2H2O(g) △H<0,测得有关数据如下表:
N2(g)+CO2(g)+2H2O(g) △H<0,测得有关数据如下表:
实验编号 | 温度 | 0min | 10min | 20min | 40min | 50min | |
1 | 130℃ | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
2 | 180℃ | n(CH4)/mol | 0.50 | 0.30 | 0.18 | 0.15 |
(4)180℃时达到平衡状态时,CH4的平衡转化率为___________________。
(5)己知130℃时该反应的化学平衡常数为6.4,试计算a=__________。
(6)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图。在使用过程中石墨I电极上生成氧化物Y (Y为氮元素最高价化化物),该电极反应为_________________。

查看答案和解析>>
科目: 来源: 题型:
【题目】公元前一世纪,我国已使用天然气,天然气的主要成分为甲烷。下列关于甲烷的叙述中,错误的是
A. 通常情况下,甲烷跟强酸、强碱、强氧化剂不起反应
B. 甲烷化学性质比较稳定,不能被任何氧化剂氧化
C. 甲烷跟氧气反应无论生成CH3Cl、CH2Cl、CHCl3还是CCl4,都属于取代反应
D. 甲烷的四种取代物都难溶于水
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关乙烯的说法,其中错误的是
A. 乙烯分子的双键中有一个键较易断裂
B. 乙烯分子里所有原子都在同一平面上,且碳氢键之间的键角约为120°
C. 乙烯的化学性质比乙烷活泼
D. 乙烯和环丙烷( )的分子组成符合通式CnH2n,因此它们属于同系物
)的分子组成符合通式CnH2n,因此它们属于同系物
查看答案和解析>>
科目: 来源: 题型:
【题目】下列坐标图均涉及平衡原理,其中相关表述正确的是( )
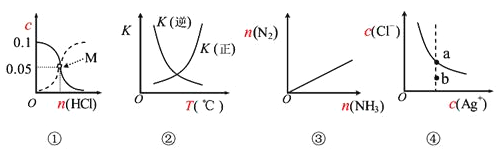
A.图①表示室温下,用0.1mol·L-1氨水吸收HCl气体时,溶液的粒子浓度随吸收HCl的变化,实线表示c(NH3·H2O),虚线表示c(NH4+),处于M点时溶液呈中性
B.图②表示2SO2(g)+O2(g) ![]() 2SO3(g) △H<0正逆反应的平衡常数K随温度的变化
2SO3(g) △H<0正逆反应的平衡常数K随温度的变化
C.图③表示反应2NH3(g) ![]() 3H2(g)+N2(g)在恒温恒压装置中达平衡时,N2的物质的量与通入NH3的物质的量的变化关系
3H2(g)+N2(g)在恒温恒压装置中达平衡时,N2的物质的量与通入NH3的物质的量的变化关系
D.图④表示AgCl(s) ![]() Ag+(aq)+Cl-(aq)的离子的浓度关系,当处于b点时,蒸发部分的水后,可以到达平衡线的a点处
Ag+(aq)+Cl-(aq)的离子的浓度关系,当处于b点时,蒸发部分的水后,可以到达平衡线的a点处
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com