
科目: 来源: 题型:
【题目】在一密闭容器中进行反应:2SO2(g)+O2(g) ![]() 2SO3(g)。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.4mol/L、0.2mol/L、0.4mol/L,当反应达平衡时,可能存在的数据是
2SO3(g)。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.4mol/L、0.2mol/L、0.4mol/L,当反应达平衡时,可能存在的数据是
A. SO2为0.8mol/L,O2为0.4mol/L
B. SO2为0.5mol/L
C. SO3为0.8mol/L
D. SO2、SO3一定均为0.3mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,其中甲池的总反应式为::2CH3OH+3O2+4KOH=2K2CO3+6H2O。下列说法正确的是
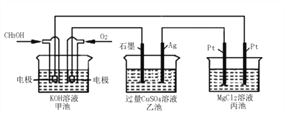
A. 甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置
B. 甲池通入CH3OH的电极反应为CH3OH-6e-+2H2O=CO32-+8H+
C. 反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度
D. 甲池中消耗280 mL(标准状况下)O2,此时丙池中理论上最多产生1.45g固体
查看答案和解析>>
科目: 来源: 题型:
【题目】氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如右图。下列有关氢氧燃料电池的说法不正确的是
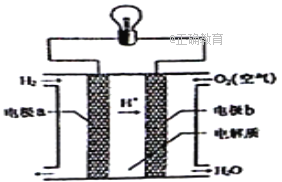
A. 该装置将化学能转化为电能
B. 为了增加灯泡亮度,可以将电极碳棒变得粗糙多孔
C. 电子迁移方向:电极a→灯泡→电极b→电解质溶液→电极a
D. 该电池的总反应:2H2+O2=2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关“化学与生活”的叙述不正确的是( )
A.点燃爆竹后,硫燃烧生成SO3
B.中国古代利用明矾溶液的酸性清除铜镜表面的铜锈
C.服用阿司匹林出现水杨酸反应时,用NaHCO3溶液解毒
D.高铁车厢大部分材料采用铝合金,因为铝合金强度大、质量轻、抗腐蚀能力强
查看答案和解析>>
科目: 来源: 题型:
【题目】苯甲酸是一种重要的化工原料。实验室合成苯甲酸的原理、有关数据及装置示意图如下:

![]()
![]()
![]()
![]()
![]()
名称 | 性状 | 熔点/℃ | 沸点/℃ | 密度 /g·cm-3 | 溶解性 | |
水 | 乙醇 | |||||
甲苯 | 无色液体易燃易挥发 | -95 | 110.6 | 0.866 9 | 不溶 | 互溶 |
苯甲酸 | 白色片状或针状晶体 | 112.4 (100℃左右升华) | 248 | 1.265 9 | 微溶 | 易溶 |
苯甲酸在水中的溶解度如表中所示:
温度/℃ | 4 | 18 | 75 |
溶解度/g | 0.2 | 0.3 | 2.2 |
某学习小组在实验室制备、分离、提纯苯甲酸,并测定所得样品的纯度,步骤如下:
一、制备苯甲酸
在三颈烧瓶中加入2.7 mL甲苯、100 mL水和2~3片碎瓷片,开动电动搅拌器,a中通入流动水,在石棉网上加热至沸腾,然后分批加入8.5 g高锰酸钾,继续搅拌约4~5 h,直到甲苯层几乎近于消失、回流液不再出现油珠,停止加热和搅拌,静置。
二、分离提纯
在反应混合物中加入一定量草酸(H2C2O4)充分反应,过滤、洗涤,将滤液放在冰水浴中冷却,然后用浓盐酸酸化,苯甲酸全部析出后减压过滤,将沉淀物用少量冷水洗涤,挤压去水分后放在沸水浴上干燥,得到粗产品。
三、测定纯度
称取mg产品,配成100 mL乙醇溶液,移取25.00 mL溶液于锥形瓶中,滴加2~3滴酚酞,然后用标准浓度KOH溶液滴定。
请回答下列问题:
(1)装置a的名称是________,其作用为_________________________________。
(2)甲苯被高锰酸钾氧化的原理为![]() +KMnO4
+KMnO4![]() +MnO2↓+H2O+ ________,请完成并配平该化学方程式。
+MnO2↓+H2O+ ________,请完成并配平该化学方程式。
(3)分离提纯过程中加入的草酸是一种二元弱酸,反应过程中有酸式盐和无色气体生成。加入草酸的作用是_______________________,请用离子方程式表示反应原理:__________________。
(4)产品减压过滤时用冷水洗涤的原因是_______________________________。
(5)选用下列________(选填字母)操作,可以将粗产品进一步提纯。
A.溶于水后过滤 B.溶于乙醇后蒸馏
C.用甲苯萃取后分液 D.升华
(6)测定纯度步骤中,滴定终点溶液的颜色变化是_________________________。
若m=1.200 g,滴定时用去0.120 0 mol·L-1标准KOH溶液20.00 mL,则所得产品中苯甲酸的质量分数为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素A、B、C、D原子序数依次增加。X、Y、Z、W是由这四种元素中的两种组成常见的化合物,Y为淡黄色固体,甲为气体单质,乙为红棕色气体,上述物质之间的转化关系如下图所示(部分反应物或生成物省略),则下列说法正确的是
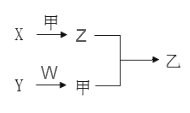
A. 原子半径:D>C>B>A
B. C、D的氢化物均为共价化合物
C. 图示转化关系涉及的反应均为氧化还原反应
D. 最简单气态氢化物的稳定性:B>C
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y和Z均为短周期主族元素,原子序数依次增大,X的单质为密度最小的气体,Y原子最外层电子数是其周期数的三倍,Z与X原子最外层电子数相同。回答下列问题:
(1)Y元素的名称为________。Z的离子结构示意图为_________。
元素Y的简单离子和元素Z的简单离子,半径较大的是________(写出离子符号)。
(2)X和Y组成的化合物中,既含极性共价键又含非极性共价键的是______(写化学式),该物质核外电子总数为______。
(3)化合物Z2Y2的电子式为___________。
(4)X的单质与Y的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则正极电极反应式为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知水在25℃和95℃时,其电离平衡曲线如图所示.

(1)95℃时水的电离平衡曲线应为______(填“A”或“B”),理由是______.
(2)曲线A所对应的温度下,pH=2的HCl溶液和pH=12的某BOH溶液中,若水的电离程度分别用α1、α2表示,则α1______α2(填“大于”、“小于”、“等于”或“无法确定”,下同),若将二者等体积混合,则混合溶液的pH______7.
(3)在曲线B所对应的温度下,将0.02molL﹣1的Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合,所得混合液的pH=______.
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化硼的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是
A. 氯化棚液态时能导电而固态时不导电 B. 氯化硼中心原子采用sp杂化
C. 氯化硼分子呈平面三角形,属非极性分子 D. 其分子立体构型类似NH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com