
科目: 来源: 题型:
【题目】关于反应速率、反应限度的下列说法中错误的是
A.其它条件不变时,升高温度化学反应速率加快
B.其它条件不变时,增大浓度化学反应速率加快
C.化学反应达到反应限度时,反应物的浓度与生成物的浓度相等
D.化学反应达到反应限度时,正反应的速率与逆反应的速率相等
查看答案和解析>>
科目: 来源: 题型:
【题目】在四个不同的容器中,在不同的条件下进行合成氨反应,根据下列在相同时间内测得的结果判断,生成氨的反应速率最快的是
A.v(NH3)=0.3 mol/(L·min) B.v(N2)=0.01 mol/(L·s)
C.v(N2)=0.2 mol/(L·min) D.v(H2)=0.3 mol/(L·min)
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,对于密闭容器中进行的可逆反应:2SO2(g)+O2(g) ![]() 2SO3(g)。下列说法不正确的是
2SO3(g)。下列说法不正确的是
A. 改变反应条件可以改变该反应的限度
B. 达到平衡后,SO3、SO2、O2在密闭容器中共存
C. 达到平衡后,反应停止,正、逆反应速率都等于零
D. 增大压强,正逆反应速率均增大
查看答案和解析>>
科目: 来源: 题型:
【题目】CH4、H2、C都是优质的能源物质,它们燃烧的热化学方程式为
①CH4(g)+2O2(g)===CO2(g)+2H2O(l)
ΔH=-890.3 kJ·mol-1
②2H2(g)+O2(g)===2H2O(l)
ΔH=-571.6 kJ·mol-1
③C(s)+O2(g)===CO2(g)
ΔH=-393.5 kJ·mol-1
(1)在深海中存在一种甲烷细菌,它们依靠酶使甲烷与O2作用产生能量而存活,甲烷细菌使1 mol甲烷生成CO2气体与液态水,放出的能量________(填“>”、“<”或“=”)890.3 kJ。
(2)甲烷与CO2可用于合成合成气(主要成分是一氧化碳和氢气):CH4+CO2===2CO+2H2,1 g CH4完全反应可释放15.46 kJ的热量,则:
①下图能表示该反应过程中能量变化的是________(填字母)。
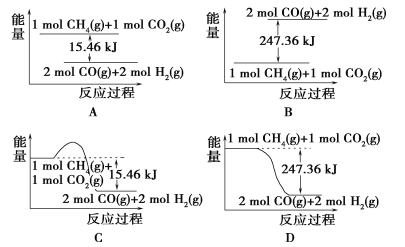

②若将物质的量均为1 mol的CH4与CO2充入某恒容密闭容器中,体系放出的热量随时间的变化如图所示,则CH4的转化率为________。
(3)C(s)与H2(g)不反应,所以C(s)+2H2(g)===CH4(g)的反应热无法直接测量,但通过上述反应可求出C(s)+2H2(g)===CH4(g)的反应热ΔH=________。
(4)目前对于上述三种物质的研究是燃料研究的重点,下列关于上述三种物质的研究方向中可行的是________(填字母)。
A.寻找优质催化剂,使CO2与H2O反应生成CH4与O2,并放出热量
B.寻找优质催化剂,在常温常压下使CO2分解生成C与O2
C.寻找优质催化剂,利用太阳能使大气中的CO2与海底开采的CH4合成合成气(CO、H2)
D.将固态C合成为C60,以C60作为燃料
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)若分子式为C4H6的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为_________________。
(2)分子式为C9H20的某烃其一氯代物只有两种产物,写出符合要求的结构简式________________。
(3)分子式为C5H10的烯烃中不存在顺反异构的物质有_____种。
(4)已知烯烃、炔烃在臭氧作用下发生以下反应:
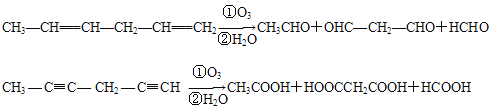
某烃化学式为C10H10,在臭氧作用下发生反应:C10H10![]() CH3COOH+3HOOC-CHO+CH3CHO ①C10H10分子中含________个双键,________个三键。
CH3COOH+3HOOC-CHO+CH3CHO ①C10H10分子中含________个双键,________个三键。
②C10H10结构简式为________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】含有弱酸HA及其钠盐NaA的混合溶液,在化学上可用作缓冲溶液。向其中加入少量酸或碱时,溶液的酸碱性变化不大。
(1)现将0.04 mol·L-1HA溶液和0.02 mol·L-1NaOH溶液等体积混合,得到缓冲溶液。
①若HA为HCN,则该溶液显碱性,该溶液显碱性的原因是___________________,溶液中c(Na+)__________c(CN-)(填“<”、“=”或“>”),你得出该结论的依据是________________________。
②若HA为CH3COOH,则该溶液显酸性。溶液中所有的离子按浓度由大到小排列为_______________________。
(2)Na2HPO4/Na3PO4的混合溶液可以将体系的pH稳定在11.3~13.3之间,是一种常用的缓冲溶液。下列有关该缓冲溶液的说法或关系式错误的是__________。
A.加入少量强碱,发生反应:HPO![]() +OH-===PO
+OH-===PO![]() +H2O
+H2O
B.加入少量强酸,发生反应:HPO![]() +H+===H2PO
+H+===H2PO![]()
C.c(Na+)+c(H+)=c(OH-)+c(H2PO![]() )+2c(HPO
)+2c(HPO![]() )+3c(PO
)+3c(PO![]() )
)
D. ![]() c(Na+)>c(PO
c(Na+)>c(PO![]() )+c(HPO
)+c(HPO![]() )+c(H2PO
)+c(H2PO![]() )+c(H3PO4)>
)+c(H3PO4)> ![]() c(Na+)
c(Na+)
(3)一定浓度的NaHCO3和Na2CO3的混合溶液也是一种缓冲溶液,写出在这种溶液中加入少量NaOH或盐酸时发生反应的离子方程式:_____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上用H2和N2直接合成氨:N2+3H2=2NH3,下列措施肯定能使合成氨反应速率加快的是:
①升高温度 ②加入正催化剂 ③增大反应物浓度 ④增大压强
A.只有①②③ B.只有①②④ C.只有①③④ D.①②③④
查看答案和解析>>
科目: 来源: 题型:
【题目】在铝与稀硫酸的反应中,已知10s末硫酸的浓度减少了0.6 mol/L,若不考虑反应过程中溶液体积的变化,则10s内生成硫酸铝的平均反应速率是
A、0.02 mol/(Lmin) B、1.8mol/(Lmin)
C、1.2 mol/(Lmin) D、0.18 mol/(Lmin)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列电离方程式错误的是 ( )
A.NaHCO3 = Na++H++CO32- B.NaHSO4 = Na++H++SO42-
C.Mg(NO3)2 = Mg2++2NO3- D.Na2SO4 = 2Na++SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com