“神七”登天谱写了我国航天事业的新篇章.火箭升空需要高能燃料,经常是用肼(N
2H
4)作为燃料,N
2O
4做氧化剂.
(1)已知:N
2(g)+2O
2(g)═2NO
2(g)△H=+67.7kJ?mol-1
N
2H
4(g)+O
2(g)═N
2(g)+2H
2O(g)△H=-534.0kJ?mol-1
2NO
2(g)═N
2O
4(g)△H=-52.7kJ?mol-1
请写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:
2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g)△H=-1 083.0 kJ?mol-1
2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g)△H=-1 083.0 kJ?mol-1
.
(2)工业上可用次氯酸钠与过量的氨反应制备肼,该反应的化学方程式为
NaClO+2NH3═N2H4+NaCl+H2O
NaClO+2NH3═N2H4+NaCl+H2O
.
(3)一定条件下,在2L密闭容器中起始时投入2mol NH
3和4mol O
2,发生反应:
4NH
3(g)+5O
2(g)?4NO(g)+6H
2O(g)△H<0,测得平衡时的数据如下表:
| 有关物质的物质的量/mol |
n(NO) |
n(H2O) |
| 温度T1 |
1.6 |
2.4 |
| 温度T2 |
1.2 |
1.8 |
①在T
1时,若经过10min反应达到平衡,则10min内反应的平均速率v(NH
3)=
0.08 mol?L-1?min-1
0.08 mol?L-1?min-1
.
②T
1和T
2的大小关系是T
1<
<
T
2(填“>”“<”或“=”).
(4)在载人航天器的生态系统中,不仅要求分离去除CO
2,还要求提供充足的O
2.某种电化学装置可实现如下转化:2CO
2═2CO+O
2,CO可用作燃料.已知该装置的阳极反应为:4OH
--4e
-═O
2↑+2H
2O,则阴极反应为
2CO2+4e-+2H2O═2CO+4OH-(或CO2+2e-+H2O═CO+2OH-)
2CO2+4e-+2H2O═2CO+4OH-(或CO2+2e-+H2O═CO+2OH-)
.
有人提出,可以设计反应2CO═2C+O
2(△H>0)来消除CO的污染,请你判断该反应是否能自发进行并说明理由?答:
不能,因为该反应的△S<0
不能,因为该反应的△S<0
.
(5)某空间站能量转化系统的局部如图所示,其中的燃料电池采用KOH溶液作电解液.
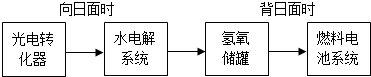
如果某段时间内,氢氧储罐中共收集到33.6L气体(已折算成标准状况),则该段时间内水电解系统中转移电子的物质的量为
2
2
mol.


 实验化学
实验化学 物质结构与性质
物质结构与性质