
科目: 来源: 题型:
【题目】A、B、C、D、E、F是元素周期表前四周期中原子序数依次增大的六种常见元素,其相关信息如下表:
元素 | 相 关 信 息 |
A | 原子核外有7种运动状态不同的电子 |
B | 外围电子排布式为nsnnpn+2 |
C | 常见的金属,在周期表中周期序数与族序数相等 |
D | 气态氢化物及最高价氧化物对应的水化物均为强酸 |
E | 一种核素的质量数为56,中子数为30 |
F | 单质紫红色,电缆材料,常见氧化物为黑色 |
回答下列问题:
(1)元素E在元素周期表中的位于第四周期第__族,其高价态离子核外有__个未成对电子
(2)B、C、D三种元素的离子半径由小到大的顺序是______(用离子符号表示).
(3)A、D两元素的简单氢化物发生反应生成的化合物的电子式为_______
(4)常温下AD3是一种淡黄色液体。以下关于AD3的说法中,正确的是__________
A.AD3分子中只有非极性键 B.AD3分子中各原子均达8e-稳定结构
C.AD3的晶体属于分子晶体 D.AD3液体气化时化学键被破坏
(5)金属C与E的黑色磁性晶体氧化物在高温下反应,该反应的化学方程式为___________________
(6)向F的硫酸盐溶液中通入AH3气体至过量,观察到的现象是__________;该过程总的离子反应式为________________向反应后的溶液中加入适量乙醇,析出深蓝色晶体,该晶体中不含有的化学键类型是________
A.配位键 B.极性共价键 C.非极性共价键 D.离子键
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ、现有如图几种有机物:

请利用如图给出的物质按要求回答下列问题:
(1)相对分子质量为44的烷烃的结构简式为__;
(2)分子中含有14个氢原子的烷烃的分子式是__;
(3)与③互为同分异构体的是__(填序号);
(4)具有特殊气味,常作萃取剂的有机物在铁作催化剂的条件下与液溴发生一取代反应的化学方程式__;
(5)用“>”表示①③④⑨熔沸点高低顺序:__(填序号);
(6)有机物②在加热条件下和CuO反应的化学方程式__;
(7)在120℃,1.01×105Pa条件下,某种气态烃与足量的O2完全反应后,测得反应前后气体的体 积没有发生改变,则该烃是__(填序号);它与⑧互为__关系;
(8)有机物⑤和②在一定条件下发生反应的化学方程式是__.
Ⅱ、油脂的组成可用“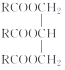 ”来表示,其中R为碳原子数目多于10的链烃基,可以相同也可以不同。分子式为C51H92O6的某油脂在稀硫酸中加热水解后得到A、B两种物质,若A的相对分子质量为92(已知:R1—CH===CH—R2
”来表示,其中R为碳原子数目多于10的链烃基,可以相同也可以不同。分子式为C51H92O6的某油脂在稀硫酸中加热水解后得到A、B两种物质,若A的相对分子质量为92(已知:R1—CH===CH—R2![]() R1—COOH+R2—COOH),则
R1—COOH+R2—COOH),则
(1)B的分子式为________,A的结构简式为________。
(2)B![]() C+D,等物质的量的C、D分别与足量的NaOH溶液反应时,消耗的NaOH的质量之比为1∶2,C、D的相对分子质量相差30且C、D结构中均无支链,则B的结构简式为________。
C+D,等物质的量的C、D分别与足量的NaOH溶液反应时,消耗的NaOH的质量之比为1∶2,C、D的相对分子质量相差30且C、D结构中均无支链,则B的结构简式为________。
(3)若A和乙酸在一定条件下反应后生成相对分子质量为134的E,写出E所有可能的结构简 ______________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】绿色化学是“预防污染”的根本手段,它的目标是研究和寻找能充分利用的无毒害原材料,最大限度地节约能源,在化工生产各环节都实现净化和无污染的反应途径。下列各项属于“绿色化学”的是( )。
A.处理废弃物 B.治理污染点
B.减少有毒物 D.杜绝污染源
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,在一容积可变的容器中,反应2A(g)+B(g) ![]() 2C(g)达到平衡时,A、B、C的物质的量分别为4mol、2mol、4mol,保持温度和压强不变,对平衡混合物中三者的物质的量作如下调整,平衡右移的是
2C(g)达到平衡时,A、B、C的物质的量分别为4mol、2mol、4mol,保持温度和压强不变,对平衡混合物中三者的物质的量作如下调整,平衡右移的是
A. 均增加1mol B. 均减小1mol C. 均减半 D. 均加倍
查看答案和解析>>
科目: 来源: 题型:
【题目】(Ⅰ)某化学兴趣小组要完成中和热的测定.回答下列问题:
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5molL﹣1盐酸、0.55molL﹣1NaOH溶液,实验尚缺少的玻璃用品是_______.
(2)已知:反应后溶液的比热容c为4.18J·℃﹣1g﹣1,0.5molL﹣1盐酸和0.55mol·L﹣1NaOH溶液的密度均为1g·cm﹣3.实验时记录的实验数据如下:
实验 次数 | 反应物及用量 | 溶 液 温 度 | ||
t1 | t2 | |||
1 | 50mL0.55molL-1NaOH溶液 | 50mL.0.5molL-1HCl溶液 | 20℃ | 23.3℃ |
2 | 50mL0.55molL-1NaOH溶液 | 50mL.0.5molL-1HCl溶液 | 20℃ | 23.5℃ |
①盐酸和氢氧化钠反应的中和热△H1=____________(保留两位小数)
②已知:CH3COOH(aq)![]() CH3COO-(aq)+H+(aq) △H2>0 ,
CH3COO-(aq)+H+(aq) △H2>0 ,
CH3COOH(aq)+OH-(aq)= CH3COO-(aq)+H20(l) △H3 则△H3_____△H1(填“>”、“<”、“=”)
(Ⅱ)某实验小组利用硫酸酸化的KMnO4与H2C2O4反应来探究“外界条件对化学反应速率的影响”。该小组实验方案如下(实验测定KMnO4溶液完全褪色时间)。回答下列问题:
实验 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | H2O/mL | 温度/℃ | KMnO4溶液完全褪色时间(s) | ||
浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | ||||
① | 0.20 | 2.0 | 0.010 | 4.0 | 2.0 | 25 | t1 |
② | 0.20 | 4.0 | 0.010 | 4.0 | 0 | 25 | t2 |
③ | 0.20 | 4.0 | 0.010 | 4.0 | 0 | 50 | t3 |
(3)上述反应的离子方程式为______________________________________
(4)t1_____ t2(填“>”、“<”、“=”),其理由是__________________
(5)实验②和实验③两组实验的目的是______________________________
(6)有同学做实验时发现,硫酸酸化的KMnO4与H2C2O4反应开始时,溶液褪色慢,但反应一段时间后溶液褪色明显加快。针对上述实验现象,该同学提出下列猜想:
猜想①:硫酸酸化的KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。
猜想②:__________________(请你补充)
要证实猜想②,除硫酸酸化的高锰酸钾溶液、草酸溶液外,还需要选择的试剂是______。
A.硫酸钾 B.硫酸锰 C.水 D.氯化锰
查看答案和解析>>
科目: 来源: 题型:
【题目】将纯水加热至较高温度,下列叙述正确的是( )
A.Kw变大、pH变小、呈酸性
B.Kw变大、pH不变、呈中性
C.Kw变小、pH变大、呈碱性
D.Kw变大、pH变小、呈中性
查看答案和解析>>
科目: 来源: 题型:
【题目】干冰和二氧化硅晶体同属ⅣA族元素的最高价氧化物,它们的熔、沸点差别很大的原因是
A. 二氧化硅相对分子质量大于二氧化碳相对分子质量 B. C—O键键能比Si—O键键能小
C. 干冰为分子晶体,二氧化硅为原子晶体 D. 干冰易升华,二氧化硅不能
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.已知:CO2(g)+ 3H2(g) ![]() CH3OH(g)+ H2O(g) △H
CH3OH(g)+ H2O(g) △H
现在体积为1L的密闭容器中,充入CO2和H2。实验测得反应体系中物质的物质的量与时间关系如下表,
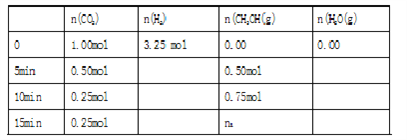
回答下列问题:
(1)表格中的n1=______________
(2)0-5min内 v (H2)=_______________
(3)该条件下CO2的平衡转化率为__________________
Ⅱ.在容积为100L的密闭容器中,加入1.0molCH4和2.0molH2O(g)。一定条件下发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H
CO(g)+3H2(g) △H
已知CH4的转化率与温度、压强的关系如图1所示。回答下列问题:
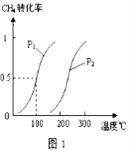
(4)100℃时平衡常数为_________________.
(5)图1中的p1_______p2(填“<”、“>”或“=”),其理由是:_________________
(6)若100℃时该可逆反应的平衡常数是K1,200℃该该可逆反应的平衡常数是K2,则K1___ K2(填“<”、“>”或“=”).其理由是__________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com