
科目: 来源: 题型:
【题目】下列关于Na2O和Na2O2的叙述正确的是( )
A. Na2O与Na2O2颜色相同 B. 均可与CO2、H2O反应产生氧气
C. 阴、阳离子的个数比均为1∶2 D. 所含氧元素的化合价均为-2
查看答案和解析>>
科目: 来源: 题型:
【题目】硫及其化合物广泛存在于自然界中。
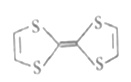
(1)四硫富瓦烯分子结构如图所示,其碳原子杂化轨道类型为_________,根据电子云的重叠方式其含有的共价键类型为___________,1mol四硫富瓦烯中含有σ键数目为__________。
(2)煅烧硫铁矿时发生的反应为FeS2+O2![]() Fe2O3+SO2,所得产物SO2再经催化氧化生成SO3,SO3被水吸收生成硫酸。
Fe2O3+SO2,所得产物SO2再经催化氧化生成SO3,SO3被水吸收生成硫酸。
①基态S原子存在____________对自旋方向相反的电子。
②离子化合物FeS2中,Fe2+的电子排布式为__________,与S22-互为电子体的离子是____________。
③气体SO3分子的空间构型为__________,中心原子阶层电子对数为____________。
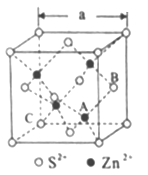
(3)闪锌矿是一种自然界含Zn元素的矿物,其晶体结构属于立方晶体(如下图所示),Zn属于_______区元素,在立方ZnS晶体结构中S2-的配位数为______________,若立方ZnS晶体的密度为ρg·cm-3,晶胞参数a=______nm(列出计算式),晶胞中A、B的坐标分别为A(![]() ,
, ![]() ,
, ![]() )、B(
)、B(![]() ,
, ![]() ,
, ![]() ),则C点的坐标为____________。
),则C点的坐标为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸亚铁是人体常用的补铁剂,缺少Fe2+会导致缺铁性贫血。绿矾(FeSO4·7H2O)在不同温度下易分解得各种铁的氧化物和硫的氧化物。已知SO3是一种无色晶体,熔点16.8℃,沸点44.8℃,氧化性及脱水性较浓硫酸强,能漂白某些有机染料,如品红等。回答下列问题:
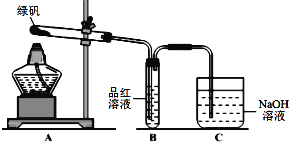
(1)第一组同学按照上图装置做绿矾的分解实验,并检验其分解产物。装置B中观察到品红褪色,第一组同学得出结论:绿矾的分解产物中含有______________________。
(2)第二组同学为了进一步探究褪色的原因,对第一组同学做完实验B装置的试管加热,发现褪色的品红溶液未恢复红色,则可证明绿矾分解的产物中________。(填字母)
A.不含SO2 B.一定含有SO3 C.可能含SO2
(3)第三组同学查阅资料发现绿矾受热分解还可能有O2放出,为此,第三组同学从下图中选取了部分仪器设计了一套检验绿矾分解的气体产物装置:
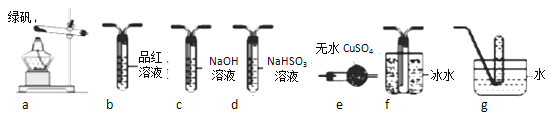
①第三组同学的实验装置中,依次连接的合理顺序为a→___→ → → → 。
②验证分解产物中有O2的简要实验操作步骤及现象是____________________________
(4)检验绿矾分解产物中含有三价铁,应选用的实验仪器有试管、胶头滴管、_______;选用的试剂为____________、____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知X、Y、Z三种短周期元素的族序数之和为11,且X、Y、Z能形成化合物X2YZ3。下列判断正确的是
A. X、Y、Z不可能为同周期元素
B. 化合物X2YZ3可能难溶于水
C. Y的原子半径一定比Z小
D. X可能位于第IIA族
查看答案和解析>>
科目: 来源: 题型:
【题目】由Mg、P、S、Cl、Ni等元素组成的新型材料有着广泛的用途,请回答下列问题。
(1)基态Mg原子L层电子排布式为_____,P、S、Cl的第一电离能由大到小顺序为_______。
(2)PH4Cl的电子式为_________,Ni与CO能形成配合物Ni(CO)4,该分子中σ键与π键个数比为__________。
(3)SCl2分子中的中心原子杂化轨道类型是_______,该分子构型为_________。
(4)已知MgO与NiO的晶体结构(如图1)相同,其中Mg2+和Ni2+的离子半径分别为66pm和69 pm。则熔点:MgO_____NiO(填“>”、“<”或“=”),理由是_____________。
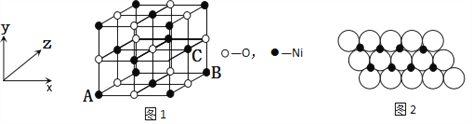
(5)如图1所示,NiO晶胞中离子坐标参数A为(0,0,0),B为(1,0,1),则C离子坐标参数为___________。
(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图2),已知O2-的半径为a m,每平方米面积上分散的该晶体的质量为______g。(用a、NA表示)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述中,错误的是( )
A. 苯与浓硝酸、浓硫酸共热并保持55-60℃反应生成硝基苯
B. 苯乙烯在合适条件下催化加氢可生成乙基环己烷
C. 乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷
D. 甲苯与氯气在光照下反应主要生成2,4-二氯甲苯
查看答案和解析>>
科目: 来源: 题型:
【题目】C、N、S对应的化合物,是重要的化学物质。试回答下列问题:
(1)已知:氢气的燃烧热为286.0kJ/mol,氨气的燃烧热为382.5 kJ/mol ,则合成氨反应的热化学方程式
为_____________________。
(2)利用Fe2+、Fe3+的催化作用,常温下可将SO2转化为SO42-,从而实现对SO2的治理。已知含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,则另一反应的离子方程式为________________。
(3)用活性炭还原法处理氮氧化物。 有关反应为C(s)+2NO(g) ![]() N2(g)+CO2(g)。
N2(g)+CO2(g)。
某研究小组向密闭的真空容器中(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T)条件下反应,反应进行到不同时间测得各物质的浓度如表:
时间(min) 浓度(molL-1) | NO | N2 | CO2 |
0 | 1.00 | 0 | 0 |
10 | 0.58 | 0.21 | 0.21 |
20 | 0.40 | 0.30 | 0.30 |
30 | 0.40 | 0.30 | 0.30 |
40 | 0.32 | 0.34 | 0.17 |
50 | 0.32 | 0.34 | 0.17 |
①10min~20min以v(CO2)表示的反应速率为_________________。
②根据表中数据,计算T℃时该反应的平衡常数为Kp=___________,(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,保留两位小数)
③一定温度下,随着NO的起始浓度增大,则NO的平衡转化率_________(填“增大”“不变”或“减小”)。
④该反应达到平衡时下列说法正确的是______填序号字母)。
a.容器内压强保持不变 b.2v(NO)=v(N2)
c.容器内CO2的体积分数不变 d.混合气体的密度保持不变
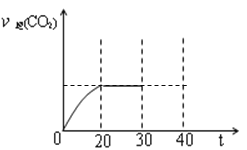
⑤30min时改变某一条件,过一段时间反应重新达到平衡,则改变的条件可能是______。请在图中画出30~40min的变化曲线______。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化合物的分子式为C5H11Cl,分析数据表明:分子中有两个—CH3、两个—CH2—、一个![]() 和一个—Cl,它的可能的结构有几种( )
和一个—Cl,它的可能的结构有几种( )
A. 3 B. 4 C. 5 D. 6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com