
科目: 来源: 题型:
【题目】下列关于物质用途的说法中,不正确的是( )
A. 硅酸钠可用于制备硅胶和木材防火剂等
B. 氧化铝熔点高可用作耐火材料
C. 晶体硅可用于制造光导纤维
D. 漂白粉和臭氧可用于自来水消毒
查看答案和解析>>
科目: 来源: 题型:
【题目】某无色溶液能溶解Al(OH)3,则此溶液中一定能大量共存的离子组是
A. Fe2+、Cl-、Na+、NO3- B. K+、Na+、NO3-、HCO3-
C. Na+、Ba2+、Cl-、NO3- D. Na+、K+、AlO2-、SO42-
查看答案和解析>>
科目: 来源: 题型:
【题目】近年全国各地雾霾严重,为有效控制雾霾,各地积极采取措施改善大气质量。研究并有效控制空气中氮氧化物、碳氧化物等污染物是一项重要而艰巨的工作。
Ⅰ.氮氧化物的研究

(1)一定条件下,将2mol NO与2mol O2置于恒容密闭容器中发生反应:2NO(g)+O2(g) ![]() 2NO2(g),下列状态能说明该反应达到化学平衡的是(_______)
2NO2(g),下列状态能说明该反应达到化学平衡的是(_______)
A.混合气体的密度保持不变
B.NO的转化率保持不变
C.NO和O2的物质的量之比保持不变
D.O2的消耗速率和NO2的消耗速率相等
(2)已知反应. 2NO(g) ![]() N2(g)+O2(g) ΔH<O,在不同条件时N2的体积分数随时间(t)的变化如图1所示。根据图象可以判断曲线R1、R2对应的下列反应条件中不同的是______ (填字母序号)。
N2(g)+O2(g) ΔH<O,在不同条件时N2的体积分数随时间(t)的变化如图1所示。根据图象可以判断曲线R1、R2对应的下列反应条件中不同的是______ (填字母序号)。
A.压强 B.温度 C.催化剂
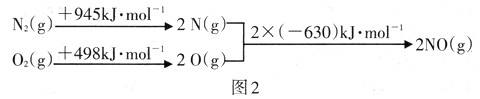
根据图2中的能量变化数据.计算反应2NO(g) ![]() N2(g)+O2(g)的ΔH=__________
N2(g)+O2(g)的ΔH=__________
Ⅱ.碳氧化物研究
(3)CO和H2在一定条件下可以合成甲醇:CO(g)+2H2(g) ![]() CH3OH(g) ΔH<O ,现在体积为1L的恒容密闭容器(图3甲)中通入1mol CO和2mol H2,测定不同时间、不同温度(T)下容器中CO的物质的量,如下表:
CH3OH(g) ΔH<O ,现在体积为1L的恒容密闭容器(图3甲)中通入1mol CO和2mol H2,测定不同时间、不同温度(T)下容器中CO的物质的量,如下表:

请回答:
①T1_____ T2(填“>”或“<”或“=”),理由是____________________。已知T2℃时,第20min时容器内压强不再改变,此时H2的转化率为_________,该温度下的化学平衡常数为________ 。
②若将1mol CO和2mol H2通入原体积为1L的恒压密闭容器(图3乙)中,在T2℃下达到平衡,此时反应的平衡常数为_________;若再向容器中通入l mol CH3OH(g),重新达到平衡后,CH3OH(g)在体系中的百分含量_________(填“变大”或“变小”或“不变”)。
(4)一定条件下也可用NaOH溶液与CO反应生成甲酸钠,进一步反应生成甲酸来消除CO污染。常温下将a mol的CO通入2 L bmol/L NaOH 溶液中,恰好完全反应生成甲酸钠和含少量甲酸的混合溶液(假设溶液体积不变),测得溶液中c(Na+)=c(HCOO-),则该混合溶液中甲酸的电离平衡常数 Ka=____________ (用含a和b的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容中发生下列反应aA(g)cC(g)+dD(g),压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
A.A的转化率变大
B.平衡向正反应方向移动
C.D的体积分数变大
D.a<c+d
查看答案和解析>>
科目: 来源: 题型:
【题目】锗(Ge)原子结构示意图为:
(1)锗位于元素周期表中的第_________周期,第________族,
(2)最高价氧化物化学式为________,对应水化物化学式为___________。
(3)根据示意图: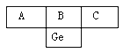
推得A、B、C依次为______、____、_____元素。A、B、C中,________是典型的非金属元素(填元素符号,下同),__________的最高价氧化物具有两性;可用作半导体的是_______,可作导体是________,常用来制农药的是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】苹果汁是人们喜爱的饮料。由于此饮料中含有Fe2+,现榨苹果汁在空气中会由淡绿色(Fe2+) 变为棕黄色(Fe3+)。若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有( )
A.氧化性 B.还原性 C.碱性 D.酸性
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于容量瓶及其使用方法的叙述正确的是
①是配制一定物质的量浓度的溶液的专用仪器 ②使用前要先检查容量瓶是否漏液 ③容量瓶可用来加热 ④不能用容量瓶长期贮存配制好的溶液 ⑤可以用500 mL容量瓶配制250 mL溶液
A. ①B. ①②④C. 除了③D. 除了⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】配位化合物的数量巨大,组成和结构形形色色,丰富多彩。请指出配合物 [Cu(H2O)4](OH)2的中心离子、配体、中心离子的电荷数和配位数
A.Cu2+、H2O、+2、4 B.Cu+、H2O、+1、4
C.Cu2+、OH-、+2、2 D.Cu2+、H2O、+2、2
查看答案和解析>>
科目: 来源: 题型:
【题目】元素A、B、C、D、E、F、G在元素周期表中的位置如图1所示。
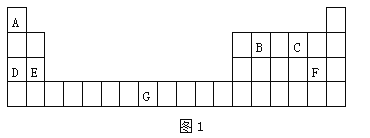
回答下列问题:
(1)G的基态原子核外电子排布式为___________;原子的第一电离能:D_____E(填“>”或“<”)。
(2)根据价层电子对斥理论,A2C中的“A—C—A”键角是_________(填字母序号)。
A.180° B.接近120°,但小于120°
C.接近120°,但大于120 D.接近109°28ˊ,但小于109°28ˊ
(3)已知化合物G(BC)5的G元素化合价为0,熔点为-20℃,沸点为103℃,其固体属于_______晶体,该物质中存在的化学键类型有________,它在空气中燃烧生成红棕色氧化物,反应的化学方程式为_________________________。
(4)化合物BCF2的分子立体构型为________,其中B原子的杂化轨道类型是_________。写出一个与BCF2具有相同空间构型的含氧酸根离子符号_____________。
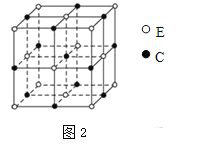
(5)化合物EC的晶胞结构如图2所示。每个晶胞中含有_______个E2+。若EC晶体的密度为dg·cm-3,阿伏伽德罗常数值为NA,则晶胞参数a=_________nm(列出计算式,不要求最终结果)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com