
科目: 来源: 题型:
【题目】“毒胶囊”泛指利用由工业皮革废料为原料生产的含重金属铬(Cr)超标的胶囊,其中含有可能引起人体肾伤害的+6价的铬.下列铬的化合物中铬呈+6价的是( )
A.Cr2(SO4)3B. Cr2O3 C.K2CrO4 D.CrCl2
查看答案和解析>>
科目: 来源: 题型:
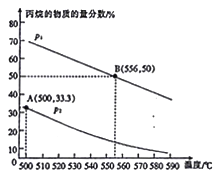
【题目】利用液化石油气中的丙烷脱氢可制取丙烯:C3H8(g)![]() C3H6 (g)+H2 (g) △H。起始时,向一密闭容器中充入一定量的丙烷,在不同温度、压强下测得平衡时反应体系中丙烷的物质的量分数如图所示(已知pl为0.1 MPa)。
C3H6 (g)+H2 (g) △H。起始时,向一密闭容器中充入一定量的丙烷,在不同温度、压强下测得平衡时反应体系中丙烷的物质的量分数如图所示(已知pl为0.1 MPa)。
(1)反应的△H_________(填“>”“<”或“=’’,下同)
(2)以丙烯为燃料、熔融碳酸盐为电解质制作新型电池,放电时CO32-移向该电池的______(填“正极,或“负极”),当消耗2.8 L(标准状况)C3H6时,电路中转移电子的物质的量为__________。
(3)根据图中B点坐标计算,556℃时该反应酌平衡常数为______Pa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),若图中A、B两点对应的平衡常数用K(A)、K (B)表示,则K(A) _____(填“>” “<”或“=”)K(B)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)下列物质中,由极性键形成的非极性分子是____。
A.CO2 B.H2O C.CO D.CCl4
(2)近年来,我国北方地区雾霾频发。引起雾霾的PM2.5微细粒子包含(NH4)2SO4、NH4NO3、有机颗粒物及扬尘等。通过测定雾霾中锌等重金属的含量,可知交通污染是目前造成雾霾天气的主要原因之一。回答下列问题:
(1)基态O原子核外电子的运动状态有______种,其电子云形状有____种。
(2)基态Zn原子的核外电子排布式为____。
(3)(NH4)2SO4中存在的化学键类型有_______。
(4)N和F能形成化合物N2F2,N2F2中氮原子的杂化轨道类型为________,写出N2F2的一种结构式:____,1mol N2F2分子中所含σ键的数目是_________。
(5)下列说法正确的是________(填字母)。
a.N2O为直线形分子
b.C、N、O的第一电离能依次增大
c.O3与SO2、NO2-互为等电子体
d.相同压强下,HCOOH的沸点比CH3OCH3的高,说明前者是极性分子,后者是非极性分子
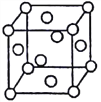
(6)测定大气中PM2.5浓度的方法之一是β-射线吸收法,其放射源可用85Kr。已知85 Kr晶体的晶胞结构如图所示。设晶胞中所含85Kr原子数为m,与每个85 Kr原子相紧邻的85 Kr原子数为n,则![]() _______(填数值)。该晶胞的边长为a nm,则85Kr晶体的密度为______g/cm3.(设NA为阿伏加德罗常数的值)
_______(填数值)。该晶胞的边长为a nm,则85Kr晶体的密度为______g/cm3.(设NA为阿伏加德罗常数的值)
查看答案和解析>>
科目: 来源: 题型:
【题目】四种短周期元素A、B、C、D的性质或结构信息如下:
信息:①原子半径:A>B>C>D ②四种元素之间形成的某三种分子的比例模型及部分性质如下:
甲:![]() 是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二.
是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二.
乙:![]() 无色,无气味并且易燃.是常见的一种基础能源,17年5月18日,我国首次开采成功它的水合物并连续产量,可解千年能源之忧。
无色,无气味并且易燃.是常见的一种基础能源,17年5月18日,我国首次开采成功它的水合物并连续产量,可解千年能源之忧。
丙:![]() 有强氧化性的弱酸,可以用于消毒杀菌.
有强氧化性的弱酸,可以用于消毒杀菌.
请根据上述信息回答下列问题.
(1)B元素在元素周期表中的位置为_____,请写出BC2分子的电子式:______.
(2)A、E、F在同一周期,E元素的单质还原性最强,F元素的某些盐类常用作净水剂.E单质与甲反应有化合物X生成.请写出以下两个反应的离子方程式:
①A元素的单质与物质甲发生反应:________________________________.
②F、C两种元素组成的化合物Y可作为耐高温结构的材料,X与Y两种化合物在溶液中发生反应的离子方程式:_________________________________________________.
(3)物质丁的元素组成和甲相同,丁分子具有18电子结构.向盛有一定浓度丁溶液的试管中,逐滴加入硫酸酸化的硫酸亚铁溶液.滴加过程中的现象为:①试管中溶液变成深棕黄色,②开始有少量气泡出现(经验证是氧气),片刻后反应变得剧烈,继续滴加溶液,静置一段时间,试管底部出现红褐色沉淀.请回答“片刻后反应变得剧烈”的原因
a_____________________b_________________.
(4)物质戊的元素组成和乙相同,戊分子具有18电子结构.与乙互为同系物,则戊的氯取代有机物的共________种。
查看答案和解析>>
科目: 来源: 题型:
【题目】关于 Na2 CO3和NaH CO3下列说法不正确的是( )
A.可以用加热的方法除去Na2 CO3中的NaH CO3
B.分别向Na2 CO3和NaH CO3溶液滴加少量盐酸,产生CO2气体较快的为NaH CO3
C.可以用Ca( OH)2 溶液区分Na2 CO3和NaH CO3溶液
D.Na2 CO3比NaH CO3易溶于水
查看答案和解析>>
科目: 来源: 题型:
【题目】正硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子之间通过氢键相连(层状结构如图所示,图中‘‘虚线”表示氢键)。下列有关说法正确的是
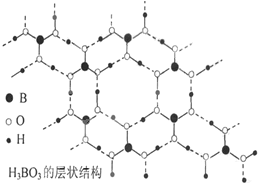
A. H3BO3分子的稳定性与氢键有关
B. 含1 molH3BO3的晶体中有3 mol氢键
C. 分子中B、O最外层均为8e-稳定结构
D. B原子杂化轨道的类型为sp2,同层分子间的主要作用力是范德华力
查看答案和解析>>
科目: 来源: 题型:
【题目】科学家曾合成了一系列具有独特化学特性的(A1H3)n氢铝化合物。己知,最简单的氢铝化合物的分子式为A12H6,它的熔点为150 ℃,燃烧热极高。A12H6球棍模型如图。下列有关说法肯定错误的是

A. Al2H6在固态时所形成的晶体是分子晶体
B. 氢铝化合物可能成为未来的储氢材料和火箭燃料
C. Al2H6在空气中完全燃烧,产物为氧化铝和水
D. Al2H6中含有极性共价键、配位键和离子键
查看答案和解析>>
科目: 来源: 题型:
【题目】为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验。
(1)称取a g样品,向其中加入足量的NaOH溶液,测得生成的气体(标准状况,下同)体积为b L,反应的离子方程式为 。
(2)称取同样的a g样品,在高温下恰好完全反应。
(3)待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为c L,该气体与(1)中所得气体的体积比,c:b为_______________。
根据上述实验可确定该铝热剂中含Al的质量分数为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ、在容积为2L的密闭容器中进行如下反应:A(g)+2B(g)![]() 3C(g)+XD(g),开始时A为4mol,B为6mol;5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。计算
3C(g)+XD(g),开始时A为4mol,B为6mol;5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。计算
(1)5min末A的物质的量浓度为______________mol/L·
(2)前5min内用B表示的化学反应速率v(B)为_________mol/(L·min)。
(3)化学方程式中X值为__________ 。
(4)此反应在四种不同情况下的反应速率分别为:①v(A)=5mol/(L·min);②v(B)=6mol/(L·min);③v(C)=4.5mol/(L·min);④v(D)=8mol/(L·min)。
其中反应速率最快的是__________(填编号)。
Ⅱ、(1)相对分子质量为72的烷烃,它的一氯代物只有一种,此烷烃的结构简式为_________。
(2)某气态烷烃和一气态烯烃组成的混合气体在同温、同压下对氢气的相对密度为13,取标准状况下此混合气体4.48 L,通入足量的溴水,溴水质量增加2.8 g,此两种烃的组成为______________(填分子式)。
(3) 有机物的结构可用“键线式”表示,如:![]() 可简写为
可简写为![]()
![]() 可简写为
可简写为 ![]() 。玫瑰的香味物质中包含苧烯,苧烯的键线式如右图,
。玫瑰的香味物质中包含苧烯,苧烯的键线式如右图,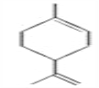 ,苧烯的分子式为___________。
,苧烯的分子式为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】除金、铂等极少数金属外,绝大多数金属元素以化合物形式存在于自然界中,将金属元素从其化合物中还原出来的工业工程称为金属的冶炼。下列材料描述了部分常见金属的冶炼方法。
①工业上冶炼镁的方法有两种,电解法和皮江法。电解法是电解熔融的氯化镁;皮江法是硅在高温下还原氧化镁。
②霍尔-埃鲁铝电解法是以氧化铝为原料、冰晶石(Na3AlF6)为熔剂组成的电解质,在950-970℃的条件下通过电解的方法使电解质熔体中的氧化铝分解为铝和氧气。
③冶炼锰一般用铝热法,即在高温下用铝还原二氧化锰。
④相关各物质熔点见下表:
物质 | Al2O3 | AlCl3 | MgO | MgCl2 | Al | Mn | Mg |
熔点/℃ | 2303 | 190 | 2800 | 712 | 660 | 1244 | 649 |
Ⅰ、根据上述信息回答下列问题:
(1)冶炼镁时电解熔融MgCl2而不电解熔融MgO,冶炼铝时电解熔融Al2O3而不电解熔融AlCl3的原因是______________________________________________。
(2)写出铝热法冶炼锰的化学方程式___________________________,
一般使用铝热法冶炼的金属具有哪些性质_____________________________。
(3)将铝和镁作电极分别插入稀硫酸、氢氧化钠溶液中,镁、铝分别作______极、_____极;写出介质是稀硫酸溶液时的正极电极反应式:______。
Ⅱ、下面是皮江法冶炼镁的工业流程示意图:

(1)气体a是_______。
(2)还原炉需控制温度为1200℃左右,并抽空气到近似真空。还原炉中发生的主要反应有____________________________、_______________________。
(3)还原炉中抽空气到近似真空的原因是________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com