
科目: 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)从氯化钾溶液中得到氯化钾固体,选择装置___(填代表装置图的字母,下同);除去自来水中的Cl﹣等杂质,选择装置___。
(2)从碘水中分离出I2,选择装置____,该分离方法的名称为____。
(3)装置A中①的名称是_____,进水的方向是从_____口(填“上”或“下”)进水。装置B在分液时为使液体顺利滴下,除打开漏斗下端的旋塞外,还应进行的具体操作是______。
(4)粗盐中含Ca2+、Mg2+、Fe3+、SO42﹣等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④过滤 ⑤溶解 ⑥加盐酸调节溶液的pH等于7 ⑦蒸发,操作顺序合理的是_____(选填项字母)
a.⑤②③①④⑥⑦ b.⑤①②③④⑥⑦ c.⑤②①③⑥④⑦ d.⑤③②①④⑥⑦
查看答案和解析>>
科目: 来源: 题型:
【题目】近年来雾霾天气多次肆虐我国中东部地区,其中汽车尾气和燃煤尾气是造成空气污染的原因之一。有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要。
(1)在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质。主要原理为:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)。
2CO2(g)+N2(g)。
①该反应的平衡常数表达式为______________。
②在密闭容器中发生该反应时,c(CO2)随温度(T)和时间(t)的变化曲线如下图1所示。据此判断该反应的△H_______0(填“>”或“<”),在T1温度下,02 s内N2的平均反应速率v(N2) =________。
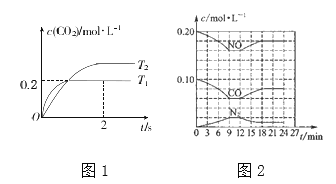
③将0.2mol NO和0.1mol CO充入一个容积为1L的密闭容器中,反应过程中物质浓度变化如上图2所示。第12min时改变的反应条件可能为______________。
A.升高温度 B.加入NO C.加催化剂 D.降低温度
(2)工业上常采用“低温臭氧氧化脱硫脱硝”技术来同时吸收氮的氧化物(NOx))和SO2气体,在此过程中还获得了(NH4)2SO4的稀溶液。
①在(NH4)2SO4溶液中,水的电离程度受到了_______(填“促进”、“抑制”或“没有影响)”
②若往(NH4)2SO4溶液中加入少量稀盐酸,则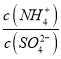 值将_________(填“变大”、“变小”或“不变”)。
值将_________(填“变大”、“变小”或“不变”)。
(3)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①煤燃烧产生的烟气中含有氮的氧化物,用CH4催化还原NOx可消除氮氧化物的污染。
已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867.0 kJ·mol-1
2NO2(g) ![]() N2O4(g) △H = - 56.9 kJ·mol-1
N2O4(g) △H = - 56.9 kJ·mol-1
则CH4催化还原N2O4(g)生成N2和H2O(g)的热化学方程式为______________。
(2)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极b作______极,表面发生的电极反应式为________________。

查看答案和解析>>
科目: 来源: 题型:
【题目】最能代表细胞膜基本化学成分的一组化学元素是( )
A. C、H、O、N B. C、H、O、N、P
C. C、H、O、S、P D. C、H、O、Mg、Fe
查看答案和解析>>
科目: 来源: 题型:
【题目】C是一种植物生长调节剂,用它可以催熟果实。根据以下化学反应框图填空:

(1)写出A的电子式__________________;
C的实验式______________________;
(2)写出碳化钙与水反应制取A的化学方程式_____________ ;苯和液溴反应生成D的化学方程式________________。
(3)写出 A→B的反应类型:_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】1,4﹣环己二醇是一种重要的化工原料,它可通过下列路线合成:

(1)反应⑧的反应类型是__________。
(2)有机物C按照系统命名,其名称是:_______,D中的官能团名称是______________。
(3)写出反应⑤的化学方程式为___________________________________。
(4)环己烷的一种同分异构体W,已知W分子中所有碳原子均在同一平面上,写出其结构简式_______________________,写出比W的相对分子质量少14的同系物中有顺反异构的顺式异构体的结构简式__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是:
A. 乙烷中混有乙烯可用酸性高锰酸钾溶液来除去
B. 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法
C. 已知2SO2(g)+ O2(g)![]() 2SO3 (g) △H<0,该反应在任何温度下均可自发进行
2SO3 (g) △H<0,该反应在任何温度下均可自发进行
D. 室温下,Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=9.0×10-12,向浓度相等的Na2CrO4和KCl溶液中滴加AgNO3溶液,最先生成Ag2CrO4沉淀
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验操作或方法中,不合理的是( )
A. 用丁达尔现象区分氯化钠溶液和淀粉溶液
B. 用重结晶法来提纯含有少量氯化钾杂质的硝酸钾晶体
C. 分别将SO2和Cl2通入滴有酚酞的氢氧化钠溶液中,验证两者的漂白性
D. 通过饱和碳酸氢钠溶液除去CO2中的HCl气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com