
科目: 来源: 题型:
【题目】I.根据下列叙述写出相应的热化学方程式:
(1)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,该反应的热化学方程式是__________________________。
(2)下图是198 K时N2与H2反应过程中能量变化的曲线图。
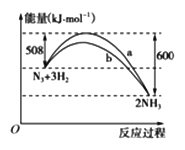
该反应的热化学方程式为:_____________________。
(3)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态水。已知室温下1 g甲硅烷自燃放出热量44.6 kJ,其热化学方程式是___________________。
II.
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是_____________________。
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) △H<0
C.2H2(g)+O2(g)=2H2O(1) △H<0
(2)以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其负极反应为__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】雷雨天闪电时空气中有臭氧(O3)生成,下列说法中不正确的是( )
A.O2和O3互为同素异形体
B.O3是由3个氧原子构成的化合物
C.O2和O3相互转化属于化学变化
D.O3的摩尔质量为48g.mol﹣1
查看答案和解析>>
科目: 来源: 题型:
【题目】可逆反应2NO2 ![]() 2NO + O2在体积不变的密闭容器中反应,现有以下几种说法:
2NO + O2在体积不变的密闭容器中反应,现有以下几种说法:
①反应混合物中各物质的物质的量浓度相等
②单位时间内生成n mol O2 的同时生成2n mol NO2
③用NO2、NO、O2的物质的量浓度变化表示的反应速率比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均摩尔质量不再改变的状态
其中表示达到平衡状态的表述是( )
A.①④ B.②④⑥ C.①②③ D.①②④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是某同学设计的放热反应的观察装置。
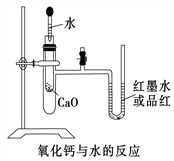
其实验顺序是:
①按图所示将实验装置连接好。
②在U形管内加入少量红墨水(或品红)溶液。打开T型管螺旋夹,使U形管内两边的液面处于同一水平面,再夹紧螺旋夹。
③在中间的试管里盛1 g氧化钙,当滴入2 mL左右的蒸馏水后,同时打开螺旋夹即可观察。
试回答:
(1)实验中观察到的现象是_____________________。
(2)该实验中必须进行的一步实验操作是______________。
(3)该实验的原理是_______________________________。
(4)实验中反应的化学反应方程式是_______________________。
(5)说明CaO、H2O的能量与Ca(OH)2的能量之间的关系_________________。
(6)若该实验中CaO换成NaCl,实验还能否观察到相同现象?______。
查看答案和解析>>
科目: 来源: 题型:
【题目】许多金属及它们的化合物在科学研究和工业生产中具有许多用途。回答下列有关问题:
(1)基态Ni核外电子排布式为____________;第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是______________。
(2)配合物 Ni(CO)n的中心原子价电子数与配体提供电子总数之和为 18,则n=_______, CO与N2结构相似,CO分子内σ 键与π键个数之比为_____________。
(3)NiO、FeO的晶体结构类型均与氯化钠的相同, 回答:
①Ni2+和 Fe2+的离子半径分别为69 pm 和78 pm, 则熔点NiO_______FeO(填“<”或“>”);
②NiO晶体中 Ni 的配位数为___________________;
(4) 金属 Cu 单独与氨水或单独与过氧化氢都不能反应, 但可与氨水和过氧化氢的混合溶液反应,其原因是_______________, 反应的离子方程式为_____________________。
(5)一种铜金合金晶体具有面心立方最密堆积的结构。在晶胞中,Au原子位于顶点,Cu原子位于面心,则该合金中Au原子与Cu原子个数之比为_______,若该晶胞的边长为a pm,则合金的密度为____g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
查看答案和解析>>
科目: 来源: 题型:
【题目】氢氧燃料电池已用于航天飞机,它是以铂作电极,以KOH溶液作电解质,下列叙述中不正确的是
A.H2在负极发生氧化反应
B.燃料电池的化学能可以全部转化为电能
C.产物为无污染的水,属于环境友好电池
D.供电时的总反应为:2H2 + O2 = 2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】对于硫酸工业中SO2的催化氧化反应 2SO2+O2![]() 2SO3,下列说法错误的是( )
2SO3,下列说法错误的是( )
A.使用催化剂能加快化学反应速率
B.增大O2浓度可以使SO2转化率达到100%
C.降低反应温度,化学反应速率减慢
D.增大O2浓度,化学反应速率增大
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中可以说明2HI(g)![]() H2(g)+I2(g)已达到平衡状态的是( )
H2(g)+I2(g)已达到平衡状态的是( )
(1)单位时间内生成n mol H2的同时生成n mol HI
(2)一个H—H键断裂的同时有两个H—I键断裂
(3)c(HI)= c(I2)
(4)反应速率υ(H2)=υ(I2)=0.5υ(HI)
(5)c(H2)∶c(I2)∶c(HI)=2∶1∶1
(6)温度和体积一定时,某一生成物浓度不再变化
(7)温度和体积一定时,容器内压强不再变化
(8)条件一定,混合气体的平均相对分子质量不再变化
(9)温度和体积一定时,混合气体的颜色不再发生变化
(10)温度和压强一定时,混合气体的密度不再发生变化
A. (1)(2)(5)(9)(10) B. (2)(6)(9) C. (6)(7)(10) D. 全部
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物H为芳香酯,其合成路线如下:
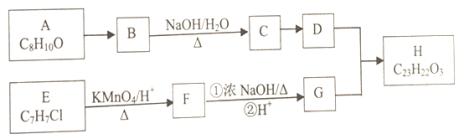
已知以下信息:
①A—H均为芳香族化合物,A的苯环上只有一个取代基,B能发生银镜反应,D的相对分子质量比C大4,E的核磁共振氢谱有3组峰。
② 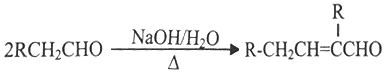
③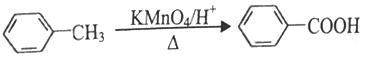
请回答下列问题:
(1)A→B的反应类型为____________,G所含官能团的名称为 ________________。
(2)B与银氨溶液反应的化学方程式为_____________________。
(3)H的结构简式为____________。
(4)符合下列要求的A的同分异构体有________________种。
①遇氯化铁溶液显紫色 ②属于芳香族化合物
其中苯环上有两个取代基的有 ___________________ (写结构简式)
(5)根据已有知识并结合相关信息,写出以CH3CH2OH为原料制备CH3CH2CH2CH2OH的合成路线流程图(无机试剂任用)______________合成路线流程图示例如下:
CH3CH2Br ![]() CH3CH2OH
CH3CH2OH ![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com