
科目: 来源: 题型:
【题目】CoCl2·6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2·6H2O的工艺流程如下:

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中Co2O3发生反应的离子方程式 。
(2)写出NaClO3发生反应的主要离子方程式 ;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式 。
(3)“加Na2CO3调pH至a”,过滤所得到的沉淀成分为 。
(4)“操作1”中包含3个基本实验操作,它们依次是 、 和过滤。制得的CoCl2·6H2O在烘干时需减压烘干的原因是 。
(5)萃取剂对金属离子的萃取率与pH的关系如图。向“滤液”中加入萃取剂的目的是 ;其使用的最佳pH范围是 。

A.2.0~2.5 B.3.0~3.5
C.4.0~4.5 D.5.0~5.5
(6)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是 。(答一条即可)
查看答案和解析>>
科目: 来源: 题型:
【题目】在恒温恒容的密闭容器中,对于可逆反应A(g)+B(g)![]() 2C(g),可以判断达到化学平衡状态的是
2C(g),可以判断达到化学平衡状态的是
A. 体系压强不变 B. A的浓度不变
C. 单位时间消耗mol A,同时生成2 nmol C D. 容器内气体密度不变
查看答案和解析>>
科目: 来源: 题型:
【题目】将足量CO2气体通入水玻璃中,然后加热蒸干,再在高温下充分燃烧,最后所得的固体物质是( )
A.硅酸钠 B.碳酸钠、硅酸钠
C.碳酸钠、二氧化硅 D.二氧化硅
查看答案和解析>>
科目: 来源: 题型:
【题目】纤维素被称为“第七营养素”,食物中的纤维素虽然不能为人体提供能量,但能促进肠道
蠕动、吸附排出的有害物质。从它的化学成分看,它是一种( )
A.二糖 B.多糖 C.氨基酸 D.脂肪
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于 ![]() 的说法正确的是( )
的说法正确的是( )
A. 所有碳原子不可能都在同一平面上
B. 最多只可能有9个碳原子在同一平面上
C. 有7个碳原子可能在同一直线上
D. 至少有14个原子在同一平面上
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关环境问题都是由化学物质引起的,其中对应关系不正确的是
A.温室效应﹣﹣﹣二氧化碳 B.光化学烟雾﹣﹣﹣二氧化氮
C.酸雨﹣﹣﹣二氧化碳 D.赤潮﹣﹣﹣含氮、磷的物质
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA代表阿伏加德罗常数,下列叙述正确的是
A. 78 g Na2O2中含有的离子总数为4NA
B. 标准状况下,1.12 L HF中所含的分子总数为0.05 NA
C. 由CO2和O2组成的混合物共有Na个分子,其中的氧原子数为2 NA
D. 0.1 mol L-1 FeCl3溶液中含有的Cl-数目为0.3 NA
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上利用CO和H2合成甲醇,而CO和H2来源于煤的气化。回答下列问题。
(I).(1)己知:①H2(g)+1/2O2(g)=H2O(g) △H1=-241.8kJ/mol
②C(s)+ ![]() O2(g)=CO(g) △H2=-110.5kJ/mol
O2(g)=CO(g) △H2=-110.5kJ/mol
则焦炭与水蒸气反应的热化学方程式为_____________。
(2)已知反应CO(g)+2H2(g)![]() CH3OH(g) △H=-99kJ/mol中的相关化学键键能如下:
CH3OH(g) △H=-99kJ/mol中的相关化学键键能如下:
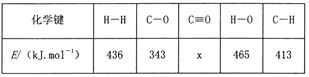
则x=________
(II)(3)在一容积可变的密闭容器中,lmolCO与2molH2发生反应:CO(g)+2H2(g) ![]() CH3OH(g), CO在不同温度下的平衡转化率(a)与总压强的关系如下图所示。
CH3OH(g), CO在不同温度下的平衡转化率(a)与总压强的关系如下图所示。
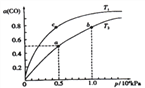
①该反应的△S_____0,图中的Tl____T2(填“>”、“<”或“=”)。
②该合成反应的温度一般控制在240~270℃,选择此温度范围的原因有:________。
③图中a点时以CH3OH的物质的量分数为_______,该反应的压强平衡常数为Kp=______(KPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)利用合成气(主要成分为CO和H2)合成甲醇,发生主要反应如下:
I: CO(g)+2H2(g) ![]() CH3OH(g) △H1
CH3OH(g) △H1
II:CO2(g)+H2(g) ![]() CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
III:CO2(g)+3H2(g) ![]() CH3OH(g) +H2O(g) △H31
CH3OH(g) +H2O(g) △H31
上述反应对应的平衡常数分别为K1、K2、K3,它们随温度变化曲线如下图所示。

则△H1______△H3(填“>”、“<”或“=”)。理由是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示,则下列对混合烃的判断正确的是( )
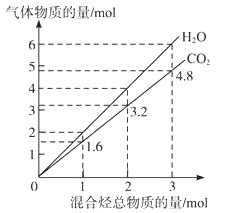
①一定有乙烯 ②一定有甲烷 ③一定有丙烷
④一定没有乙烷 ⑤可能有甲烷 ⑥可能有乙炔
A. ②⑤⑥ B. ②⑥ C. ②④ D. ②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com