
科目: 来源: 题型:
【题目】下列不能用于金属防腐处理的是( )
A. 涂油漆 B. 海轮在海洋上航行,为防止船体腐蚀,常在船体上镶上铜块
C. 在金属表面进行电镀 D. 改变金属内部结构
查看答案和解析>>
科目: 来源: 题型:
【题目】方铅矿(主要成分是PbS,含少量ZnS、Fe、Ag)是提炼铅及其化合物的重要矿物,其工艺流程如下:
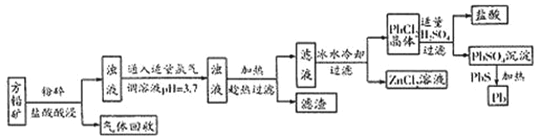
回答下列问题:
(1)流程中“趁热”过滤的原因是_____________,滤渣的主要成分是_________________。
(2)该工艺流程中可循环利用的物质是__________________。
(3)PbSO4与PbS在加热条件下发生反应的化学方程式为_____________________。
(4)《药性论》中有关铅丹(Pb3O4)的描述是:“治惊悸狂走,呕逆,消渴。”将PbO高温焙烧可制得铅丹,铅丹中含有的PbO与Al2O3性质相似,可用氢氧化钠溶液提纯铅丹,提纯时发生反应的离子方程是_______________。
(5)以石墨为电极,电解Pb(NO3)2溶液制备PbO2,电解过程中阳极的电极反应式为____________;若电解过程中以铅蓄电池为电源,当电解装置中阳极增重23.9g时(忽略副反应),理论上蓄电池负极增重_____g。
(6)取一定量含有Pb2+、Cu2+的工业废水,向其中滴加Na2S溶液,当PbS开始沉淀时,溶液中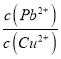 =__________。(已知KSP(PbS)=3.4×10-28,Ksp(CuS)=1.3×10-36)
=__________。(已知KSP(PbS)=3.4×10-28,Ksp(CuS)=1.3×10-36)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述中,正确的是
A.铝和酸、碱反应都表现出较强的还原性
B.铝箔在空气中受热熔化并迅速燃烧
C.钠燃烧后得到白色固体
D.自然界中钠以过氧化钠、氢氧化钠和氯化钠等形式存在
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E均为有机化合物,A是分子式为C5H10O的直链化合物,B与NaHCO3溶液完全反应,其物质的量之比为1:2,它们之间的关系如图所示(提示:RCH=CHR′在酸性高锰酸钾溶液中反应生成RCOOH和R′COOH,其中R和R′为烷基)。下列叙述错误的是( )
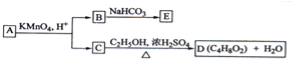
A.B的结构简式为HOOC﹣CH2﹣COOH
B.C与乙醇发生了酯化反应
C.A的结构简式是CH3﹣CH(OH)﹣CH=CH﹣CH3
D.E的分子式为C3H2O4Na2
查看答案和解析>>
科目: 来源: 题型:
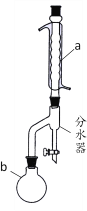
【题目】乙酸丁酯是优良的有机溶剂,因有愉快的果香气味,也用于香料工业。实验室制取乙酸丁酯的有关信息及装置示意图如下:
密度/(g·cm-3) | 沸点/℃ | 水溶性 | |
1-丁醇 | 0.81 | 117.7 | 可溶 |
乙 酸 | 1.05 | 117.9 | 互溶 |
乙酸丁酯 | 0.88 | 126.3 | 微溶 |
实验操作流程为:

(1)装置a的名称是_____________,其中冷却水的流动方向是____________。
(2)制取乙酸丁酯的化学方程式为___________________________________。加热回流时,分水器中液体分为两层,适时放出水使上层液体流入烧瓶b,从平衡角度考虑,分水器的作用是________________________________________。
(3)反应结束后,把分水器中的酯层和b中的反应液一起倒入分液漏斗中。在分液漏斗中加入10mL水洗涤,除去下层,上层继续用10mL10%Na2CO3溶液洗涤至中性,分液后将上层液体再用10mL水洗涤,除去溶于酯中的少量无机盐。下列说法不正确的是____________(填序号)。
A.最初用10mL水洗涤的目的是除去酸及少量的正丁醇
B.用10mL10%Na2CO3洗涤的目的是除去残留的硫酸和乙酸
C.分液时先将水层从分液漏斗的下口放出,再将乙酸丁酯从上口倒出
D.分液时先将水层从分液漏斗的下口放出,再将乙酸丁酯从下口放出
(4)在洗涤、分液后的乙酸丁酯中加入少量无水硫酸镁,其目的是________________________。
(5)在蒸馏操作中,仪器选择及安装都正确的是________(填标号)。
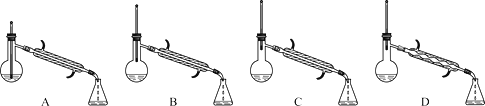
(6)本实验的产率是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关说法正确的是
A.H2SO4、NaOH、NaNO3都是强电解质
B.Na2O、Al2O3、Fe2O3都是碱性氧化物
C.磁铁矿、铝土矿、小苏打都是混合物
D.烧碱、纯碱、熟石灰都是碱
查看答案和解析>>
科目: 来源: 题型:
【题目】丙烯醇(CH2=CH—CH2OH)可发生的化学反应有( )
①加成 ②氧化 ③燃烧 ④加聚 ⑤取代
A. ①②③B. ①②③④
C. ①②③④⑤D. ①③④
查看答案和解析>>
科目: 来源: 题型:
【题目】下列电离方程式中,书写错误的是 ( )
A. Ca(OH)2=Ca2++2OH- B. NaOH=Na++O2-+H+ C. HCl=H++Cl- D. K2SO4=2K++SO42-
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸镁晶体(MgSO4·7H2O)是一种重要的化工原料。以菱镁矿(主要成分是MgCO3,含少量FeCO3和不溶性杂质)为原料制取硫酸镁晶体的流程如下:
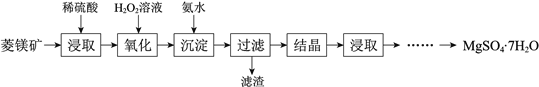
(1)MgCO3溶于稀硫酸的离子方程式是_________________________。
(2)加入H2O2溶液的目的是____________________(用离子方程式表示)。
(3)已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
阳离子 | Mg2+ | Fe2+ | Fe3+ |
开始沉淀 | 9.1 | 7.6 | 1.9 |
完全沉淀 | 11.1 | 9.7 | 3.2 |
“沉淀”步骤中,用氨水调节溶液pH的范围是______________________________。
(4)“过滤”所得滤液中存在大量的阳离子有Mg2+、____________。
(5)“结晶”步骤中需蒸发浓缩滤液,使用的仪器有铁架台、酒精灯和_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com