
科目: 来源: 题型:
【题目】下列有关原电池和电解池的叙述中,正确的是
A.纯锌与稀硫酸的反应比Zn-Cu合金与稀硫酸的反应更快
B.钢铁发生吸氧腐蚀时,负极的反应式为:Fe-3e-=Fe3+
C.在铁制容器上镀铜时,铁制容器连接外接电源的正极
D.电解精炼铜时,阴极的电极反应为:Cu2+ + 2e-=Cu
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与我们人类生活息息相关,下列说法不正确的是
A. 开发氢能、太阳能、风能、生物质能等是实现“低碳生活”的有效途径
B. 工业上,电解熔融MgCl2制金属镁
C. 研发使用高效催化剂,可提高反应中原料的转化率
D. “冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高
查看答案和解析>>
科目: 来源: 题型:
【题目】由锌、铁、铝、镁四种金属中的两种组成的混合物10g,与足量的盐酸反应产生的氢气在标准状况下为11.2L,则混合物中一定含有的金属是
A. 锌 B. 铁 C. 铝 D. 镁
查看答案和解析>>
科目: 来源: 题型:
【题目】有一在空气里暴露过的KOH固体样品,经分析其含水7.65%,含K2CO34.32%,其余是KOH。若将ag样品放入bmL1mol/L的盐酸中,使其充分作用后,残酸用25.25mL,cmol/L的KOH溶液恰好中和完全。蒸发所得溶液,得到固体质量的表达式中(单位g) ( )
A. 只含有a B. 只含有 b C. 可能含有b D. 一定有a、b和c
查看答案和解析>>
科目: 来源: 题型:
【题目】已知0.3 mol·L-1酒精溶液的密度为ρ1 g·mL-1,0.1 mol·L-1酒精溶液的密度为ρ2 g·mL-1,其中ρ1<ρ2,若将上述两溶液等质量混合,(忽略混合时溶液体积的变化)所得酒精溶液的物质的量浓度是 ( )
A. 等于0.2 mol·L-1 B. 大于0.2 mol·L-1
C. 小于0.2 mol·L-1 D. 无法估算
查看答案和解析>>
科目: 来源: 题型:
【题目】碳、硫的含量影响钢铁性能。某兴趣小组用如下流程对钢样进行探究。
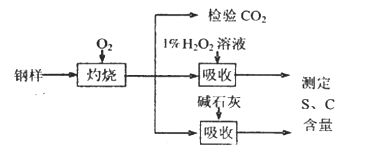
(1)钢样中硫元素以FeS形式存在,FeS在足量氧气中灼烧,生成的固体产物中Fe、O两种元素的质量比为21:8,则该固体产物的化学式为_____________。
(2)检验钢样灼烧生成气体中的CO2,需要的试剂是____________ (填字母)。
a.酸性KMnO4溶液 b.澄清石灰水 c.饱和小苏打溶液 d.浓H2SO4
(3)取10.00 g钢样在足量氧气中充分灼烧,将生成的气体用足量1%的H2O2溶液充分吸收,再用0.1000 mol·L-1NaOH溶液滴定吸收液至终点,消耗NaOH溶液20.00mL;另取10.00g钢样在足量氧气中充分灼烧,将生成的气体通过盛有足量碱石灰的U型管(如下图),碱石灰增重0.614 g。
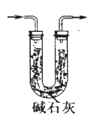
①用l%H2O2溶液吸收SO2,发生反应的离子方程式为___________________。
②分别计算该钢样中硫、碳元素的质量分数(写出计算过程)。
③实验测得的碳元素质量分数比真实值偏高,其可能的原因是______________(填字母)
a.U型管中生成的亚硫酸盐吸收了O2
b.碱石灰吸收了空气中的CO2
c.气体通过碱石灰的流速过快,末被充分吸收
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、NH![]() 、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO
、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO![]() 、SO
、SO![]() 、CO
、CO![]() ,已知:
,已知:
①五种盐均溶于水,水溶液均为无色。
②D的焰色反应呈黄色。
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失。
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题:
(1)五种盐中,一定没有的阳离子是__________________;所含阴离子相同的两种盐的化学式是_________________。
(2)D的化学式为 __________________,D溶液显碱性的原因是_____________________(用离子方程式表示)。
(3)A和C的溶液反应的离子方程式是_____________________;
E和氨水反应的离子方程式是_____________________________________。
Ⅱ.向100 mL FeI2溶液中逐渐通入Cl2,会依次生成I2、Fe3+、IO![]() ,其中Fe3+、I2的物质的量随n(Cl2)的变化如图所示,请回答下列问题:
,其中Fe3+、I2的物质的量随n(Cl2)的变化如图所示,请回答下列问题:
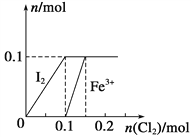
(1)由图可知,I-、Fe2+、I2三种粒子的还原性由强到弱的顺序为__________________;
(2)当n(Cl2)=0.12 mol时,溶液中的离子主要为_____________________,
从开始通入Cl2到n(Cl2)=0.12 mol时的总反应的化学方程式为_________________________
(3)当溶液中n(Cl-)∶n(IO![]() )=8∶1时,通入的Cl2在标准状况下的体积为_____________。
)=8∶1时,通入的Cl2在标准状况下的体积为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com