
科目: 来源: 题型:
【题目】下列各物质的沸点按由高到低顺序排列的是
①乙醇 ②乙烷 ③丙烷 ④乙二醇 ⑤1,2,3-丙三醇
A. ①③④②⑤ B. ①④⑤③②
C. ⑤④①③② D. ⑤①③④②
查看答案和解析>>
科目: 来源: 题型:
【题目】用黄铁矿(FeS2)、氯酸钠和硫酸溶液混合反应制备ClO2气体,再用水吸收该气体可得ClO2溶液。
(1)已知:黄铁矿中的硫元素在酸性条件下可被![]() 氧化成
氧化成![]() ,若生成标准状况下3.36 L ClO2气体,至少需要黄铁矿的质量为 。
,若生成标准状况下3.36 L ClO2气体,至少需要黄铁矿的质量为 。
(2)工业上以“m(ClO2)/m(NaClO3)”作为衡量ClO2产率的指标。若取NaClO3样品3.0 g,通过反应和吸收获得200 mL ClO2溶液,取此溶液20 mL与37.00 mL 0.500 mol·L-1 (NH4)2Fe(SO4)2溶液充分反应后,过量的Fe2+再用0.040 0 mol·L-1 K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7标准溶液25.00 mL。
①写出ClO2溶液与(NH4)2Fe(SO4)2溶液反应的离子方程式 。
②试计算ClO2的“产率”(写出计算过程) 。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表列出了①~⑥六种元素在周期表中的位置。
族 周期 | ⅠA | 0 | ||||||
1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ||||
请按要求回答下列问题:
(1)写出①的元素符号___________________。
(2)⑥的原子结构示意图是_______________。
(3)写出③与⑤的单质反应的化学方程式__________________________。
(4)③和④中金属性较弱的是_______________(填化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)可作为脱氯剂,已知1mol Na2S2O3溶液恰好把4mol Cl2完全转化为Cl-离子,则S2O32-将转化成 ( )
A. SO42- B. S C. SO32- D. S2-
查看答案和解析>>
科目: 来源: 题型:
【题目】Na2CO3俗名纯碱,下面是对纯碱采用不同分类法的分类,不正确的是
A、Na2CO3是碱 B.Na2CO3是盐 C.Na2CO3是钠盐 D.Na2CO3是碳酸盐
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上常以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)和H2SO4为原料,制备高纯PbO和副产品Na2SO4。其工作流程如下:
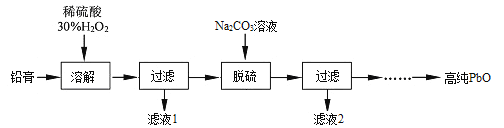
(1)①该工艺中采用H2O2取代原工艺中的FeSO4减少了杂质的进入,写出溶解时H2O2参与反应的离子方程式 。
②脱硫过程是把PbSO4转化为PbCO3,然后煅烧生成PbO而不直接煅烧PbSO4生成PbO,其原因是 。
③煅烧碳酸铅得到粗PbO。在NaOH溶液中,存在平衡:
PbO(s)+NaOH(aq)![]() NaHPbO2(aq) ΔH>0,其溶解度曲线如图所示。
NaHPbO2(aq) ΔH>0,其溶解度曲线如图所示。
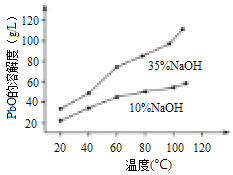
结合上述溶解度曲线,简述由粗PbO制备高纯PbO的实验方案: 。
(2)滤液1和滤液2按一定比例混合得到主要成分为Na2SO4及少量Pb2+等重金属离子的混合液,实验室中提纯其中的Na2SO4步骤如下:
Ⅰ.取100 mL滤液,调节滤液的pH,向滤液中加入10 g活性炭充分搅拌,过滤
Ⅱ.加热滤液
Ⅲ.向滤液中加入100 mL乙醇
Ⅳ.过滤、洗涤,烘干
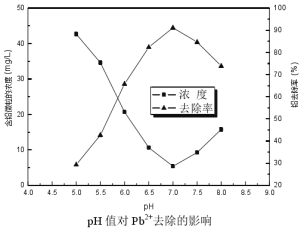
①不同pH下滤液中铅的去除率如图所示,pH>7时,铅去除率下降的原因可能是 。
②步骤Ⅱ加热除了把滤液浓缩到15%外,还有一个作用为 。
③步骤Ⅲ加入乙醇的作用为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸和硝酸都是重要的化工原料,也是化学实验室里必备的重要试剂。
(1)常温下,可用铁或者铝制的容器盛放浓硝酸,说明浓硝酸具有_________ 性
A.酸性 B.强氧化性 C.吸水性 D.脱水性
(2)工业上用洗净的废铜屑作原料来制备硫酸铜。下列制备方法符合“绿色化学”思想的是_______________________________(填序号)。
① Cu + H2SO4(浓)![]() CuSO4 ② Cu
CuSO4 ② Cu![]() CuO
CuO![]() uSO4
uSO4
写出①中反应的化学方程式:________________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】硫化钠在染料工业有着重要的用途。工业中常用煤粉(主要成分为碳)还原芒硝(Na2SO4)制备硫化钠。
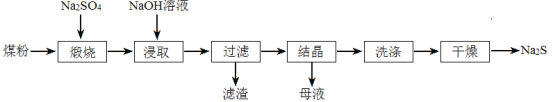
(1)①煅烧时煤粉把Na2SO4还原为Na2S,反应方程式为 。煤粉的作用是a.作为还原剂生成CO2、b. 。
②煅烧时常有副反应发生:Na2S+4CO2![]() Na2CO3+SO2+3CO
Na2CO3+SO2+3CO
4Na2S+O2![]() 2Na2S2+2Na2O
2Na2S2+2Na2O
为了控制杂质的生成可采取的措施是 。
(2)浸取用NaOH溶液而不用水的原因是 。
(3)滤渣需要用水洗涤回收,其目的是 。

(4)随温度升高溶液中Na2S最高含量如图所示,工业上加热滤液到100 ℃以上但只蒸发到含Na2S 38%—39%,然后冷却结晶,其原因是 。
(5)干燥需要在真空中操作,其原因是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法错误的是( )
A. 在NH![]() 和[Cu(NH3)4]2+中都存在配位键
和[Cu(NH3)4]2+中都存在配位键
B. H2O是极性分子,分子中O原子不处在2个H原子所连成的直线的中央
C. SO2、SO3、BF3、NCl3都是极性分子
D. 向含有0.1 mol [Co(NH3)4Cl2]Cl的水溶液中加入足量AgNO3溶液只能生成0.1 mol AgCl
查看答案和解析>>
科目: 来源: 题型:
【题目】屠呦呦受“青蒿一握,以水二升渍,绞取汁”启发,改用乙醚从青蒿中提取出抗疟药物青蒿素。青蒿素的提取过程不包含的操作是
A. 过滤B. 萃取C. 蒸馏D. 灼烧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com