
科目: 来源: 题型:
【题目】下列关于丙烯(CH3—CH=CH2)的说法正确的
A. 丙烯分子有8个σ键,1 个π键 B. 丙烯分子中3个碳原子都是sp3杂化
C. 丙烯分子不存在非极性键 D. 丙烯分子中所有原子都共平面
查看答案和解析>>
科目: 来源: 题型:
【题目】铁元素在地壳中含量丰富,下列有关说法不正确的是
A. 不锈钢属于铁合金B. 用KSCN溶液可检验溶液中的Fe3+
C. 铁制品腐蚀过程中铁被还原D. 铁矿石炼铁过程中涉及化学变化
查看答案和解析>>
科目: 来源: 题型:
【题目】碳及其化合物在工农业上有重要作用。
(1)水煤气是将水蒸气通过灼热的焦炭而生成的气体,水煤气的主要成分为_________
(用化学式表示);
(2)高温时,用CO还原MgSO4可制备高纯度MgO。若在750℃时,测得气体中含有等物质的量的SO2、SO3,则反应的化学方程式为____________;
(3)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。科学家提出由CO2制取碳的太阳能工艺如右图所示。
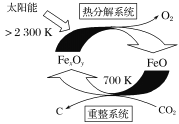
①若“重整系统”发生的反应中![]() =6,则FexOy的化学式为____________;
=6,则FexOy的化学式为____________;
②“热分解系统”中每分解1mol FexOy,转移电子的物质的量为____________。
(4)工业上用CO2和H2反应合成甲醚。
已知:2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(g) ΔH=130.8 kJ·mol-1
CH3OCH3(g)+3H2O(g) ΔH=130.8 kJ·mol-1
①一定条件下,上述合成甲醚的反应达到平衡状态后,若改变反应的某一个条件,下列变化能说明平衡一定向正反应方向移动的是____________(填标号)。
a.逆反应速率先增大后减小 b.反应物的体积百分含量减小
c.H2的转化率增大 d.容器中的n(CO2)/n(H2)值变小
②某压强下,合成甲醚的反应在不同温度、不同投料比时,CO2的转化率如图所示。
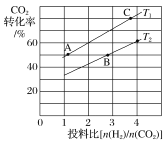
T1温度下,将4molCO2和8molH2充入2L的密闭容器中,5min后该反应达到平衡,则0~5min内的平均反应速率v(CH3OCH3)=______________;
KA、KB、KC三者之间的大小关系为_____________。
(5)常温下,用氨水吸收CO2可得到NH4HCO3溶液,在该溶液中,c(NH4+)________(填“>”、“<”或“=”)c(HCO3-;反应NH4++HCO3+H2O![]() NH3·H2O+H2CO3的平衡常数K=__________。
NH3·H2O+H2CO3的平衡常数K=__________。
(已知常温下NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数K1=4×10-7,K2=4×10-11)
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,Y和Z位于同一主族。m、n、p均为由这些元素组成的二元化合物,甲、乙、丙为其中三种元素对应的单质,丙为淡黄色固体,易溶在XZ2中,n是一种二元弱酸。上述物质的转化关系如图所示(反应条件省略)。下列说法正确的是
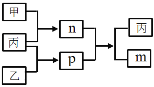
A.原子半径:W<X<Y
B.W与X组成的化合物中只有极性键
C.Y与Z组成的化合物一定有漂白性
D.非金属性:Y>Z>X
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有机物的鉴别方法(必要时可加热)不能达到实验目的的是
A. 用蒸馏水鉴别乙二醇、甲苯、氯苯
B. 用溴水鉴别苯、苯酚、2-己烯
C. 用酸性高锰酸钾溶液鉴别苯、甲苯、正己烷
D. 用含氢氧化钠的氢氧化铜悬浊液鉴别甲酸、乙醛、乙酸
查看答案和解析>>
科目: 来源: 题型:
【题目】若用AG表示溶液的酸度,其表达式为:AG=lg[![]() ]。室温下,实验室里用0.1 mol/L的盐酸溶液滴定10 mL 0.1 mol/L MOH溶液,滴定曲线如图所示:
]。室温下,实验室里用0.1 mol/L的盐酸溶液滴定10 mL 0.1 mol/L MOH溶液,滴定曲线如图所示:
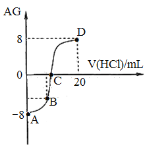
下列说法错误的是
A.该滴定过程应该选择甲基橙作为指示剂
B.C点时加入盐酸溶液的体积小于10 mL
C.滴定过程中从A点到D点溶液中水的电离程度逐渐增大
D.若B点加入的盐酸溶液体积为5 mL,所得溶液中:c(M+)+2c(H+)=c(MOH)+2c(OH)
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁酸盐是一种高效绿色氧化剂,可用于废水和生活用水的处理。从环境保护的角度看,制备高铁酸盐较好的方法为电解法:Fe+2H2O+2OH![]()
![]() +3H2↑,工作原理如图所示。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。下列说法正确的是
+3H2↑,工作原理如图所示。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。下列说法正确的是
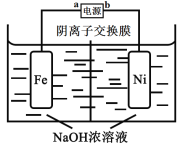
A.b是电源的正极
B.阳极电极反应为Fe6e+4H2O![]()
![]() +8H+
+8H+
C.电解过程中,不需要将阴极产生的气体及时排出
D.当电路中通过1mol电子的电量时,会有0.5mol的H2生成
查看答案和解析>>
科目: 来源: 题型:
【题目】大马酮是一种主要用于高级化妆品和食品的香料,可通过紫罗兰酮A以下列方法合成:

(1)B中的含氧官能团名称为 和 。
(2)D→E的反应类型为 。
(3)试剂X的分子式为C3H5Br,X的结构简式为 。
(4)写出同时满足下列条件的F的一种同分异构体的结构简式 。
①能与FeCl3溶液发生显色反应;
②分子中只有5种不同化学环境的氢。
(5)请以氯化苄![]() 和溴乙烷为原料制备苯丙烯
和溴乙烷为原料制备苯丙烯 ![]() ,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ氢、碳、氮都是重要的非金属元素,它们的单质及其化合物在科学研究和工业生产中有重要的应用。
(1)下列微粒基态的电子排布中未成对电子数最多的是__(填序号)
a.N3- b.Fe3+ c.Cu d.Cr e.C
(2)第一电离能介于B、N之间的第二周期元素有_____种。
(3)已知HCO3-在水溶液中可通过氢键成为二聚体(八元环结构),试画出该二聚体的结构式:____________________________。
(4)[Zn(CN)4]2-在水溶液中与HCHO发生如下反应:
4HCHO+[Zn(CN)4]2-+4H++4H2O![]() [Zn(H2O)4]2++4HOCH2CN
[Zn(H2O)4]2++4HOCH2CN
①Zn2+基态核外电子排布式为____。1 mol HCHO分子中含有σ键的物质的量为____mol。
②HOCH2CN分子中碳原子轨道的杂化类型是__。与H2O分子互为等电子体的阴离子为__。
③[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为______。
Ⅱ.由原子序数由小到大的A、B、C、D、E五种元素构成某配位化合物X,其原子个数比为14∶4∶5∶1∶1。其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-1)dn+6ns1,回答下列问题。
(1)该配位化合物X的化学式为________。
(2)元素B、C、D的第一电离能由小到大排列顺序为________。(用元素符号表示)
(3)D元素原子的最外层电子轨道表示式为________。
(4)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1∶1和1∶2,两种化合物可任意比互溶,解释其主要原因为_______________________。
(5)A元素与E元素可形成一种红色离子化合物Y,其原子个数比为1∶1,该化合物Y可与稀硝酸反应,生成一种蓝色溶液和两种无色气体(其中一种为A元素的单质),写出该反应的化学方程式_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com