
科目: 来源: 题型:
【题目】具有下列电子排布式的原子中,半径最大的是( )
A. 1s22s22p63s1B. 1s22s22p2C. 1s22s22p3D. 1s22s22p63s2
查看答案和解析>>
科目: 来源: 题型:
【题目】若用X代表F、C1、Br、I四种卤族元素,下列能够表达它们的共性反应的是( )
A. X2+H2=2HX B. X2+H2O=HX+HXO
C. 2Fe+3X2=2FeX3 D. X2+2NaOH=NaX+NaXO+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】电化学及溶解沉淀的相关问题
(1)由下列物质冶炼相应金属时,采用电解法的是________(填字母,下同)。
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的
是_________。
a.电能全部转化为化学能 b.粗铜接电源正极、发生氧化反应
c.溶液中Cu2+向阳极移动 d.利用阳极泥可回收Ag、Pt、Au等金属
e.若阳极质量减少64g,则转移电子数为2NA个 f. SO42-的物质的量浓度不变(不考虑溶液体积变化)
(3)以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为:______________。
(4)高铁电池的总反应为3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,该电池放电时正极反应式为____________。
3Zn(OH)2+2Fe(OH)3+4KOH,该电池放电时正极反应式为____________。
(5) 为了研究难溶盐的沉淀溶解平衡和沉淀转化,某同学设计如下实验。
步骤1:向2mL0.005mol·L-1AgNO3溶液中加入2mL0.005 mol·L-1KSCN溶液,静置 | 出现白色沉淀 |
步骤2:取1mL上层清液于试管中,滴加1 mol·L-1滴2Fe(OH3)3溶液。 | 溶液变为红色 |
步骤3:向步骤2的溶液中,继续加入5滴3 mol·L-1AgNO3溶液 | 现象a_____________, 溶液红色变浅。 |
步骤4:向步骤1余下的浊液中加入5滴3 mol·L-1KI溶液 | 出现黄色沉淀。 |
已知:. AgSCN是白色沉淀。
Ⅱ. 相同温度下,Kap(AgI)=8.3×10-17,Kap(AgSCN)=1.0×10-12。
①步骤3中现象a是__________________。
②用沉淀溶解平衡原理解释步骤4的实验现象_________________。
③向50mL0.005 mol·L-1AgNO3溶液中加入150mL0.005 mol·L-1的KSCN溶液,混合后溶液中Ag+的浓度约为___________mol·L-1。(忽略溶液体积变化)
查看答案和解析>>
科目: 来源: 题型:
【题目】电解质溶液相关问题
(1)下列事实可证明氨水是弱碱的是_______(填字母序号)。
A.氨水能跟氯化亚铁溶液反应生成氢氧化亚铁
B.常温下,0.1 mol·L-1氨水pH为11
C.铵盐受热易分解
D.常温下,0.1 mol· L-1氯化铵溶液的pH 为5
(2)常温下,0.1 mol·L-1NaHCO3溶液的pH大于7,则溶液中c(H2CO3)_______c(CO32-)(填“>”、 “=”或“<”),原因是________(文字说明);常温下,已知0.1 mol·L-1NaHCO3溶液的pH等于8,则溶液中c(H2CO3)-c(CO32-)=_____________mol··L-1(写出计算数值结果)。
(3)现有①Na2CO3溶液②CH3COONa溶液③NaOH溶液各25mL,物质的量浓度均为0.1 mol·L-1,下列说法正确的是_____________。
A.3种溶液pH的大小顺序是③>②>①
B.若将3种溶液稀释相同倍数,pH变化最大的是②
C.若分别加入25mL0.1 mol·· L-1盐酸后,pH最大的是①
D.若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>②
(4)用标准浓度的酸性KMnO4溶液滴定草酸(H2C2O4)溶液的测定其物质的量浓度。
① 滴定时,KMnO4溶液应装在__________(填“酸式”、“碱式”)滴定管中。
②滴定达到终点的标准是:__________________。
③滴定时所发生反应的离子方程式:_____________________。
④实验中,下列操作(其它操作正确)一定会造成测定结果偏高的是___________。
A.称取草酸晶体(7.2g)时,将草酸晶体放在托盘天平右盘
B.锥形瓶水洗后用草酸溶液润洗
C.读取KMnO4溶液体积时,开始仰视读数,滴定结束时俯视读数
D.盛KMnO4溶液的酸式滴定管尖嘴部分有气泡,滴定后气泡消失
查看答案和解析>>
科目: 来源: 题型:
【题目】研究人员最近开发出被称为第五形态的固体碳,这种新的碳结构被称作“纳米泡沫”,纳米泡沫碳与金刚石的关系是( )
A. 同素异形体 B. 同位素 C. 同系物 D. 同分异构体
查看答案和解析>>
科目: 来源: 题型:
【题目】乙烯是重要的化工原料,以乙烯为原料在不同条件下可合成下列物质(部分条件未标出):

(1)乙醇能与乙酸反应生成有果香味的物质,其名称为__________,该反应类型是____________
(2)反应⑥的化学方程式是______________实验现象是__________________
(3)反应③用KOH的乙醇溶液处理二氯乙烷制氯乙烯的方程式为:____________
(4)苯乙烯中所含官能团的名称_____________
(5)苯乙烯合成聚苯乙烯的化学方程式是_____________________
(6)以乙醇和苯乙烯为原料合成有机物![]() ,写出合成路线图_________________。
,写出合成路线图_________________。
(合成路线常用的表示方法为:![]() )
)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于苯(下图所示)的叙述正确的是( )
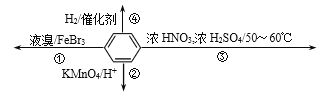
A. 反应②不发生,但是仍有分层现象,紫色层在下层
B. 反应①常温下能进行,其有机产物为![]()
C. 反应③为加成反应,产物是三硝基甲苯
D. 反应④中1mol苯最多与3 mol H2发生加成反应,是因为苯分子含有三个碳碳双键
查看答案和解析>>
科目: 来源: 题型:
【题目】1mol/L的硫酸溶液的含义是( )
A.1L水中含有1molH2SO4 B.一定量的溶液中含有1molH2SO4
C.将98g浓硫酸溶于水配成1L溶液 D.指1L硫酸溶液中含有98gH2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com