
科目: 来源: 题型:
【题目】金属具有延展性的原因是
A. 金属原子半径都较大,价电子数较少
B. 金属受外力作用变形时,金属阳离子与自由电子间仍保持较强烈的作用
C. 金属中大量自由电子受外力作用时,运动速率加快
D. 自由电子受外力作用时能迅速传递能量
查看答案和解析>>
科目: 来源: 题型:
【题目】4P(红磷s)![]() P4(白磷s) △H = +17kJmol﹣1根据以上方程式,下列推论正确的是
P4(白磷s) △H = +17kJmol﹣1根据以上方程式,下列推论正确的是
A. 正反应是一个放热反应
B. 当lmol白磷完全转变成红磷时放出17kJ热量
C. 当4g红磷转变成白磷时吸收17kJ热量
D. 白磷比红磷稳定
查看答案和解析>>
科目: 来源: 题型:
【题目】某钴矿石的主要成分为Co2O3,同时含有少量Fe2O3、Al2O3、MnO、MgO、CaO等杂质。用该种钴矿石制取CoC2O4·2H2O的工艺流程如下:
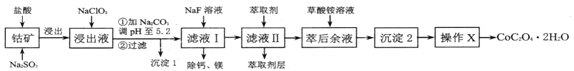
①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形成沉淀时溶液的pH见下表:
![]()
(1)写出两条提高浸出速率所采取的措施_______、________。
(2)浸出过程中加入Na2SO3的主要目的是___________。
(3)沉淀1的成分是___________(写化学式)。
(4)在C1O3-和Co3+中,氧化性最强的是_____________。
(5)浸出液中加入NaC1O3所发生反应的离子方程式为_________。
(6)滤液II中加入萃取剂的作用是__________。
(7)“操作X”包括______和_____________。
(8)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。当加入过量NaF后,所得滤液中c(Mg2+):c(Ca2+)= 0.67,则Ksp(MgF2)=_________(已知Ksp(CaF2)=1.10×10-10)。
查看答案和解析>>
科目: 来源: 题型:
【题目】.甲醇作为一种较好的可再生能源,具有广泛的应用前景。
已知在常温常压下反应的热化学方程式:
①CO(g)+2H2(g) ![]() CH3OH(g) H1=-90kJ·mol-1
CH3OH(g) H1=-90kJ·mol-1
②CO(g)+H2O(g) ![]() CO2(g) + H2(g) H2=-41kJ·mol-1
CO2(g) + H2(g) H2=-41kJ·mol-1
写出由二氧化碳、氢气制备甲醇的热化学方程式:___________________。
Ⅱ. 已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应 | 平衡 常数 | 温度 | ||
500℃ | 700℃ | 800℃ | ||
2H2(g) + CO(g) | K1 | 2.5 | 0.34 | 0.15 |
H2(g) + CO2(g) | K2 | 1 | 1.7 | 2.52 |
3H2(g)+CO2(g) | K3 | |||
请回答下列问题:
(1)反应①是__________(填“吸热”或“放热“)反应
(2)观察①②③可推导出K1、K2、K3之间的关系,则K3=_______(用K1、K2表示)
(3)某温度时,反应①式中各物质的平衡浓度符合下式:20×c(CH2OH)=3×c(CO)×c3(H2),试判断此时的温度为____________。
(4)500℃时测得反应③在某时刻H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度分别为0.4 mol· L-1、1 mol·L-1、0.5 mol·L-1、0.4 mol·L-1molL-1,则此时V(正)______V(逆)(填“>”、 “=”或“<”)。
(5)对应反应③,一定条件下将H2(g)和CO2(g)以体积比3:1置于恒温恒容的密闭容器发生反应,下列能说明该反应达平衡状态的有_____________。
A.体系密度保持不变
B.H2和CO2的体积比保持不变
C.混合气体的平均相对分子量不变时,反应一定达到平衡状态
D.当破坏CO2中2个碳氧双键,同时破坏H2O中的2个氧氢键,反应一定达到平衡状态
查看答案和解析>>
科目: 来源: 题型:
【题目】砹(At)是原子序数最大的卤族元素,推测砹或砹的化合物最不可能具有的性质是
A. HAt 很稳定 B. 砹易溶于某些有机溶剂
C. 砹是黑色固体 D. AgAt 难溶于水
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容器中,对于可逆反应A+3B![]() 2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是( )
2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是( )
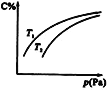
A. 若正反应方向ΔH<0,则T 1 >T 2
B. 压强增大时,混合气体的平均相对分子质量减小
C. B一定为气体
D. A一定为气体
查看答案和解析>>
科目: 来源: 题型:
【题目】目前世界上60%的镁是从海水中提取的.主要步骤如下: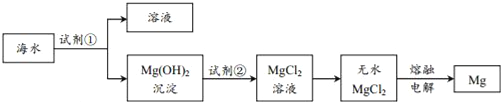
下列说法不正确的是( )
A. 为使海水中的MgSO4转化成Mg(OH)2,试剂①可选择石灰乳
B. 加入试剂①后,分离得到Mg(OH)2沉淀的方法是过滤
C. 加入试剂②反应的离子方程式为:OH﹣+H+=H2O
D. 通过电解熔融的无水MgCl2得到48gMg,共转移4mol电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com