
科目: 来源: 题型:
【题目】若将15P原子的电子排布式写成了1s22s22p63s23px23py1,则它违背了( )
A. 能量守恒原理 B. 泡利不相容原理
C. 能量最低原理 D. 洪特规则
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是
A. NaCl晶体属于离子晶体,熔化时离子键被削弱
B. CO2晶体属于分子晶体,汽化时需克服分子间作用力
C. SiO2晶体属于原子晶体,熔化时需破坏共价键
D. C60晶体与金刚石均属于原子晶体,其晶体熔点高、硬度大
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ、铁能形成多种价态的化合物,单质铁能被众多的氧化剂所氧化。
(1)将5.6g的生铁与足量的稀盐酸反应,生成H2的质量______0.2g(填“>”“<”“=”),向此生铁上滴加几滴稀硝酸,写出反应的离子方程式:___________________________。
(2)配制FeCl3溶液时常会出现浑浊现象,其原因是______________________(用离子方程式表示)。室温下配制5mol/L 200mL FeCl3溶液,至少需要添加_______mL 2mol/L的盐酸才会不出现浑浊(已知室温时Ksp[Fe(OH)3]=4.0×10-38,忽略加入盐酸对溶液体积的影响)。
(3)钢铁制品易生锈,导致其生锈的最主要原因是发生了________腐蚀;用NaOH、NaNO2等溶液对铁制品进行钝化处理可提高其抗腐蚀能力,下面是处理过程中所发生的一个反应:____Na2FeO2+_____NaNO2+_____H2O===_____Na2Fe2O4+_____NH3↑+_____,请完善该反应方程式。
II、硝化法是一种古老的生产硫酸的方法,同时实现了氮氧化物的循环转化,主要反应为
NO2(g)+SO2(g)![]() SO3(g)+NO(g)△H=-41.8kJ·mol-1
SO3(g)+NO(g)△H=-41.8kJ·mol-1
(1)下列说法中可以说明该反应已达到平衡状态的是_________。
a. 体系内混合气体的密度保持不变 b. ![]()
c. 容器内气体的总压强保持不变 d. NO体积分数不再改变
(2)某温度下,NO2(g)+SO2(g)![]() SO3(g)+NO(g)的平衡常数k=2.25,该温度下在甲、乙、丙三个体积为2L的恒容密闭容器中,投入NO2(g)和SO2(g),其起始浓度如下表所示。
SO3(g)+NO(g)的平衡常数k=2.25,该温度下在甲、乙、丙三个体积为2L的恒容密闭容器中,投入NO2(g)和SO2(g),其起始浓度如下表所示。
起始浓度 | 甲 | 乙 | 丙 |
c(NO2)/mol/L | 0.10 | 0.20 | 0.20 |
c(SO2)/mol/L | 0.10 | 0.10 | 0.20 |
①10min后,甲中达到平衡,则甲中反应的平均速率![]() ___________。
___________。
②丙达到平衡所用的时间_________(填“<”“>”“=”)10min,达到平衡后,设甲、乙、丙中SO2(g)的转化率分别为a、b、c,则三者的大小关系为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是
A. 含有NA个氯原子的氯气的质量是71g
B. 标准状况下,2.24L CCl4所含分子数为0.1 NA
C. 1L 1mol/L 盐酸中所含离子总数为NA
D. 2.4g镁在足量的氧气中燃烧,转移的电子数为0.2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为长式周期表的一部分,其中的编号代表对应的元素。
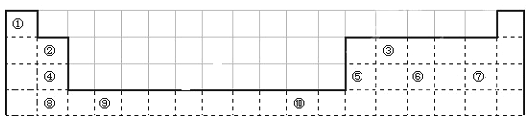
请回答下列问题:
(1)表中属于d区元素的是________(填元素符号)。
(2)⑥和⑦形成的分子中各个原子均满足8电子稳定结构,其立体构型为________。
(3)某元素原子的外围电子排布式为nsnnpn+1,该元素原子和⑦形成的分子,中心原子上的价层电子对数为_______。
(4)元素⑦和⑧形成的化合物的电子式为__________。
(5)元素⑩的基态+2价离子的电子排布式是__________。
(6)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质.请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】对于反应:2SO2+O2![]() 2SO3,当其他条件不变时,只改变一个条件,将生成SO3的反应速率的变化填入下表格里(填“增大”、“ 减小”或“不变”)。
2SO3,当其他条件不变时,只改变一个条件,将生成SO3的反应速率的变化填入下表格里(填“增大”、“ 减小”或“不变”)。
编号 | 改变的条件 | 生成的SO3的速率 |
① | 降低温度 | _______ |
② | 升高温度 | _______ |
③ | 增大O2的浓度 | _______ |
④ | 恒容下充入Ne | _______ |
⑤ | 压缩体积 | _______ |
⑥ | 使用催化剂 | _______ |
查看答案和解析>>
科目: 来源: 题型:
【题目】高分子树脂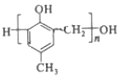 ,化合物C和化合物N的合成路线如下
,化合物C和化合物N的合成路线如下
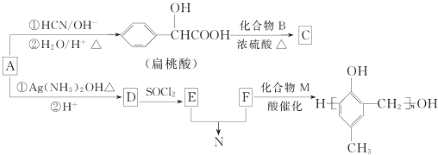 已知:
已知: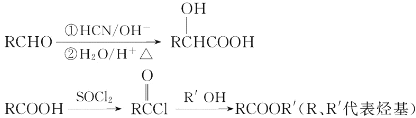 (1)A的结构简式为__________________,D的含氧官能团的名称是_______________。
(1)A的结构简式为__________________,D的含氧官能团的名称是_______________。
(2)A在催化剂作用下可与足量H2反应生成B.该反应的反应类型是____________,酯类化合物C的结构简式是________________________________________。
(3)F与醛类化合物M合成高分子树脂的化学方程式是____________________________________。
(4)酯类化合物N在NaOH溶液中发生水解反应的化学方程式是____________________________。
(5)扁桃酸(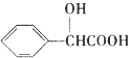 )有多种同分异构体.其中含有三个取代基,能与FeCl3溶液发生显色反应,也能与NaHCO3溶液反应放出气体的同分异构体共有______种,写出符合条件的三个取代基不相邻的一种同分异构体的结构简式________________________________________________。
)有多种同分异构体.其中含有三个取代基,能与FeCl3溶液发生显色反应,也能与NaHCO3溶液反应放出气体的同分异构体共有______种,写出符合条件的三个取代基不相邻的一种同分异构体的结构简式________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】I.可以由下列反应合成三聚氰胺:CaO+3C![]() CaC2+CO, CaC2+N2
CaC2+CO, CaC2+N2![]() CaCN2+C,CaCN2+2H2O=NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
CaCN2+C,CaCN2+2H2O=NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
(1)CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和_____(填化学式), 由此可以推知CN22-的空间构型为_______。
(2)三聚氰胺( )俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸(
)俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸(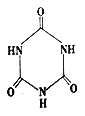 )
)
后,三聚氰酸与三聚氰胺分子相互之间通过______结合,在肾脏内易形成结石。
II.碳元素形成的单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔触的钾相互作用,形成某种青铜色的物质(其中的元素钾用“●”表示),原子分布如图所示,该物质的化学式为_________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com