
科目: 来源: 题型:
【题目】在怛容条件下,反应:2SO2 ( g ) + O2 ( g ) ![]() 2SO3( g ) ;△H =-QkJ·mol-1在上述条件下分别充入的气体和反应放出的热量 ( Q>0 )如下表所列:
2SO3( g ) ;△H =-QkJ·mol-1在上述条件下分别充入的气体和反应放出的热量 ( Q>0 )如下表所列:
容 器 | SO2 (mol) | O2(mol) | N2(mol) | Q(kJ·mol-1) |
甲 | 2 | 1 | 0 | Q1 |
乙 | 1 | 0.5 | 0 | Q2 |
丙 | 1 | 0.5 | 1 | Q3 |
根据以上数据,下列叙述正确的是
A. 在上述条件下反应生成 lmolSO3 固体放热 Q/2 kJ B. 2Q3 <2Q2=Q1<Q
C. Ql =2 Q2= 2Q3 = Q D. 2Q2 = 2Q3 < Q1 < Q
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)氮是地球上含量丰富的一种元素,氮及其化合物在工、农业生产和生活中有着重要作用。
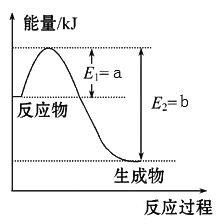
①上图是一定的温度和压强下N2和H2反应生成1molNH3过程中能量变化示意图,请写出工业合成氨的热化学反应方程式:____________________________。(△H的数值用含字母a、b的代数式表示)
②在25°C时,将x mol·L-1的氨水与y mol·L-1的盐酸等体积混合,反应后溶液显中性,则反应后的溶液中:c(NH4+)_______c(Cl-)(填“>”、“<”或“=”)
(2)海水中含有大量的元素,常量元素如氯、微量元素如碘在海水中均以化合态存在。在25°C时,向0.1mol·L-1的NaCl溶液中逐滴加入适量的0.1mol·L-1的硝酸银溶液,有白色沉淀生成,向反应后的浊液中,继续加入0.1mol·L-1的NaI溶液,看到的现象是________________,产生该现象的原因是(用离子方程式表示)___________________________。
(3)下图为一电化学装置,电极分别为铁棒和碳棒。U形管中盛有电解质溶液。
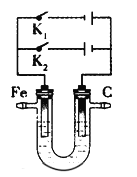
①若U形管中盛有饱和食盐水,打开K2,闭合K1, 铁棒为_______极,碳棒上的电极反应式为_______________________。
②若U形管中是含Cr2O72-的酸性废水,通过该装置可以除去Cr2O72-离子。闭合K2,打开K1,阳极区所发生的反应有:Fe-2e- =Fe2+和____________________ (写离子反应方程式)
查看答案和解析>>
科目: 来源: 题型:
【题目】S2Cl2是广泛用于橡胶工业的硫化剂,常温下S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体,其结构与H2O2类似。下列说法错误的是( )
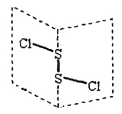
A. S2Cl2分子中的两个S原子均是sp3杂化
B. S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl
C. S2Br2与S2Cl2结构相似,熔沸点S2Br2>S2Cl2
D. S2Cl2分子中的S为+1价,是含有极性键和非极性键的非极性分子
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于氯气和氯水的说法中正确的是
A. 氯气是一种无色、密度比空气大的有毒气体
B. 红热的铁丝在Cl2中剧烈燃烧生成FeCl2
C. 新制氯水能使有色布条褪色是因为Cl2有漂白性
D. 氯水放置数天后酸性增强
查看答案和解析>>
科目: 来源: 题型:
【题目】下面有关晶体的叙述中,不正确的是
A. 金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子
B. 12g石墨中含有σ键的个数为2NA (NA表示阿伏伽德罗常数)
C. 氯化铯晶体中,每个Cs+周围紧邻8个Cl-
D. 干冰晶体中,每个CO2分子周围紧邻12个CO2分子
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是______________。若电解电路中通过2mol电子,MnO2的理论产量为______ 克。
(2)高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O![]() Na2FeO4+3H2↑,则电解时阳极的电极反应式是_____________________。
Na2FeO4+3H2↑,则电解时阳极的电极反应式是_____________________。
(3)用惰性电极电解100ml4mol/L的Cu(NO3)2溶液,一段时间后在阳极收集到标况下气体1.12L,
停止电解,向电解后的溶液中加入足量的铁粉,充分作用后溶液中Fe2+浓度为(设溶液体积不
变)_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】一种用烃A合成高分子化合物N的流程如下:
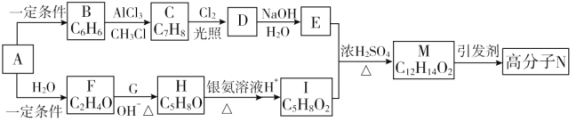
经测定烃A在标准状况下的密度为1.16 g·L-1;F和G是同系物;核磁共振氢谱显示有机物H中有四种峰,且峰值比为3∶3∶1∶1。
已知:Ⅰ.![]()
![]()
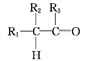
Ⅱ.![]() +R1Cl
+R1Cl![]()
![]() +HCl
+HCl
Ⅲ.R1CHO+R2CH2CHO![]()
![]() +H2O
+H2O
(R1、R2、R3代表烃基或氢原子)
(1) 写出A的结构简式:___________。
(2) H中所含官能团的名称是___________。
(3) H→I、M→N的反应类型分别是______、______。
(4) 写出F和G反应生成H的化学方程式:________________________________。
(5) E和I反应生成M的化学方程式为_________________________________。
(6) 芳香族化合物Q是M的同分异构体,与M具有相同官能团,且水解可以生成 2-丙醇,则Q有____种(不考虑立体异构)。
(7) 请参考以上流程,依照:原料![]() ……→产物模式,设计一个由乙烯合成2-丁烯醛的流程,无机试剂自选。
……→产物模式,设计一个由乙烯合成2-丁烯醛的流程,无机试剂自选。
____________________________________________________________________________________________________________________________________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】(10分)某化学活动小组设计以下装置进行不同的实验。其中a为用于鼓入空气的气囊,b为螺旋状铜丝,c中盛有冰水。
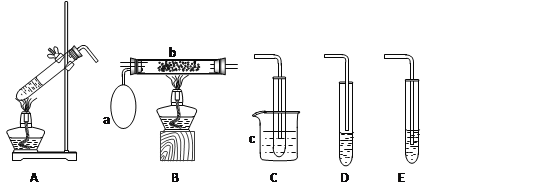
(1)若用A装置做乙醇与乙酸的酯化反应实验,则还需连接的装置是 (填序号),该装置中应加入试剂 。从实验安全角度考虑,A装置试管中除加入反应液外,还需加入的固体物质是 。
(2)该小组同学欲做乙醇氧化成乙醛的实验,则应选用的装置是 (填序号),再用制得的乙醛溶液进行银镜反应,正确的操作顺序是 (填序号)。
①向试管中滴入3滴乙醛溶液
②一边振荡一边滴入2%的稀氨水,直至最初产生的沉淀恰好溶解为止
③振荡后放入热水中,水浴加热
④在洁净的试管中加入1mL2%的AgNO3溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】有四种物质的量浓度相等且都由一价阳离子A+和B+及一价阴离子X-和Y-组成的盐溶液。据测定常温下AX和BY溶液的pH=7,AY溶液的pH>7,BX溶液的pH<7,由此判断不水解的盐是( )
A. BX B. AY C. AX D. BY
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇来源丰富、价格低廉,是一种重要的化工原料,有着重要的用途和应用前景。
(1)工业生产甲醇的常用方法是:CO(g)+2H2(g) ![]() CH3OH(g) △H = —91kJ/mol。
CH3OH(g) △H = —91kJ/mol。
已知:2H2(g)+O2(g)=2H2O(l) △H = —580kJ/mol;
2CO(g)+O2(g)=2CO2(g) △H = —570kJ/mol
计算2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(l) △H = ________________。
若在恒温恒容的容器内进行反应CO(g)+2H2(g) ![]() CH3OH(g),下列表示该反应没有达到平衡状态的有________(填字母序号)。
CH3OH(g),下列表示该反应没有达到平衡状态的有________(填字母序号)。
A.CO百分含量保持不变 B.容器中混合气体的密度不变化
C.有1个H—H键生成的同时有 3个C—H键生成 D.容器中混合气体的压强不变化
(2)制甲醇所需要的H2,可用下列反应制取:H2O(g)+CO(g) ![]() H2(g)+ CO2(g) △H<0,某温度下该反应达到平衡时,c(H2)·c(CO2)= c(CO)·c(H2O) 若起始时c(CO)=1mol/L-1,c(H2O)=1mol/L-1,试回答下列问题:
H2(g)+ CO2(g) △H<0,某温度下该反应达到平衡时,c(H2)·c(CO2)= c(CO)·c(H2O) 若起始时c(CO)=1mol/L-1,c(H2O)=1mol/L-1,试回答下列问题:
①该温度下,反应进行一阶段时间后,测得H2的浓度为0.5mol/L-1,则此时该反应v(正)__________v(逆)(填“>”、“<”或“=”);
②若反应温度不变,达到平衡后,H2O的转化率为________。
(3)某实验小组设计了甲醇以氢氧化钾为电解质溶液的燃料电池装置。
①试想该电池工作时,OH— 向_______极移动(填“负”或“正”);
②工作一段时间后,测得溶液的pH减小,该电池负极反应的离子方程式为______________________。总反应的化学方程式______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com