
科目: 来源: 题型:
【题目】t℃时,将0.200mol/L的某一元酸HA与0.200mol/L的NaOH溶液等体积混合,所得混合溶液中部分离子浓度如下表。
微粒 | H+ | Na+ | A- |
浓度(mol/L) | 2.50×10-10 | 0.100 | 9.92×10-2 |
下列说法中正确的是
A. 所得溶液中: c(Na+) >c(A-) >c(HA) >c(OH-)
B. t℃时,水的离子积Kw < 1.0×10-14
C. t℃时,一元酸HA的电离常数K=3.10×10-8
D. t℃时,0.100mol/LNaA溶液中A-的水解率为0.400%
查看答案和解析>>
科目: 来源: 题型:
【题目】谢弗勒尔盐(Cu2SO3·CuSO3·2H2O)是一种深红色固体,不溶于水和乙醇,100℃时发生分解。可由CuSO4·5H2O和SO2等为原料制备,实验装置如下图所示:
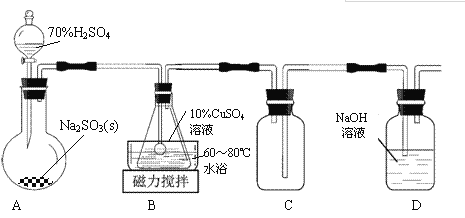
(1)装置A在常温下制取SO2时,用较浓的硫酸而不用稀硫酸,其原因是_______________。
(2)装置B中发生反应的离子方程式为_______________。
(3)装置C的作用是____________________。
(4)从B中获得的固体需先用蒸馏水充分洗涤,再真空干燥。
①检验洗涤已完全的方法是__________________。
②不用烘干的方式得到产品,其原因是________________。
(5)请补充完整由工业级氧化铜(含少量FeO)制备实验原料(纯净CuSO4·5H2O)的实验方案:向工业级氧化铜中边搅拌边加入稍过量的硫酸溶液,微热使其完全溶解,_______________,过滤,用95%酒精洗涤晶体2~3次,晾干,得到CuSO4·5H2O。
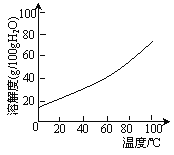
[已知:①该溶液中氢氧化物开始沉淀与沉淀完全时的pH范围分别为:Fe(OH)2(5.8,8.8);Cu(OH)2(4.2,6.7);Fe(OH)3(1.1,3.2)。②在水溶液中超过100℃,硫酸铜晶体易失去结晶水。③硫酸铜晶体溶解度曲线如右图所示]
查看答案和解析>>
科目: 来源: 题型:
【题目】二氯化砜(SO2Cl2)是一种无色液体,主要用于有机物和无机物的氯化等。其熔点为-54.1℃.沸点为69.2℃;常温下比较稳定,受热易分解,遇水剧烈反应生成硫酸和盐酸。
(1)制备。实验室可利用SO2和Cl2按下列装置制取少量SO2Cl2(丙中放有樟脑液,起催化作用)。已知SO2(g)+Cl2(g)![]() SO2Cl2(g) △H<0
SO2Cl2(g) △H<0
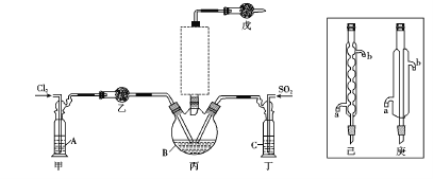
①可以用浓盐酸和酸性高锰酸钾制取氯气,该反应的化学方程式为 ;溶液A为 。
②上图实框中仪器己的名称为 ;反应装置图的虚框中未画出的仪器是 (填“己”或“庚”)。
③如果将丙装置放入冰水中,会更有利于二氯化砜的生成,其原因是 。
④下列有关说法错误的是 (填编号)。
a.乙、戊装置相同,在实验中的作用也完全相同
b.甲、丁装置为洗气装置,可用于气体的除杂和干燥
c.组装仪器后首先要进行的操作是检查装置的气密性
d.为提高反应物的利用率,可控制甲、丁装置中产生气泡的速率相等
(2)提纯。将收集到的产物进行减压蒸馏,减压蒸馏的目的是 。
(3)测定。取1.00g蒸馏后液体,小心地完全溶于水,向所得的溶液中加入足量氯化钡溶液,测得生成沉淀的质量为1.60g,则所得蒸馏成分中二氯化砜的质量百分含量为 %。
(4)贮存。二氯化砜应储存于阴凉、干燥、通风良好的库房。但久置后微显黄色,其原因是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,将3 mol A和1 mol B两种气体混合于2L恒容密闭容器中,发生如下反应:3A(g) + B(g)![]() xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol.L-l。下列判断正确的是( )
xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol.L-l。下列判断正确的是( )
A. A的转化率为40%
B. 2 min内B的反应速率为0.2 mol.L-l.min-1
C. x=2
D. 若混合气体的密度不变,则表明该反应已达到平衡状态
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组原子中,彼此的化学性质一定相似的是 ( )
A. P原子:1s2;Q原子:2s2
B. P原子:M能层上有2个电子;Q原子:N能层上有2个电子
C. P原子:2p能级上有1个未成对电子;Q原子:3p能级上也有1个未成对电子
D. P原子:最外层L能层上只有一个空轨道;Q原子:最外层M能层上也只有一个空轨道
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于Fe(OH)3胶体的说法中不正确的是:
A. Fe(OH)3胶体与食盐溶液混合将产生聚沉现象
B. Fe(OH)3胶体粒子在电场影响下将向阳极移动
C. 胶体中Fe(OH)3胶体粒子不停地作布朗运动
D. 光线通过Fe(OH)3胶体时会发生丁达尔效应
查看答案和解析>>
科目: 来源: 题型:
【题目】ClO2 是一种高效安全的杀菌消毒剂。用氯化钠电解法生成ClO2的工艺原理示意图如下图, 发生器内电解生成ClO2。下列说法正确的是
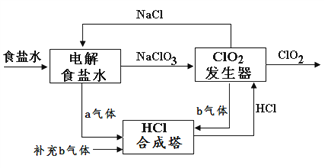
A. a气体是氯气,b气体是氢气
B. 氯化钠电解槽内每生成2 mol a气体,转移2mol e-
C. ClO2发生器中阴极的电极反应式为:2ClO3- + 12H+ + 10e-![]() Cl2↑ + 6H2O
Cl2↑ + 6H2O
D. 为使a、b气体恰好完全反应,理论上每生产1molClO2需要补充56L(标准状况)b气体
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各有机物的数目与分子式C4H7ClO2且能与NaHCO3溶液反应生成CO2的有机物的数目(不考虑立体异构)相同的是
A. 分子式为C5H10的烯烃 B. 甲苯的一氯代物
C. 相对分子质量为74的一元醇 D. 立方烷(![]() )的二硝基取代物
)的二硝基取代物
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某化学反应的平衡常数表达式为K=![]() ,在不同的温度下该反应的
,在不同的温度下该反应的
平衡常数如表所示
t ℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
下列有关叙述正确的是( )
A. 该反应的化学方程式是: H2(g)+CO2(g) ![]() CO(g)+H2O(g)
CO(g)+H2O(g)
B. 上述反应的正反应是吸热反应
C. 如果在一定体积的密闭容器中加入CO2和H2各1 mol,5 min后温度升高到830 ℃,如果此时测得CO2为0.5 mol,则该反应达到平衡状态
D. 某温度下,如果平衡常数符合下列关系式: ![]() =
=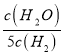 ,则此时温度700℃
,则此时温度700℃
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机物A化学式为CxHyOz , 15 g A完全燃烧可生成22 g CO2和9 g H2O。试求:
(1)该有机物的最简式______________;
(2)若A的相对分子质量为60,且A和Na2CO3溶液反应有气体放出,A和醇能发生酯化反应, 则A的结构简式为_________________;
(3)若A的相对分子质量为60,且A是易挥发有水果香味的液体,能发生水解反应,则其结构简式为_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com