
科目: 来源: 题型:
【题目】化学与能源开发、环境保护、资源利用等密切相关。下列说法正确的是
A. 为提高农作物的产量和质量,应大量使用化肥和农药
B. 绿色化学的核心是应用化学原理对环境污染进行治理
C. 实现化石燃料清洁利用,就无需开发新能源
D. 垃圾是放错地方的资源,应分类回收利用
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:![]()
水杨酸酯E为紫外吸收剂,可用于配制防晒霜。E的一种合成路线如下:

请回答下列问题:
(1)一元醇A中氧的质量分数约为21.6%。则A的分子式为 ;结构分析显示A只有一个甲基,A的名称为 。
(2)B能与新制的Cu(OH)2发生反应,该反应的化学方程式为 。
(3)C有 种结构;若一次取样,检验C中所含官能团,按使用的先后顺序写出所用试剂 ;
(4)第③的反应类型为 ;D所含官能团的名称为 。
(5)写出同时符合下列条件的水杨酸所有同分异构体的结构简式: 。
A、分子中含有6个碳原子在一条线上
B、分子中所含官能团包括水杨酸具有的官能团
(6)第④步的反应条件为 ;写出E的结构简式 。
查看答案和解析>>
科目: 来源: 题型:
【题目】[化学—选修3物质结构与性质] T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表。
元素 | 相关信息 |
T | T元素可形成自然界硬度最大的单质 |
W | W与T同周期,核外有一个未成对电子 |
X | X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/molkJ/mol,I4=11575kJ/mol |
Y | 常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质 |
Z | Z的一种同位素的质量数为63,中子数为34 |
(1)TY2是一种常用的溶剂,是 (填极性分子或非极性分子),分子中存在 个σ 键。W的最简单氢化物容易液化,理由是 。
(2)在25℃、101kpa下,已知13.5g的X固体单质在O2气体中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为 。
(3)基态Y原子中,电子占据的最高能层符号 ,该能层具有的原子轨道数为 、电子数为 。Y、氧、W元素的第一电离能由大到小顺序为 (用元素符号作答)。
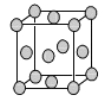
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00 g/cm3,则晶胞边长为 ;ZYO4常作电镀液,其中YO42-的空间构型是 ,其中Y原子的杂化轨道类型是 。元素Z与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z+HCl+O2=ZCl+HO2,HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是
A.O2是 氧化剂
B.HO2 是氧化产物
C. HO2在碱中能稳定存在
D.1 mol Z参加反应有1 mol电子发生转移
查看答案和解析>>
科目: 来源: 题型:
【题目】如图,直线交点处的圆圈为NaCl晶体中Na+离子或Cl-离子所处的位置。
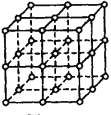
这两种离子在空间三个互相垂直的方向上都是等距离排列的。
(1)请将其中代表Na+离子的圆圈涂黑(不必考虑体积大小),以完成NaCl晶体的结构示意图。_______
(2)晶体中,在每个Na+离子的周围与它最接近的且距离相等的Na+离子共有_____个。
(3)晶体中每一个重复的结构单元叫晶胞。在NaCl晶胞中正六面体的顶点上、面上、棱上的Na+或Cl-离子为该晶胞与其相邻的晶胞所共有。一个晶胞中,Cl-离子的个数等于______,即______(填计算式),Na+离子的个数等于_______,即__________(填计算式)。
(4)设NaCl的摩尔质量为M g/mol,食盐晶体的密度为![]() g/cm3,阿伏加德罗常数为NA。食盐晶体中两个距离最近的钠离子中心间的距离为______cm。
g/cm3,阿伏加德罗常数为NA。食盐晶体中两个距离最近的钠离子中心间的距离为______cm。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)下面是4种粒子的结构示意图:
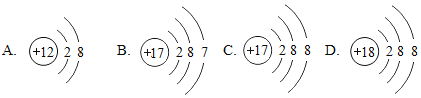
图中粒子共能表示_______种元素,图中表示的阳离子是____________(用离子符号表示),图中A所表示的元素在元素周期表中的位置_____________________________.
(2)在1-18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题:
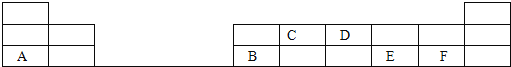
①写出D单质的电子式_____________________;
②写出C的最高价氧化物的结构式_____________________;
③E和F分别形成的气态氢化物中较稳定的是(填写氢化物的化学式)_____________________;
④A最高价氧化物的水化物所含化学键为___________________,其晶体类型为________,其水溶液与B反应的离子方程式为___________________________;
(3)X、Y、Z、M、N、Q皆为短周期主族元素,其原子半径与主要化合价的关系如图所示.下列说法正确的是 (______)

A.金属性:N>Q B.最高价氧化物对应水化物酸性:M>Y>N
C.简单离子半径:Q>N>X D.原子序数:Z>M>X>Y
查看答案和解析>>
科目: 来源: 题型:
【题目】单晶硅的晶体结构与金刚石一种晶体结构相似,都属立方晶系晶胞,如图:
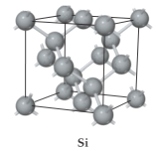
(1)将键联的原子看成是紧靠着的球体,试计算晶体硅的空间利用率(计算结果保留三位有效数字,下同)。
(2)已知Si—Si键的键长为234 pm,试计算单晶硅的密度是多少g/cm3。
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物A和G的结构简式分别为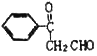 、
、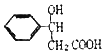 ,它们是一种重要的有机合成中间体,D、F为高分子化合物。
,它们是一种重要的有机合成中间体,D、F为高分子化合物。
(1)写出有机物G分子中两种含氧官能团的名称_______________。
(2)有机物G可以发生如下图的转化。请回答下列问题:
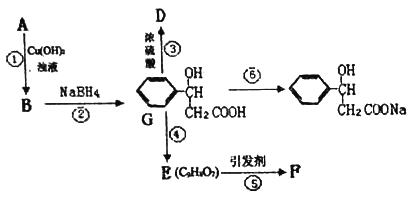
完成反应⑥可选用的试剂名称为___________________________________________,反应④的反应类型是___________________________________________。
写出下列反应的化学方程式:
反应①____________________________________。
反应③____________________________________;
反应⑤____________________________________。
(3)G的一种同分异构体![]() 是一种医药中间体。请设计合理方案用
是一种医药中间体。请设计合理方案用![]() 合成
合成![]() (其他原料自选,用反应流程图表示,并注明必要的反应条件)。例如:
(其他原料自选,用反应流程图表示,并注明必要的反应条件)。例如: ![]()
__________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】用废铅蓄电池的铅泥(含PbSO4、PbO和Pb等)可制备精细化工产品3PbO·PbSO4· H 2O(三盐),主要制备流程如下。
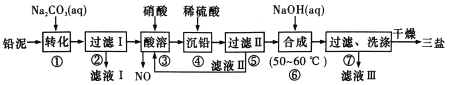
(1)铅蓄电池在生活中有广泛应用,其工作原理是Pb+PbO2+2H2SO4 ![]() 2PbSO4+2H2O。铅蓄电池在充电时,阳极的电极反应式为_________。若铅蓄电池放电前正、负极质量相等,放电时转移了lmol电子,则理论上两极质量之差为___________。
2PbSO4+2H2O。铅蓄电池在充电时,阳极的电极反应式为_________。若铅蓄电池放电前正、负极质量相等,放电时转移了lmol电子,则理论上两极质量之差为___________。
(2)将滤液I、滤液III合并,经蒸发浓缩、降温结晶、过滤等操作,可得到一种结晶水合物( Mr=322) ,其化学式为______________。
(3)步骤③酸溶时铅与硝酸反应生成Pb(NO3)2及NO的离子方程式为_____________;滤液II中溶质的主要成分为________(填化学式)。
(4)步骤⑥合成三盐的化学方程式为____________ 。
(5)步骤⑦的洗涤操作中,检验沉淀是否洗涤完全的操作方法是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】莽草酸是一种合成药物达菲的原料,鞣酸存在于苹果、生石榴等植物中。下列关于这两种有机化合物的说法正确的是

A. 莽草酸分子式为C7H10O5
B. 两种酸都能与溴水发生加成反应
C. 鞣酸分子与莽草酸分子互为同系物
D. 等物质的量的两种酸与足量氢氧化钠反应,消耗氢氧化钠的物质的量相同
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生产生活联系紧密,下列有关说法正确的是
A. 只用淀粉溶液即可检验食盐是否为加碘盐
B. 氢氟酸刻蚀水晶饰品体现其酸性
C. 水垢中的CaSO4,可先转化为CaCO3,再用酸除去
D. 煤经过气化和液化等物理变化可转为清洁能源
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com