
科目: 来源: 题型:
【题目】[化学——选修5:有机化学基础]
氯贝特(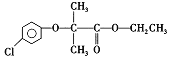 )是临床上一种抗血栓药物,它的一种合成路线如图28(图中部分反应条件及部分反应物、生成物已略去)。
)是临床上一种抗血栓药物,它的一种合成路线如图28(图中部分反应条件及部分反应物、生成物已略去)。
回答下列问题: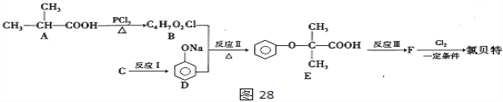
(1)有机物A命名为________,反应II的反应类型为_________,E分子中含有的官能团名称是___________。
(2)要实现反应I的转化,加入下列物质能达到目的有__________。
a. NaHCO3 b. NaOH c.Na2CO3 d. CH3COONa
(3)写出反应Ⅲ的化学方程式__________________________________ 。
(4)产物E有多种同分异构体,满足下列条件的所有同分异构体G有______种。
① 属于酯类且与FeCl3溶液显紫色 ② 能发生银镜反应
③ 1molG最多与2molNaOH反应 ④ 苯环上只有2个取代基且处于对位
其中核磁共振氢谱有五组峰的有机物结构简式为______________________。
(5)结合以上合成路线信息,设计以CH3CH2COOH为原料(无机试剂任选),合成有机物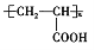 的合成流程。____________
的合成流程。____________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是( )
A. 烷烃分子中都存在碳碳单键
B. 乙醇与乙酸都存在碳氧双键
C. 普通食醋中含3%~5%(质量分数)的乙酸
D. 米酒变酸的过程涉及了酯化反应
查看答案和解析>>
科目: 来源: 题型:
【题目】NH3是一种重要的化工原料,可以制备一系列物质(见下图),下列说法正确的是( )
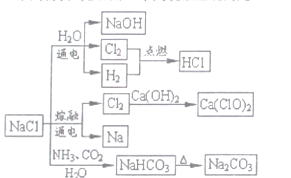
A. NH4Cl和NaHCO3都是常用的化肥
B. NH4Cl、HNO3和Na2CO3受热时都易分解
C. NH3和NO2在一定条件下可发生氧化还原反应
D. 图中所涉及的盐类物质均可与Ca(OH)2发生反应
查看答案和解析>>
科目: 来源: 题型:
【题目】配制物质的量浓度为0.1molL-1的Na2CO3溶液100 mL时,下列操作正确的是
A. 用托盘天平称取1.06 g 无水碳酸钠,在烧杯中加适量水溶解,待冷却到室温后,将溶液转移到容量瓶中
B. 在使用容量瓶前必须检查容量瓶是否完好以及瓶塞处是否漏水
C. 定容时,若加水超过刻度线,可用胶头滴管小心吸出多余部分
D. 定容时,若仰视,则所配溶液的浓度将偏高
查看答案和解析>>
科目: 来源: 题型:
【题目】铁及其化合物在生产和生活中有广泛的应用。
Ⅰ、高铁酸钠(Na2FeO4)是一种新型净水剂,工业上制备高铁酸钠的反应原理为:
Fe(OH)3 + NaClO + NaOH →Na2FeO4 + X + H2O(未配平), 则X的电子式为_______ ,反应中被氧化的物质是_________(写化学式)。
Ⅱ、铁红颜料跟某些油料混合,可以制成防锈油漆。工业制硫酸产生的硫酸渣中主要含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:
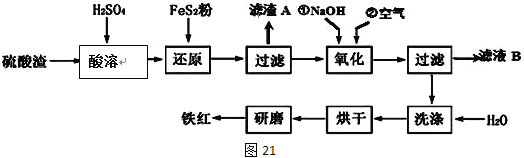
已知:
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
已知FeS2是一种黄色难溶于水的固体。
(1)酸溶过程中Fe2O3与稀硫酸反应的化学方程式为______________________;
“滤渣A”主要成份的化学式为__________________。
(2)还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4,写出该反应的离子方程式_________________。
(3)为确保铁红的质量和纯度,氧化过程中加NaOH调节溶液pH的范围是____;如果加NaOH调节溶液pH=a,则滤液B中c(Fe3+)=____mol/L(25℃时,Ksp[Fe(OH)3]=4×10﹣38)
(4)以甲醚、空气、氢氧化钾溶液为原料,石墨为电极可以构成燃料电池。该电池负极的电极反应式为________________ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A. 碳酸钙与稀盐酸反应:2H++CO![]() ===CO2↑+H2O
===CO2↑+H2O
B. 氯气与水反应:Cl2+H2O===2H++Cl-+ClO-
C. 氢氧化钡溶液与稀醋酸反应:H++OH-===H2O
D. 氯化铁溶液与铜反应:2Fe3++Cu===2Fe2++Cu2+
查看答案和解析>>
科目: 来源: 题型:
【题目】四种短周期元素在周期表中的位罝如图,其中只有M为金属元素。下列说法不正确的是( )

A. 原子半径Z
B. Y的最高价氧化物对应水化物的酸性比X的弱
C. X的最简单气态氢化物的热稳定性比Z的小
D. Z位于元素周期表中第2周期、第VIA族
查看答案和解析>>
科目: 来源: 题型:
【题目】有短周期主族元素A、B、C、D、E,其中A为地壳中含量最高的金属元素,B元素原子的M层电子数为最内层电子数的2倍,C的气态氢化物的水溶液呈碱性,D元素的最外层电子数是电子层数的3倍,E的单质为黄绿色气体,是制备漂白粉的原料。
请回答下列问题:
(1)D元素在周期表中的位置:______.
(2)A、D、E元素简单离子半径由大到小的顺序为________________(用微粒符号填).
(3)F与D同主族且相邻,其气态氢化物稳定性由大到小为___________(填化学式).
(4)用高能射线照射含有10电子的D元素氢化物分子时,一个分子能释放一个电子,同时产生一种具有较高氧化性的阳离子,试写出该阳离子的电子式______,该阳离子中存在的化学键有______.
(5)C元素的简单气态氢化物与E元素的单质反应有白烟生成,化学方程式为______.
(6)B的单质与强碱反应的离子方程式为______.
查看答案和解析>>
科目: 来源: 题型:
【题目】某次实验需用480mL、0.5mol/L的稀H2SO4溶液,某同学用98%的浓H2SO4(ρ=1.84g/cm3)进行配制,请回答下列问题:
(1)实验需要的玻璃仪器除了烧杯、胶头滴管、量筒、玻璃棒,还有__________________
(2)计算:98%的浓H2SO4(ρ=1.84g/cm3)的物质的量浓度为______,配制本次实验需要的稀硫酸需用量筒量取上述98%的浓H2SO4___________________ mL
(3)配制过程:①用量筒量取所需的浓硫酸
②将浓硫酸缓缓注入盛有适量蒸馏水的烧杯中,边加边搅拌
③用玻璃棒引流将烧杯中的溶液转移到已经检漏的合适规格的容量瓶中
④洗涤烧杯和玻璃棒2~3次,洗涤液也注入容量瓶中.轻轻摇动容量瓶,使溶液混合均匀
⑤向容量瓶中加入蒸馏水,在距离刻度1~2cm时,改用胶头滴管加蒸馏水至刻度线
⑥盖好瓶塞,反复上下颠倒,摇匀
⑦将配制好的溶液转移至试剂瓶中待用。
上述配置溶液的步骤存在缺失,缺少的步骤是_____________________,应放在步骤_____之前进行(填“序号”)。
(4)在横线上填写下列各种情况对所配制溶液浓度的影响(选填“偏高”、“偏低”或“无影响”).
①所用的浓硫酸长时间放置在密封不好的容器中______
②量取浓硫酸所用量筒有蒸馏水______
③定容时,俯视液面______.
④用量筒量取浓硫酸时仰视液面________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com