
科目: 来源: 题型:
【题目】(1)已知在常温常压下:
①CH3CH2OH(l)+3O2(g) ═ 2CO2(g)+3H2O(g) ΔH1=-1366kJ·mol-1
②H2O(g) ═ H2O(l) ΔH2=-44kJ·mol-1
③CH3CH2OH(l)+2O2(g)═2CO(g)+3H2O(l) ΔH3=-932kJ·mol-1
写出CO燃烧热的热化学方程式 ____________。
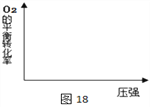
(2)在图18中画出不同温度下(T1>T2),上述反应③中O2的平衡转化率随压强变化的关系图(请在图上标注温度T1、T2)。________
(3)一定条件下,在体积为2 L的密闭容器中发生反应:CO(g) + 2H2(g)![]() CH3OH(g)达到化学平衡状态。
CH3OH(g)达到化学平衡状态。
①该反应的平衡常数表达式K=__________;根据图19判断,升高温度,平衡常数K值将_____(填“增大”、“减小”或“不变”)。

②500℃时,从反应开始至达到化学平衡,以H2的浓度变化表示的化学反应速率是____。
③X点与Y点的平均速率:v(X)____v(Y);其中X点的正反应速率v正(X)与Z点的逆反应速率v逆(Z)的大小关系为v正(X)____v逆(Z)(填“>”、“<”、“=”)。
(4)一定条件下,CO可与粉末状的氢氧化钠作用生成甲酸钠。
①已知常温时,0.1mol/L的甲酸溶液其pH约为2.4,请用离子反应方程式表示甲酸钠的水溶液呈碱性的原因_________。
②向20mL 0.1mol/L的甲酸钠溶液中小心滴加10mL 0.1mol/L的盐酸,混合液呈酸性,请按由大到小的顺序给溶液中离子浓度排序_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将等体积的SO2和Cl2充分混合,通入加有品红的氯化钡溶液,可观察到的现象是( )
A. 溶液快速褪色 B. 溶液缓慢褪色 C. 生成白色沉淀 D. 生成浅黄色沉淀
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量。某兴趣小组进行下面实验探究,查阅资料知道:
①2NO+Na2O2=2NaNO2
②2NO2+Na2O2=2NaNO3
③酸性KMnO4溶液可将NO2﹣氧化为NO3﹣,MnO4﹣被还原成Mn2+。
Ⅰ.产品制备与检验:用图20装置制备NaNO2
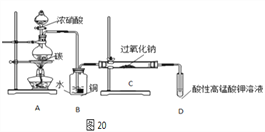
(1)写出装置A烧瓶中发生反应的化学方程式________________。
(2)B装置的作用是___________;盛浓硝酸的仪器名称为__________。
(3)有同学认为装置C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠,为制备纯净的NaNO2,应在B、C装置间增加一个干燥管。在干燥管中盛放的试剂名称为____________。
(4)请设计实验,检验装置C中NaNO2的存在(写出操作、现象和结论)_________。
Ⅱ.含量的测定
称取装置C中反应后的固体4.00g溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol/L酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
滴定次数 | 1 | 2 | 3 | 4 |
KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
(5)第一组实验数据出现异常,造成这种异常的原因可能是_________。
A.酸式滴定管用蒸馏水洗净后未用标准液润洗
B.锥形瓶洗净后未干燥
C.滴定结束后仰视读数
D.滴定结束后俯视读数
(6)根据表中数据,计算所得固体中亚硝酸钠的质量分数_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是:
A.甲烷的标准燃烧热为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式表示为:
CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B.500 ℃、30 Mpa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) ![]() 2NH3(g)ΔH=-38.6kJ·mol-1
2NH3(g)ΔH=-38.6kJ·mol-1
C.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的ΔH相同
D.HCl和NaOH反应的中和热△H=﹣57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(﹣57.3)kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于碳酸(H2CO3)和硅酸(H2SiO3)的说法中不正确的是( )
A. 两者均为弱酸
B. 两者均可使紫色石蕊试液变红色
C. CO2气体通入Na2SiO3溶液中可以制得硅酸
D. 两者受热时均可以分解
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 光导纤维的主要成分为二氧化硅 B. SiO2是酸性氧化物,它不溶于任何酸
C. SiO2的俗名叫水玻璃,不溶于水 D. Si在自然界中既有游离态又有化合态
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)合理膳食,保持营养均衡,是青少年学生健康成长的重要保证。秋葵是一种大众喜爱的食材,含有蛋白质、维生素A、维生素C、纤维素、阿拉伯果糖和丰富的铁、锌、钙等元素,根据上述内容回答下列问题:
①蛋白质在人体内最终的水解产物是_________________。
②属于人体所需微量元素的是____________________。
③属于脂溶性维生素的是_________________。
(2)材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
①硅酸盐产品在生活中使用广泛,下列不是硅酸盐产品的是 _______________。
A、水泥 B、陶瓷 C、玻璃 D、塑料
②玻璃是重要的硅酸盐产品。生产玻璃时,石灰石与石英反应的化学方程式为______。
(3)保持洁净安全的生存环境已成为全人类的共识,人与自然要和谐相处。
①pH<_________________的雨水称为酸雨;向煤中加入适量的__________________,可以大大减少燃物产物中SO2的量。
②天然水中杂质较多,常需加入明矾、ClO2等物质处理后才能饮用。加入ClO2的作用是
__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下的恒容容器中.当下列物理量不再发生变化时,不能表明反应:A(s)+3B(g)![]() 2C(g)+D(g)己达平衡状态的是( )
2C(g)+D(g)己达平衡状态的是( )
A. 混合气体的压强 B. 混合气体的密度
C. 3v逆(C)=2v正(B) D. 气体的平均相对分子质量
查看答案和解析>>
科目: 来源: 题型:
【题目】以烃A为主要原料,采用以下路线合成药物X、Y和高聚物Z。
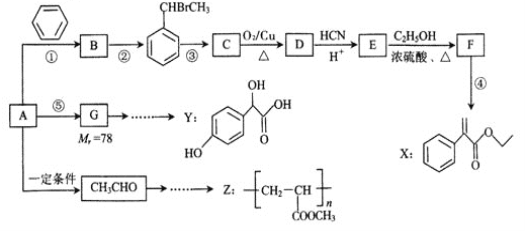
已知:
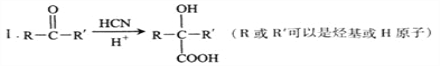
Ⅱ.反应①、反应②、反应⑤的原子利用率均为100%。
请回答下列问题:
(1)B的名称为______________。
(2)X中的含氧官能团名称为____,反应③的条件为_______,反应③的反应类型是_________。
(3)关于药物Y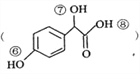 的说法正确的是_________________。
的说法正确的是_________________。
A.药物Y的分子式为C8H804,遇氯化铁溶液可以发生显色反应
B.1mol药物Y与H2、浓溴水中的Br2反应,最多消耗分别为4 mol和2 mol
C.1mol药物Y与足量的钠反应可以生成33.6 L氢气
D.药物Y中⑥、⑦、⑧三处- OH的电离程度由大到小的顺序是⑧>⑥>⑦
(4)写出反应E-F的化学方程式_____________________________________。
(5)写出符合下列条件的E的所有同分异构体的结构简式________________________。
①属于酚类化合物,且是苯的对位二元取代物;②能发生银镜反应和水解反应。
(6)设计一条以CH3CHO为起始原料合成Z的线路(无机试剂及溶剂任选) ___________________
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ、材料是人类赖以生存和发展的重要物质基础。
(1)钢筋混凝土是重要的建筑材料,钢筋混凝土______ (填“是”或“不是”)复合材料。
(2)有机玻璃受热时会软化,易于加工成型。有机玻璃是一种_________材料(选填“硅酸盐”或“纤维”或“塑料”)。
Ⅱ.(1)我国汉代器物和秦俑彩绘用的颜料“汉紫”,直到近来人们才研究出来,其成分为紫色的硅酸铜钡(铜为+2价),它的化学式为:BaCuSi2Ox,则x的值为 _________
(2)我国新修订的《环境保护法》,使环境保护有了更严格的法律依据。
①北京和张家口市已成功申办2022年冬奥会,目前北京市政府正在全力改善空气质量,下列指标不在空气质量报告范围内的是________ (填字母)。
SO2浓度 b. CO2浓度 c. 可吸入颗粒物
②废旧电池处理不当易造成重金属污染,治理废水中的重金属污染物可用沉淀法。例如,往含铅(Pb2+)废水中加入Na2S使Pb2+转变为__________ (填化学式)沉淀而除去。
③硝酸型酸雨的形成主要是由汽车排放的尾气所致,汽车尾气中的氮氧化物可以用氨气来处理。例如,氨气与二氧化氮在催化剂作用下反应生成的均是对空气无污染的物质,请写出此时氨气与二氧化氮反应的化学方程式: ______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com