
科目: 来源: 题型:
【题目】黄铁矿是生产硫酸的原料,其主要成分为FeS2。850950℃时,在空气中煅烧,发生反应
4FeS2 + 11O2![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
试回答下列问题:
(1)含硫35%的黄铁矿样品(杂质不含硫),其FeS2的含量为_____________
(2)可用来表示该反应的化学反应速率的物质为_________________(填化学式)。
(3)某时刻测得生成SO2的速率为0.64 mol·L-1·s-1,则氧气减少的速率为_____________
(4)为了提高SO2的生成速率,下列措施可行的是______________(填选项字母)。
A.增加硫铁矿石的投入量 B.增加炉的高度
C.将硫铁矿石粉碎 D.升高温度
查看答案和解析>>
科目: 来源: 题型:
【题目】热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO4+2LiCl+Ca = CaCl2+Li2SO4+Pb。下列有关说法正确的是
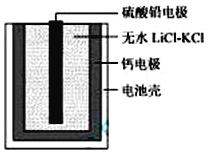
A.正极反应式:Ca + 2Cl--2e- = CaCl2
B.放电过程中,Li+向负极移动
C.常温时,在正负极间接上电流表或检流计,指针发生偏转
D.每转移0.1mol电子,理论上生成10.35 g Pb
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,可逆反应A(g)+3B(g)![]() 2C(g) 达到平衡状态的标志是
2C(g) 达到平衡状态的标志是
A. 生成的速率与A分解的速率相等
B. 单位时间生成nmolA,同时生成3nmolB
C. A、B、C的浓度不再变化
D. A、B、C的分子数比为1:3:2
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,在2 L密闭容器中投入一定量的A、B,发生反应3A(g)+bB(g) ![]() cC(g)。12 s时达到平衡,生成C的物质的量为0.8 mol,反应过程如图所示。下列说法正确的是
cC(g)。12 s时达到平衡,生成C的物质的量为0.8 mol,反应过程如图所示。下列说法正确的是
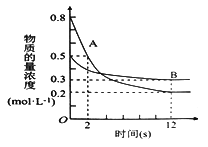
A. 前12 s内,A的平均反应速率为0. 025 mol L-1 s-1
B. 12 s后,A的消耗速率等于B的生成速率
C. 化学计量数之比b:c==1:2
D. 反应开始到12 s,A的转化率为70%
查看答案和解析>>
科目: 来源: 题型:
【题目】据报导,我国已研制出“可充室温钠一二氧化碳电池”,电极材料为钠金属片和碳纳米管,电解液为高氯酸钠一四甘醇二甲醚,电池总反应为:4Na+3CO2![]() 2Na2CO3+C,生成固体Na2CO3沉积在碳纳米管上。下列叙述不正确的是
2Na2CO3+C,生成固体Na2CO3沉积在碳纳米管上。下列叙述不正确的是
A. 放电时钠金属片发生氧化反应
B. 充电时碳纳米管接直流电源的正极
C. 放电时每消耗3molCO2,转移12mol电子
D. 充电时的阳极反应为C+2Na2CO3-4e-=3CO2↑+4Na+
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上测量SO2、N2、O2混合气体中SO2含量的装置如右图。反应管中装有碘的淀粉溶液。SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2 +2H2O==H2SO4+2HI
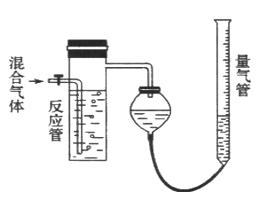
(1)混合气体进入反应管后,量气管内增加的水的体积等于__________的体积(填分子式)。
(2)反应管内的溶液蓝色消失后,没有及时停止通气,则测得的SO2含量_____(填“偏高”、“偏低”或“不受影响”)。
(3)反应管内的碘的淀粉溶液也可以用_______________代替(填写物质名称)。
(4)若碘溶液体积为V![]() mL,浓度为cmol·L
mL,浓度为cmol·L![]() 。N2与O2的体积为V
。N2与O2的体积为V![]() mL(已折算为标准状况下的体积)。用c、V
mL(已折算为标准状况下的体积)。用c、V![]() 、V
、V![]() 表示SO2的体积百分含量为:_________________。
表示SO2的体积百分含量为:_________________。
(5)将上述装置改为简易实验装置,除导管外,还需选的仪器为________(选下列仪器编号)。
a.烧杯 b.试管 c.广口瓶 d.容量瓶 e.量筒 f.单孔塞 g.双孔塞
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于元素周期表的叙述正确的是( )
A. 周期表中有八个主族,八个副族 B. 目前使用的元素周期表中,最长的周期含有32种元素
C. 短周期元素是指1-20号元素 D. 原子的最外层电子数都等于该元素所在的族序数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com