
科目: 来源: 题型:
【题目】Ⅰ.化工工业中常用乙苯脱氢的方法制备苯乙烯。已知某温度下:
反应①:CO2(g) +H2 (g)→CO(g) + H2O(g),ΔH= +41.2 kJ/mol
反应②:![]() (g)→
(g)→![]() (g)+H2(g),ΔH= +117.6kJ/mol
(g)+H2(g),ΔH= +117.6kJ/mol
②的化学反应平衡常数分别为K1、K2。
(1)请写出二氧化碳氧化乙苯制备苯乙烯的热化学反应方程式__________________。该反应的化学平衡常数K=_________(用K1、K2表示)。
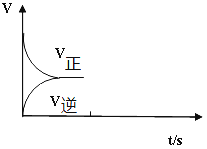
(2)温恒容条件下,反应①达到平衡后;t1时刻通入少量CO2;请在下图中画出t1之后的正逆反应曲线,并作出标注。__________________
Ⅱ.一定条件下,合成氨反应为:如图表示在此反应过程中的能量的变化,如图表示在2L的密闭中反应时N2的物质的量随时间的变化曲线.如图表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
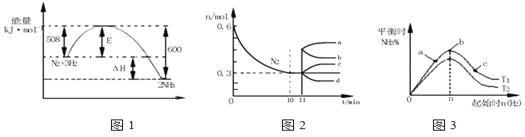
(3)由如图信息,计算10min内该反应的平均速率v(H2)=______,从11min起其它条件不变,压缩容器的体积,则n(N2)的变化曲线为____(填“a”或“b”或“c”或“d”)
(4)如图a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是____点,温度T1____T2(填“>”或“=”或“<”)
Ⅲ.H2O2是一种常用绿色氧化剂,工业上利用电解法制备H2O2的装置如图所示:

(5)a为______(正极、负极)
(6)通入空气的电极反应式为__________
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E是相邻三个周期中的五种元素,它们的原子序数依次增大,B、C、D属同一周期,A 、E在周期表中处于同一纵行。己知:①除A外,各元素原子的内层均已填满电子,其中B的最外层有4个电子;②A与B,B与C都能生成气态非极性分子的化合物;③D与E生成离子化合物,其离子的电子层结构相同。回答:
(1)A为______元素,B为______元素,C为______元素,D为______元素。
(2)C元素在周期表中属______周期______族元素,原子结构简图为_________。
(3)用电子式表示D与E形成化合物的过程_____________,D与B形成的化合物的电子式______
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于二氧化碳和二氧化硅说法中正确的是( )
A. 都可以与水化合生成对应酸
B. 都可以与氢氟酸反应生成气体
C. 都可以跟氢氧化钠溶液反应生成盐和水
D. 都可以形成空间立体网状结构
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于电解质的叙述中,不正确的是( )
A. 不只是酸、碱、盐类物质才属于电解质
B. 氯化钠溶液在电流作用下电离为钠离子与氯离子
C. 电解质未必能导电,能导电的也未必是电解质
D. 硫酸钡的水溶液虽导电性极弱,但硫酸钡是强电解质
查看答案和解析>>
科目: 来源: 题型:
【题目】实验中需2 mol·L-1的Na2CO3溶液950 mL,配制时应选用的容量瓶的规格和称量Na2CO3的质量分别为 ( )
A. 1000 mL,212 g B. 1000 mL,201.4 g
C. 950 mL,201.4 g D. 任意规格,572 g
查看答案和解析>>
科目: 来源: 题型:
【题目】金属钙线是炼制优质钢材的脱氧脱磷剂,某钙线的主要成分为金属M和Ca,并含有3.5%(质量分数)CaO。
(1)Ca元素在周期表中位置是_________,其原子结构示意图_________。
(2)Ca与最活跃的非金属元素A形成化合物D,D的电子式为_________。
(3)将钙线试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,则金属M为______;检测Mn+的方法是_______________________________________(用离子方程式表达)。
(4)取1.6g钙线试样,与水充分反映,生成224ml.H2(标准状况),在想溶液中通入适量的CO2,最多能得到CaCO3_____________g。
查看答案和解析>>
科目: 来源: 题型:
【题目】氨气是一种重要的化工原料,氨态氮肥是常用的肥料。
工业合成氨的化学方程式:N2 + 3H2![]() 2NH3+92.4KJ
2NH3+92.4KJ
(1)它是氮的固定的一种,属于_____________(选填“大气固氮”、“生物固氮” “人工固氮”);若升高温度,该平衡向____________方向移动(选填“正反应”或“逆反应”)。
(2)该反应达到平衡状态的标志是______________。(选填编号)
a.压强不变 b.v正(H2)= v正(NH3) c.c (N2)不变 d.c(NH3)= c(N2)
(3)欲使NH3产率增大,可采取的措施有_____________、____________。若容器容积为2L,开始加入的N2为0.1mol,20s后测得NH3的物质的量为0.08mol,则N2的平均反应速率为_________________________________________mol/(LS)。
(4)如下图所示,将集有氨气的试管倒置于水槽中,观察到试管内液面上升,溶液变为红色,解释发生该现象的原因____________________________________。
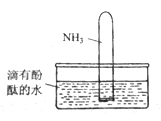
(5)(NH4)2SO4是常用的氮肥,长期施用时会使土壤酸化板结,
用离子方程式表示原因___________________________________
检验(NH4)2SO4含NH4+的方法是____________________。
____________________.
查看答案和解析>>
科目: 来源: 题型:
【题目】请将下列污染原因与结果用线连接起来:
A.氟里昂等排放物 a.酸雨
B.砍伐森林 b.土壤和水污染
C.核污染 c.放射病和癌症发病率增加
D.汽车、燃煤等排放SO2 d.臭氧层破坏
E.大量使用农药 e.土地沙漠化
_______________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组中的反应,属于同一反应类型的是
A.由溴丙烷水解制丙醇;由丙烯与水反应制丙醇
B.由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸
C.由氯代环己烷消去制环己烯;由丙烯加溴制1,2二溴丙烷
D.由乙酸和乙醇制乙酸乙酯;由苯甲酸乙酯水解制苯甲酸和乙醇
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com