
科目: 来源: 题型:
【题目】A、B为两种主族元素,A2-与B3+具有相同的电子层结构。下列有关说法正确的是
A. 原子半径:A>B B. 离子半径:A2->B3+ C. 原子序数:A>B D. A 、B 可形成化合物A2B3
查看答案和解析>>
科目: 来源: 题型:
【题目】金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如下图所示。
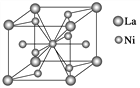
(1)该合金的化学式为__________________;
(2)一定条件下,该贮氢材料能快速、可逆地存储和释放氢气,若每个晶胞可吸收 3 个 H2, 这一过程用化学方程式表示为:______________________________________。
(3)下列关于该贮氢材料及氢气的说法中,正确的是_________( 填序号 )
A.该材料中镧原子和镍原子之间存在化学键,是原子晶体
B.氢分子被吸收时首先要在合金表面解离变成氢原子,同时放出热量
C.该材料贮氢时采用常温高压比采用常温常压更好
D.氢气很难液化是因为虽然其分子内氢键很强,但其分子间作用力很弱
(4)晶体铜是面心立方堆积,在铜的一个晶胞中,把顶点上的铜原子换成Au,可得一种合金,该合金也具有储氢功能,储氢时,氢原子进入到Au和Cu原子构成的的四面体空隙中,则达到最大储氢量的化学式为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】醋酸钡晶体[(CH3COO)2BaH2O]是一种媒染剂,易溶于水.下列有关0.1molL-1醋酸钡溶液中粒子浓度关系的表示中,错误的是( )
A.2c(Ba2+)=c(CH3COO-)+c(CH3COOH)
B.c(H+)+2c(Ba2+)=c(CH3COO-)+c(OH-)
C.c(Ba2+)>c(CH3COO-)>c(OH-)>c(H+)
D.c(H+)=c(OH-) -c(CH3COOH)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列事实的解释中错误的是
A. 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性
B. 浓硫酸和浓盐酸混合可制氯化氢,说明浓硫酸具有吸水性
C. 常温下能够用铝罐储存浓硫酸,是因为浓硫酸的强氧化性可使铝发生钝化
D. 反应:C+2H2SO4(浓)![]() CO2↑+2H2O+2SO2↑中,H2SO4既体现酸性又体现了强氧化性
CO2↑+2H2O+2SO2↑中,H2SO4既体现酸性又体现了强氧化性
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式正确的是 ( )
A. 二氧化硅与强碱溶液反应: SiO2+2OH- = SiO32-+ H2O
B. 将氯气通入NaOH溶液中:Cl2 + OH-= Cl-+ HClO
C. 金属钠与水反应:Na+2H2O=Na+ + 2OH-+ H2↑
D. 少量的金属锌加入到FeCl3溶液中: 2Fe3++3Zn = 2Fe+3Zn2+
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素的核电荷数为X元素的2倍。下列说法正确的是
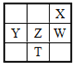
A. X、W、Z元素的原子半径及它们的气态氢化物的热稳定性均依次递增
B. Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增
C. YX2晶体熔化、液态WX3气化均需克服分子间作用力
D. 根据元素周期律,可以推测T元素的单质具有半导体特性,T2X3具有氧化性和还原性
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于如图所示电化学装置的分析正确的是( )
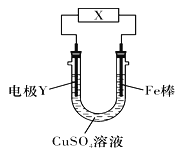
A. 若X为直流电源,Y为碳棒接负极,则Fe棒被保护
B. 若X为电流计,Y为锌棒,则SO42-移向Fe棒
C. 若X为导线,Y为铜棒,则Fe棒发生还原反应
D. 若X为直流电源,Y为铜棒接正极,则Fe棒上有铜析出
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)锌锰(Zn—MnO2)干电池应用广泛,其电解质溶液是ZnCl2—NH4Cl混合溶液。
①该电池的负极材料是_________。电池工作时,电子流向_____________(填“正极”或“负极”)。
②若ZnCl2—NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是________________________。
(2)铅蓄电池是常用的化学电源,其电极材料分别是Pb和PbO2,电解液为硫酸。该电池总反应式为:Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O。请根据上述情况判断:
2PbSO4+2H2O。请根据上述情况判断:
①该蓄电池放电时,电解质溶液中阴离子移向_____________(填“正极”或“负极”);正极附近溶液的酸性_____________(填“增强”、“减弱”或“不变”)放电时,负极的电极反应式为:_____________________________(用离子方程式表示)。(已知:硫酸铅为不溶于水的白色沉淀,生成时附着在电极上)
②实验室用铅蓄电池作电源电解饱和食盐水制取氯气,今若制得0.050 mol Cl2,这时电池内消耗的H2SO4的物质的量至少是________________。氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅蓄电池。若电解质为KOH溶液,则氢氧燃料电池的负极反应式为___________________。该电池工作时,外电路每流过2 mol e-,消耗标况下氧气_________L。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 离子键是阴离子与阳离子间的一种静电引力
B. 任何离子键在形成的过程中必定有电子的得与失
C. 带相反电荷的离子之间的相互吸引力称为离子键
D. 活泼非金属原子与活泼金属原子相遇时能形成离子键
查看答案和解析>>
科目: 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)是重要的化工原料,易溶于水,在中性或碱性环境中稳定,在酸性条件下易分解,在空气中易被氧化。某化学兴趣小组通过如图装置(省略夹持装置)制备Na2S2O3。
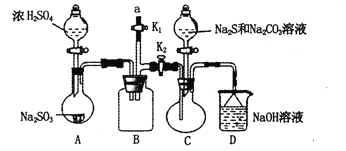
(1)实验开始的步骤,组装好仪器,____________,按图示加入试剂,关闭K1打开K2,先向C中烧瓶加入Na2S和 Na2CO3混合溶液,再向A中烧瓶滴加浓H2SO4。
(2)C中的烧瓶发生如下反应:2Na2S+ Na2CO3+4SO2=3Na2S2O3+CO2,反应开始后,C中先有浑浊产生,后又变澄清,此浑浊物是________;为了保证Na2S2O3的产量,实验中通入C的SO2不能过量,用离子方程式表示其原因_________。
(3)该实验制得的产品中含有NaSO4杂质,为减少装置C中生成Na2SO4的量,在不改变原有装置的基础上对实验开始的步骤进行了改进,改进后的操作是__________。
(4)B装置可以起到安全瓶,防止倒吸的作用,另外在实验结束后拆除装置时还可以防止污染空气,具体操作方法是____________。
(5)制取Na2S2O3的另一种方法是直接将硫粉和亚硫酸钠,数混合共热制取。为探究制取硫代硫酸钠最佳条件,设计如下对比实验(每次实验时亚硫酸钠质量均为63g,反应时间为30min):
实验序号 | 溶液pH | 亚硫酸钠与水的质量比 | 反应温度 | 硫粉质量 | 亚硫酸钠转化率 |
1 | 10 | 1.5:1 | 100℃ | 18 | 80.7% |
2 | 10 | 1.1:1 | 100℃ | 18 | 94.6% |
①实验1、2的目的是探究_________对亚硫酸钠转化率的影响;
②若要完成上表中列出的各项条件对亚硫酸钠转化率的影响探究,除实验1、2外,至少还需进行____次对比实验;
③实验表明:亚硫酸钠转化率不受硫粉质量多少的影响.原因为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com