
科目: 来源: 题型:
【题目】
元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1—36号元素),与中学常见的长式元素周期表相比,第一到第十八可看成族,k为Fe元素。试根据扇形周期表已填入元素回答问题:
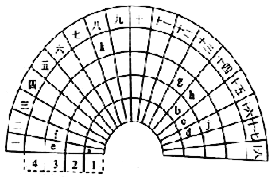
(1)c的基态原子中,核外存在______对自旋相反的电子。元素x与g同族且比g多三个电子层,元素x的价电子排布式为____________。
(2)e、f、g的第一电离能由大到小的顺序为________(用元素符号表示)。
(3)d与j所形成的某种化合物固态时通常以三聚体的环状形式存在,如下图所示,其中j的原子杂化方式为_________。
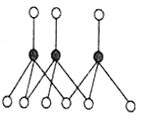
(4)b和d所形成的一种三原子分子与c和d形成的一种化合物互为等电子体,则满足上述条件的c和d形成的化合物的化学式是__________________。
(5)b和h的有关化学键键能如下表所示,简要分析和解释下列有关事实:
化学键 | b-b | b-a | b-b | h-a |
键能/kj·mol-1 | 356 | 413 | 226 | 318 |
b与a形成化合物的种类远大于h与a形成化合物的种类,从能量的角度分析原因_____________。
(6)下图为e与x所形成的合金立方晶系晶胞图,晶胞棱长为748.8pm。

①若把一类金属原子全部抽掉,剩余的金属原子与扇形周期表中哪种已填入元素形成的单质晶型相同,该单质名称为___________。
②原子坐标参数,表示晶胞内部各原子的相对位置。其中坐标参数A处x为(0,0,0);B处e为(0,0, ![]() );C处x坐标为(
);C处x坐标为(![]() ,
, ![]() ,0)。则D处x的坐标参数为___________。
,0)。则D处x的坐标参数为___________。
③该晶体的密度计算式为___________g/cm3(已知x的相对原子质量为204)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质能按照如图关系图(“→”表示反应一步完成)相互转化的是

A | B | C | D | |
X | NaOH | Cu | Fe2O3 | Ca(OH)2 |
Y | NaNO3 | CuO | Fe | CaCl2 |
Z | Na2SO4 | Cu(OH)2 | FeCl2 | CaCO3 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】镁是21世纪最具应用前景的轻金属,工业制镁常用硅热还原法和电解法。
(―)硅热还原法
以白石石(主要成分为CaCO3 MgCO3)为原料制备金属镁的工艺流程如下图所示:

(1)写出回转窑中煅烧CaCO3·MgCO3的化学方程式_________________。
(2)在混合器中,将煅烧得到的固体与还原制镁的催化剂萤石粉混合均匀,萤石粉碎的目的是_____________。
(3)向冷却后的少量烧渣中加入盐酸,观察到有气体产生,写出真空高温还原炉中生成镁蒸气的化学方程式_______________,还原炉抽成真空的目的是_______________。
(二)以MgCl2·6H2O为原料制备金属镁的工艺流程如下图所示:
MgCl2·6H2O![]() MgCl2
MgCl2![]() Mg+Cl2
Mg+Cl2
由MgCl·6H2O制取MgCl2的部分装置(铁架台、酒精灯已略)如下图所示:

(4).循环物质甲的名称是_______________。制取无水。制取无水氯化镁必须在氯化氢存在的条件下进行,原因是_______________;也可以加热亚硫酰氯(SOCl2)与MgCl2·6H2O的混合物制取无水氯化镁,该反应的化学方程式为_________________。
(5)装置b中填充的物质可能是________________。
(6)硅热还原法和电解法的共同缺点是_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】运用化学反应原理研究NH3的性质具有重要意义。请回答下列问题:
(1)已知:①NH3 (g)+3O2(g)=2N2(g)+6H2O(g) △H=-1266.5kJ·mol-1
②N2(g)+O2(g)=2NO(g) △H=+180.5 kJ·mol-1
写出氨高温催化氧化生成NO的热化学方程式___________。
(2)氨气、空气可以构成燃料电池,其电池反应原理为:4NH3+302=2N2+6H2O。已知电解质溶液为KOH溶液,则负极的电极反应式为________。
(3)合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的化学平衡常数K值和温度的关系如下:

由上表数据可知该反应的△H_______ 0 填“> ”、“< ”或“=”) ;
理论上,为了增大平衡时H2的转化率,可采取的措施是_______(选填字母);
A.增大压强 B.使用合适的催化剂 C.升高温度 D.及时分离出产物中的NH3
③400℃时,测得某时刻氨气、氮气、氢气的物质的量浓度分别为3mol·L-1、2 mol·L-1、l mol·L-1,此时刻该反应的V正(N2)=______ V逆(N2)。(填“>”、“<”或“=”)。
(4)已知25℃时,Ksp[Fe(OH)3]=1.0×l0-38, Ksp[Al(OH)3]=3.0×l0-34,当溶液中的金属离子浓度小于1.0×10-5mol·L-1时,可以认为沉淀完全。在含Fe3+、A13+的浓度均为1. 05mol·L-1的溶液中加入氨水,当Fe3+完全沉淀时,A13+沉淀的百分数____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氢能被视为21世纪最具发展潜力的清洁能源,其开发利用是科学家们研究的重要课题。试回答下列问题:
(1)与化石燃料相比,氢气作为燃料的优点是_________(至少答出两点)。
(2)与氢气直接燃烧相比较,设计成镍氢电池可以大大提高能量的转换率,在镍氢电池充电过程中储氢合金(M)吸氢转化为MH2,总反应为:xNi(OH)2+M![]() xNiOOH+MHx,试写出放电过程中负极
xNiOOH+MHx,试写出放电过程中负极
反应式____________。
(3)施莱辛(Sehlesinger)等人提出可用NaBH4与水反应制氢气:BH4-+2H2O=BO2-+4H2↑,已知NaBH4与水反应后所得溶液显碱性,溶液中各离子浓度大小关系为__________,用离子方程式表示出溶液显碱性的原因_______________。
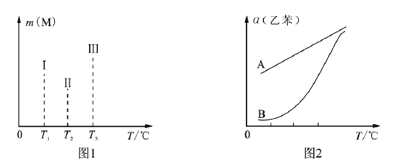
(4)在容积均为VL的Ⅰ、Ⅱ、Ⅲ三个相同密闭容器中,分别放入ag的储氢合金(M)和bmol氢气发生如下反应:2M(s)+xH2(g)![]() 2MHx(s) ΔH<0,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下,实验测得反应均进行到1min时M的质量如图1所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是___________,当三个容器反应都达到化学平衡时,H2转化率最大的反应温度是______。
2MHx(s) ΔH<0,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下,实验测得反应均进行到1min时M的质量如图1所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是___________,当三个容器反应都达到化学平衡时,H2转化率最大的反应温度是______。
(5)储氢还可以借助有机物,如利用乙苯与苯乙烯之间的可逆反应来实现脱氢和加氢;

①在恒容密闭容器中,控制不同温度进行乙苯的脱氢实验。以乙苯起始浓度均为c mol/L测定乙苯的转化率,结果如图2所示。图中A为乙苯的平衡转化率与温度关系曲线,B曲线表示不同温度下反应经过相同时间且为达到化学平衡时乙苯的转化率。试说明随温度的升高,曲线B向曲线A逼近的原因__________。
②维持体系总压恒定,在温度T时,物质的量为n、体积为V的乙苯蒸气发生催化脱氢。已知乙苯的平衡转换率为a,则在该温度下反应的平衡常数K=__________(用a等符号表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化合物的结构(键线式)及球棍模型如下:
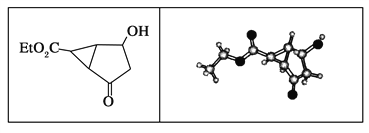
该有机分子的核磁共振氢谱图如下(单位是ppm):
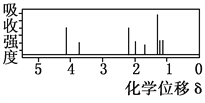
下列关于该有机物的叙述正确的是 ( )
A. 该有机物不同化学环境的氢原子有8种
B. 该有机物属于芳香化合物
C. 键线式中的Et代表的基团为—CH3
D. 该有机物在氢氧化钠醇溶液加热的情况下能发生消去反应
查看答案和解析>>
科目: 来源: 题型:
【题目】如图实验装置进行的相应实验,不能达到实验目的的是

A. 用①所示装置除去 CO2中含有的少量 HCl 气体
B. 用②所示的装置证明可燃物燃烧需要与氧气接触
C. 用③所示装置制取少量 CO2气体
D. 在实验室中,用④所示装置除去少量池水中的泥沙
查看答案和解析>>
科目: 来源: 题型:
【题目】鲜花可以蒸制芳香油,油的主要成分为左旋香芳醇,含量最高可达千分之六,供食用及化妆品用,花瓣可以制饼馅、玫瑰酒、玫瑰糖浆,干制后可以泡茶,花蕾入药治肝、胃气痛、胸腹胀满。果实含丰富的维生素C、葡萄糖、果糖、蔗糖、枸橼酸、苹果酸及胡萝卜素等.β—紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,它经多步反应可合成维生素A1。下列说法正确的是( )

A. β—紫罗兰酮与中间体X互为同分异构体
B. 1mol维生素A1最多能与5molH2发生加成反应
C. 维生素A1易溶于NaOH溶液
D. β—紫罗兰酮不可使酸性KMnO4溶液褪色
查看答案和解析>>
科目: 来源: 题型:
【题目】已知硼、氮、钴、铜是几种重要的元素,请回答下列向题:
(1)Co的基态原子中未成对电子数为________个;Cu的基态原子的电子排布式为_______。
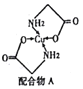
(2)Cu的配合物A的结构如右图,A中所含C、N、O三种元素的第一电离能由大到小的顺序为________。其中氮原子的杂化方式是_______________。
(3)配体氨基乙酸根(H2NCH2COO-)受热分解可产生CO2 和N2, N2中δ键和π键数目之比是________;N2O与CO2互为等电子体,结构相似,且N2O分子中O只与一个N相连,则N2O的电子式为________。
(4)立方氮化硼的晶胞结构与金刚石结构相似(如下图),是超硬材料。
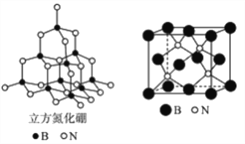
①晶胞中每个氮原子周围与其最近且等距离的硼原子有________个;
②结构化学上常用原子坐标参数表示晶胞内部各原子的相对位置,立方氮化翻的晶胞中,B原子的坐标参数分别有:B (0,0,0);B(![]() ,0,
,0, ![]() );B (
);B (![]() ,(
,(![]() ,
, ![]() ,0)等,则距离上述三个B原子最近且等距离的N原子的坐标参数为_________;
,0)等,则距离上述三个B原子最近且等距离的N原子的坐标参数为_________;
③已知氮化硼晶胞边长为apm,则氮化硼的密度为_______g·cm -3(设NA为阿伏加德罗常数值,只要求列算式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】有5 种短周期元素的原子序数按E、D、B、A、C的顺序依次增大;A、C同周期,B、C同主族;A与B可形成离子化合物A2B,A2B中所有粒子的电子数相同,且电子总数为30;D和E可形成4核10电子的分子。试回答下列问题:
(1)写出五种元素的名称:A_____B_____C_____D______E______。
(2)用电子式表示离子化合物A2B的形成过程:_____________________________;
(3)写出下列物质的电子式:D元素形成的单质_____________;B与E形成的化合物__________________;A、B、E形成的化合物_______________;D、E形成的化合物_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com