
科目: 来源: 题型:
【题目】SO2和氮氧化物的转化和综合利用既有利于节约资源,又有利于保护环境。
(1)H2还原法是处理燃煤烟气中SO2的方法之一。已知:
2H2S(g)+SO2(g)=3S(s)+2H2O(l) ΔH=a kJ·mol—1
H2S(g)=H2(g)+S(s) ΔH=b kJ·mol—1
H2O(l)=H2O(g) ΔH=c kJ·mol—1
写出SO2(g)和H2(g)反应生成S(s)和H2O(g)的热化学方程式:____________。
(2)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中SO2发生催化氧化的反应为:2SO2(g)+O2(g)![]() 2SO3(g)。若在T1℃、0.1 MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2) ∶n(O2)=2∶1],测得容器内总压强与反应时间如图所示。
2SO3(g)。若在T1℃、0.1 MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2) ∶n(O2)=2∶1],测得容器内总压强与反应时间如图所示。
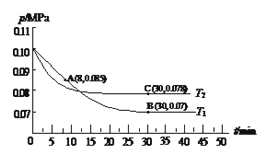
①图中A点时,SO2的转化率为____________。
②在其他条件不变的情况下,测得T2℃时压强的变化曲线如图所示,则C点的正反应速率vc(正)与A点的逆反应速率vA(逆)的大小关系为vc(正)______vA(逆)(填“>”、“<”或“=”)。
③图中B点的压强平衡常数Kp=_______________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)利用脱氮菌可净化低浓度NO废气。当废气在塔内停留时间均为90s的情况下,测得不同条件下NO的脱氮率如图Ⅰ、Ⅱ所示。
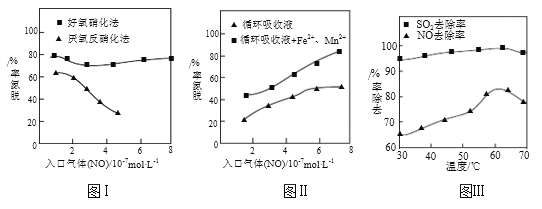
①由图I知,当废气中的NO含量增加时,宜选用_________法提高脱氮效率。
②图Ⅱ中,循环吸收液加入Fe2+、Mn2+提高了脱氮的效率,其可能原因为____________。
⑷研究表明:NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。图Ⅲ所示为复合吸收剂组成一定时,温度对脱硫脱硝的影响。
①写出废气中的SO2与NaClO2反应的离子方程式:____________________________。
②温度高于60℃后,NO去除率随温度升高而下降的原因为_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是
A. 甲醛的水溶液具有杀菌、防腐性能
B. 煤进行气化和液化加工可获得清洁燃料
C. 蚕丝和核酸都属于天然高分子化合物
D. 合成纤维和光导纤维都是新型有机非金属材料
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法错误的是
A. 标准状况下,22.4L NO与11.2 LO2充分反应后分子总数小于NA
B. 1 mol Cl2溶于水,转移的电子数小于NA
C. 18g天然纯水中含16O原子数小于NA
D. 常温常压下,28 g C2H4、CO的混合气体中含有碳原子的数目等于1.5NA
查看答案和解析>>
科目: 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3·5H2O)俗称“海波”,又名“大苏打”,在纺织工业中用于棉织品漂白后的脱氯剂、染毛织物的硫染剂、靛蓝染料的防白剂、纸浆脱氯剂、医药工业中用作洗涤剂、消毒剂和褪色剂等,它易溶于水,难溶于乙醇,加热易分解,具有较强的还原性和配位能力。它是冲洗照相底片的定影剂,棉织物漂白后的脱氯剂,定量分析中的还原剂。工业上常用亚硫酸钠法、硫化碱法等制备。
(1)某实验室模拟工业硫化碱法制取(2Na2S+Na2CO3+4SO2===3Na2S2O3+CO2)硫代硫酸钠,其反应装置及所需试剂如下图,a的装置名称为________,装置c的作用是________________________________________________________________________。

(2)工业上还可以用亚硫酸钠法(亚硫酸钠和硫粉通过化合反应)制得,装置如下图所示。

已知:Na2S2O3在酸性溶液中不能稳定存在,有关物质的溶解度曲线如下图所示。

Na2S2O3·5H2O的制备:
步骤1:如图连接好装置后,检查A、C装置气密性的操作是___________________________。
步骤2:加入药品,打开K1、关闭K2,向圆底烧瓶中加入足量浓硫酸并加热。写出烧瓶内发生反应的化学方程式:_________________________________________________________。
装置B、D的作用是__________________。
步骤3:C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少。当C中溶液的pH接近7时,打开K2、关闭K1并停止加热;C中溶液要控制pH的理由是_______________________________________________________________。
步骤4:过滤C中的混合液,将滤液经过__________________________、冷却结晶、过滤、洗涤、烘干,得到产品。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 明矾净水时发生了物理及化学变化,明矾能起到杀菌消毒的作用
B. 稀豆浆、淀粉溶液、蛋白质溶液均能产生丁达尔效应
C. 红宝石、蓝宝石主要成分足氧化铝,而石英玻璃、分子筛的主要成分是硅酸盐
D. 日常生活中碱块(Na2CO3·10H2O)变成碱面(Na2CO3)属于风化,是物理变化
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应2CH3OH(g)![]() CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在体积恒定的密闭容器中加入一定量的CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在体积恒定的密闭容器中加入一定量的CH3OH,反应到某时刻测得各组分的浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
浓度/mol·L-1 | 0.44 | 0.6 | 0.6 |
下列叙述中正确的是 ( )
A. 该反应的平衡常数表达式为K=[c(CH3OCH3)×c(H2O)]/c(CH3OH)
B. 此时正、逆反应速率的大小:v正<v逆
C. 若经10 min后反应达到平衡,此时c(CH3OH)=0.04 mol·L-1
D. 0~10min内平均反应速率v(CH3OH)=1.6 mol·(L·min)-1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述错误的是( )
A. 乙烯使溴水褪色是因为发生了加成反应
B. 二氧化硫使溴水褪色是因为发生了氧化还原反应
C. 用乙酸和乙醇反应制备乙酸乙酯发生了酯化反应
D. 乙酸乙酯在酸性条件下的水解反应程度更大
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关实验原理或实验操作正确的是
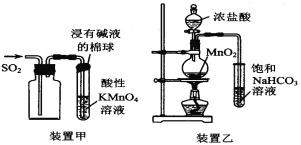
A.用装置甲收集SO2并验证其漂白性
B.用装置乙验证氯气与水反应有盐酸生成
C.用澄清石灰水鉴别苏打溶液和小苏打溶液
D.用NaOH溶液除去苯中混有的少量苯酚,反应后分液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com