
科目: 来源: 题型:
【题目】1,2二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度是2.18克/厘米3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验中可以用下图所示装置制备1,2二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有浓溴(表面覆盖少量水)。请填写下列空白:
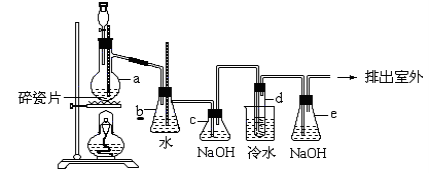
(1)烧瓶a中发生的是乙醇的脱水反应,即消去反应,反应温度是170℃,并且该反应要求温度迅速高到170℃,否则容易产生副反应。请你写出乙醇的这个消去反应方程式:____________。
(2)写出制备1,2二溴乙烷的化学方程式: 。
(3)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象: 。
(4)容器c中NaOH溶液的作用是: 。
(5)某学生做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超出许多,如果装置的气密性没有问题,试分析其可能的原因:___________。
(6)e装置内NaOH溶液的作用是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知1 mol氢气完全燃烧生成水蒸气时放出242 kJ的能量,且氧气中1 mol O===O键完全断裂时需要吸收496 kJ的能量,水蒸气中1 mol H—O键形成时放出463 kJ的能量,则氢气中1 mol H—H键断裂时吸收的能量为
A.436 kJ B.557 kJ C.920 kJ D.181 kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】苯氧布洛芬钙G是评价较好的解热、镇痛、消炎药,下面是它的一种合成路线(具体反应条件和部分试剂略)
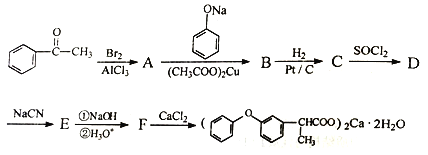
已知①氯化亚砜(SOCl2)可与醇发生反应,醇的羟基被氯原子取代而生成氯代烃。
② (X表示卤素原子)
(X表示卤素原子)
③R-X+NaCN![]() RCN+NaX
RCN+NaX
回答下列问题:
(1)写出D的结构简式:_______________。
(2)B→C的反应类型是___________;F中所含的官能团名称是_________。
(3)写出F和C在浓硫酸条件下反应的化学方程式_______________。
(4)A的同分异构体中符合以下条件的有______种(不考虑立体异构)
①属于苯的二取代物;②与FeCl3溶液发生显色反应。
其中核磁共振氢谱图中共有4个吸收峰的分子的结构简式为____________。
(5)结合上述推断及所学知识,参照上述合成路线任选无机试剂设计合理的方案,以苯甲醇(![]() )为原料合成苯乙酸苯甲酯(
)为原料合成苯乙酸苯甲酯(![]() )写出合成路线__________,并注明反应条件。
)写出合成路线__________,并注明反应条件。
查看答案和解析>>
科目: 来源: 题型:
【题目】环境污染影响人类生存,治理污染是化学工作者研究的重要课题。
(1)可用CO与H2合成甲醇(CH3OH),己知CO、CH3OH(l)、H2的燃烧热分别为:a kJ·mol-1、b kJ·mol-1、c kJ·mol-1,请写出合成CH3OH(l)的热化学方程式:___________________________________。
(2)反应:FeO(s)+CO(g)![]() Fe(s)+CO2(g)在容积固定的密闭容器中进行,其平衡常数K与温度T的关系如图所示。
Fe(s)+CO2(g)在容积固定的密闭容器中进行,其平衡常数K与温度T的关系如图所示。
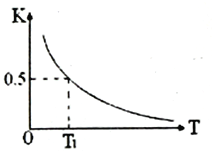
①该反应是________(填“吸热”或“放热”)反应。
②一定条件下,下列能说明该反应达到平衡状态的是__________
a.混合气体的密度不再变化 b.容器内压强不再变化
c. v(CO2)=v(CO) d. CO在混合气中的质量分数保持不变
③写出该反应的平衡常数表达式______________________________________;T1温度下,加入FeO和CO反应达平衡时CO的转化率为 ________________________________。
(3)①把含二氧化硫的工业烟气通入含Cr2O72-和Cr3+的酸性电镀废液中(Cr2O72-被还原为Cr3+,Cr3+能水解),写出该反应的离子方程式:_________________________。
②反应一段时间后开始出现Cr(OH)3沉淀,用必要的离子方程式和文字,表述产生沉淀的原因:____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
(1)Cu位于元素周期表第IB族。元素基态原子3d能级上有__________种不冋运动状态的电子;Cu2+的核外电子排布式为______________________
(2)下图是铜的某种氧化物的晶胞结构示意图,可确定该晶胞中阴离子的个数为__________。

(3)胆矾CuSO4·5H2O可写成[Cu(H2O)]SO4·H2O,其结构示意图如图,下列说法正确的是______(填字母)。

A.在上述结构示意图中,所有氧原子都采用sp3杂化
B.在上述结构示意图中,存在配位键、共价键和离子键
C.胆矾是分子晶体,分子间存在氢键
D.胆矾中的水在不同温度下会分步失去
(4)S、H、O三种元素的电负性由小到大的顺序是________________。
(5)往硫酸铜溶液中加入过量氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色透明溶液,可生成[Cu(NH3)4]2+配离子。写出沉淀转化为深蓝色溶液的的离子方程式__________________;已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是_______________________。
(6)Cu2O的熔点比Cu2S的____________(填“高”或“低”),请解释原因____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学利用CuSO4溶液,进行以下实验探究。

(1)图一是根据反应Zn+CuSO4=Cu+ZnSO4设计成的锌铜原电池。Cu极的电极反应式是_____________________________________________________,
盐桥中是含有琼胶的KCl饱和溶液,电池工作时K+向________(填“甲”或“乙”)池移动。
(2)图二中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则b处通入的是________(填“CH4”或“O2”),a处电极上发生的电极反应是_____________________________________________;
当铜电极的质量减轻3.2 g时,消耗的CH4在标准状况下的体积为________L。
查看答案和解析>>
科目: 来源: 题型:
【题目】天然大理石通常含有Fe2O3等杂质,工业上用大理石作原料时需要提纯,某研究性学习小组在老师的指导下,对大理石进行了提纯,设计了如下的实验流程:
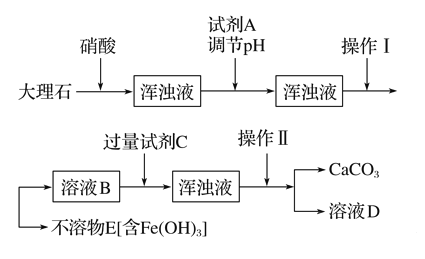
请回答下列问题:
(1)溶解大理石时,用硝酸而不用硫酸的原因是____________________________________________。
(2)操作Ⅰ的名称是________,该操作中用到玻璃棒,玻璃棒在该实验中的作用是___________________________。
(3)检验溶液B中是否含铁离子的操作方法是_________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com