
科目: 来源: 题型:
【题目】某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1)NaN3是气体发生剂,受热分解产生N2和Na,N2的电子式为________。
(2)Fe2O3是主氧化剂,与Na反应生成的还原产物为________(已知该反应为置换反应)。
(3)KClO4是助氧化剂,反应过程中与Na作用生成KCl和Na2O。KClO4含有化学键的类型为________,K的原子结构示意图为________。
(4)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将下列晶体熔化:氢氧化钠、二氧化硅、氧化钙、四氯化碳,需要克服的微粒间的相互作用有:①共价键 ②离子键 ③分子间的作用力正确的顺序是( )
A. ①②②③ B. ②①②③ C. ②③②① D. ①①②③
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 在NH![]() 和[Cu(NH3)4]2+中都存在配位键
和[Cu(NH3)4]2+中都存在配位键
B. HF、HCl、HBr、HI的熔、沸点依次升高
C. CO2、SO2都是极性分子
D. 氯的各种含氧酸的酸性由强到弱排列为HClO>HClO2>HClO3>HClO4
查看答案和解析>>
科目: 来源: 题型:
【题目】一种充电电池放电时的电极反应为:H2+2OH--2e-=2H2O;NiO(OH)+H2O+e-=Ni(OH)2+OH-当为电池充电时,与外电源正极连接的电极上发生的反应是 ( )
A. Ni(OH)2的氧化 B. NiO(OH)的还原 C. H2的氧化 D. H2O的还原
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是
A.化学反应除了生成新物质外,还伴随着能量的变化
B.放热反应不需加热就能发生
C.需要加热才能发生的反应不一定是吸热反应
D.化学反应是放热还是吸热,取决于反应物和生成物所具有的总能量的相对高低
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述中正确的是( )
A. CO2是酸性氧化物 B. 由一种元素组成的物质一定是单质
C. 单质只能用置换反应制取 D. 含氧元素的化合物称为氧化物
查看答案和解析>>
科目: 来源: 题型:
【题目】在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”。凡有一个手性碳原子的物质一定具有光学活性,物质![]() 有光学活性,发生下列反应后生成的有机物无光学活性的是
有光学活性,发生下列反应后生成的有机物无光学活性的是
A. 与甲酸发生酯化反应 B. 与NaOH水溶液共热
C. 与银氨溶液作用 D. 在催化剂存在下与HCN作用
查看答案和解析>>
科目: 来源: 题型:
【题目】FeCO3与砂糖混用可作补血剂。以黄铁矿烧渣(含CuO、Fe2O3、FeO、SiO2、Al2O3等)为主要原料制备FeCO3的流程如下:
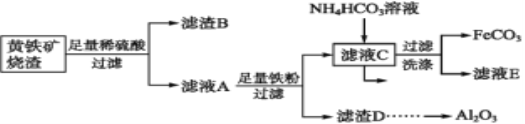
(1)质量分数为30%(密度是1.176 g·cm-3)的稀硫酸的物质的量浓度为________。
(2)检验滤液A中存在Fe2+的试剂是________。
(3)加入足量铁粉的作用除调节pH使Al3+转化为Al(OH)3沉淀外,还有两个作用,分别写出这两个反应的离子方程式:____________ , ________________。
(4)写出滤液C与NH4HCO3溶液反应的离子方程式:_____________________。
(5)FeCO3在空气中灼烧可制得铁系氧化物材料。已知25 ℃,101 kPa时:
4Fe(s)+3O2(g)![]() 2Fe2O3(s)ΔH=-1 648 kJ·mol-1
2Fe2O3(s)ΔH=-1 648 kJ·mol-1
C(s)+O2(g)![]() CO2(g)ΔH=-393 kJ·mol-1
CO2(g)ΔH=-393 kJ·mol-1
2Fe(s)+2C(s)+3O2(g)![]() 2FeCO3(s)ΔH=-1 480 kJ·mol-1
2FeCO3(s)ΔH=-1 480 kJ·mol-1
写出FeCO3在空气中灼烧生成Fe2O3的热化学方程式:________。
(6)某兴趣小组为充分利用副产品,欲利用滤渣D为原料制取Al2O3,请补充完成实验步骤:向滤渣D中加入适量________溶液,_______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物;Y与氧元素可组成Y2O和Y2O2离子化合物。
(1)写出Y2O2的电子式:_______________,
其中含有的化学键是______________。
(2)用电子式表示Y2O的形成过程_________________________________。
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是________(填化学式)。
(4)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是______________(填化学式)。
(5)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是( )
A.在分子中,两个成键的原子间的距离叫做键长
B.含有极性键的分子不一定是极性分子
C.键能越大,表示该分子越容易受热分解
D.共价键的方向性决定了原子在形成分子时相互结合的数量关系
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com