
科目: 来源: 题型:
【题目】化合物A(分子式为C6H6O)是一种有机化工原料,在空气中易被氧化。A 的有关转化反应如下(部分反应条件略去):
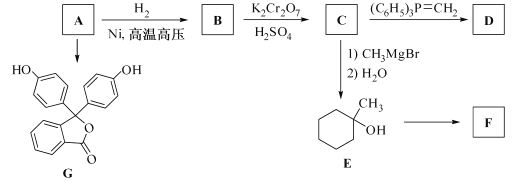
已知:①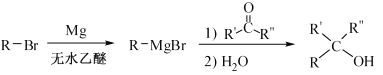
②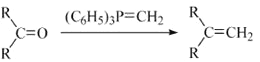 (R表示烃基,R′和R″表示烃基或氢)
(R表示烃基,R′和R″表示烃基或氢)
③F和D互为同分异构体
(1)写出A的名称:________________。
(2)G是常用指示剂酚酞,G中能够与NaOH溶液反应的官能团的名称:_______________。
(3)A能够与甲醛形成一种线型结构高分子,其结构简式为:__________。
(4)分别写出反应A→B和E→F的化学方程式,并注明反应类型:
A→B:________________________________________________,
E→F:________________________________________________,
(5)符合下列条件的C的同分异构体共_______种。
①能发生银镜反应②分子中不含环状结构
写出其中含有三个甲基的分子的结构简式_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】分子式为C8H16O2的有机物A,它能在酸性条件下水解生成B和C,且B在一定条件下能转化成C。则有机物A的可能结构有( )
A.1种B.2种C.3种D.4种
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学物质在实际生产、生活和科技等方面的应用正确的是( )
A. 我国自主研发的“龙芯1号”CPU芯片与光导纤维是同种材料
B. 生产普通玻璃的主要原料有石灰石、石英和纯碱
C. 水晶项链和餐桌上的瓷盘都是硅酸盐制品
D. 玻璃上的漂亮花纹都依靠浓硫酸的腐蚀作用
查看答案和解析>>
科目: 来源: 题型:
【题目】运用化学反应原理研究化学反应有重要意义。
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)![]() 2SO3(g),混合体系中SO3的百分含量和温度的关系如图1所示(曲线上任何一点都表示平衡状态)。
2SO3(g),混合体系中SO3的百分含量和温度的关系如图1所示(曲线上任何一点都表示平衡状态)。
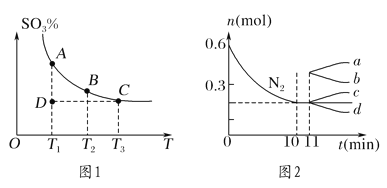
①若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡________(填“向左”“向右”或“不”)移动。
②若反应进行到状态D时,v正________(填“>”“<”或“=”)v逆。
(2)课本里介绍的合成氨技术叫哈伯法:N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,应用此法反应达到平衡时反应物的转化率不高。
2NH3(g) ΔH<0,应用此法反应达到平衡时反应物的转化率不高。
①能使该反应的反应速率增大,且平衡向正反应方向移动的措施是________(填编号)。
A.使用更高效的催化剂
B.升高温度
C.及时分离出氨气
D.充入氮气,增大氮气的浓度(保持容器体积不变)
②若在某温度下,2 L的密闭容器中发生合成氨的反应,图2表示N2的物质的量随时间的变化曲线。用H2表示0~10 min内该反应的平均速率v(H2)=________。从第11 min起,压缩容器的体积为1 L,则n(N2)的变化曲线为________(填编号)。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯碱厂电解饱和食盐水制取NaOH的化学反应方程式为:2NaCl + H2O![]() 2NaOH + H2↑+ Cl2↑,工艺流程示意图如下:
2NaOH + H2↑+ Cl2↑,工艺流程示意图如下:
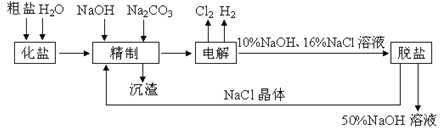
下表是NaCl和MaOH在水中的溶解度
温度 物质 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ | 100℃ |
NaCl | 35.7g | 36g | 36.6g | 37.3g | 38.4g | 39.8g |
NaOH | 42g | 109g | 129g | 174g | 314g | 347g |
依据示意图和表,完成下列填空:
(1)工业食盐中含CaCl2、MgCl2等杂质。除去Ca2+、Mg2+过程发生反应的化学反应方程式为_____。
(2)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过______、冷却、______(填写操作名称)除去NaCl。
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是________(填字母序号)。
①Ba(NO3)2 ②BaCl2
(4)为了有效地除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为_______(少选多选都不计分)。
A.先加NaOH,后加Na2CO3,再加钡试剂 B.先加Na2CO3,后加钡试剂,再加NaOH
C.先加钡试剂,后加NaOH,再加Na2CO3 D.先加NaOH,后加钡试剂,再加Na2CO3
(5)用制得的 NaOH固体配制 240 mL0.2mol/L NaOH 溶液。
①配制时,必須使用的玻璃仪器有______________________。
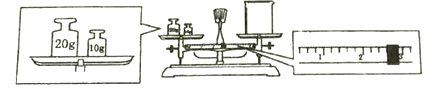
②某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。
烧杯的实际质量为________________g。
③在配制过程中,其他操作都是正确的,下列情对所配制的NaOH珩液的浓度偏高有_____。
A.没有洗涤烧杯和玻璃棒 B.容量瓶不干燥,含有少量蒸馏水
C.定容时俯视刻度线 D.定容时仰视刻度线
E.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线。
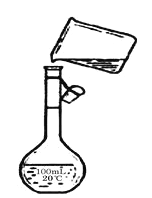
④下图是该同学转移溶液的示意图,图中的错误是_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验操作不正确的是
实验目的 | 实验操作 | |
A | 验证化学反应中的能量变化 | 将NO2球浸泡在冰水,热水中观察颜色变化 |
B | 证明非金属性:Cl>C>Si | 将纯碱与足量浓盐酸反应后产生的气体直接通入硅酸钠溶液中 |
C | 探究相同条件下,溶液浓度对反应速率的影响 | 在两支试管中各加入4 ml 0.01 mol/L的KMnO4 酸性溶液,再分别加入0.1 mol/L H2C2O4 溶液2 ml、0.2 mol/L H2C2O4 溶液2 mL, 分别记录溶液褪色所需时间 |
D | 除去氢氧化铁中少量的氢氧化铜 | 将过量氨水加入混合物中并充分搅拌,然后过滤、洗涤、干燥 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室拟将适量浓硝酸分多次加入铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图1、2所示)。

(1)图1烧瓶中随着反应分进行,可能发生反应的离子方程式为①____________________;
②_______________________________________。
(2)图2是图1的改进装置,其优点有:①_______________________________________;
②________________________________________________________________________。
(3)为符合绿色化学的要求,进行如下设计:
方案1:以空气为氧化剂,将铜粉在仪器B中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应。
方案2:将3.2g铜丝放入45mL1.5mol·L-1的稀硫酸中,控温在50℃。加入18g10%的H2O2溶液,反应0.5小时后,升温到60℃,持续反应1小时后,过滤、蒸发、结晶、减压抽滤后,用少量95%的酒精淋洗后晾干,得10.6gCuSO4·5H2O。请回答下列问题:
①方案1中仪器B的名称是________________。
②方案2中生成CuSO4·5H2O的产率是________(保留三位有效数字)。
③上述两种方案中,更符合绿色化学理念的是________(填“方案1” 或“方案2”),理由是:该方案的优点是__________________________________________________;
另一方案的缺点是_________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各原子或离子的电子排布式错误的是( )
A. Al 1s22s22p63s23p1 B. S2- 1s22s22p63s23p4 C. Na+ 1s22s22p6 D. F 1s22s22p5
查看答案和解析>>
科目: 来源: 题型:
【题目】下表中对于相关物质的分类全部正确的是
选项 | 纯净物 | 混合物 | 非电解质 | 弱电解质 | 碱性氧化物 |
A. | 液氨 | 氢氧化铁胶体 | CO | 氢硫酸 | Al2O3 |
B. | 明矾 | 漂白粉 | 乙醇 | 硫酸钡 | Na2O |
C. | 碱石灰 | 碘酒 | Cl2 | HClO | K2O |
D. | 磁性氧化铁 | 水玻璃 | SO2 | 冰醋酸 | CaO |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】重要化工原料CuSO4的制备途径及性质如图所示。下列说法错误的是

A. 途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2
B. 相对于途径①、③,途径②更好地体现了绿色化学思想
C. Y物质具有还原性,可以是葡萄糖
D. 1molCuSO4在1100℃所得混合气体X中O2一定为0.75mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com