
科目: 来源: 题型:
【题目】甲、乙、丙是三种不含相同离子的可溶性物质。它们所含离子如下表所示:
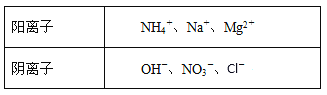
取等质量的三种化合物配制相同体积的溶液,其溶质物质的量浓度:c(甲)>c(乙)>c(丙),则乙物质可能是①MgCl2 ②NaOH ③NH4NO3
A. ① B. ② C. ③ D. ①②
查看答案和解析>>
科目: 来源: 题型:
【题目】铬渣含有Na2SO4及少量Cr2O72-、Fe2+。从化工厂铬渣中提取硫酸钠的工艺如下:
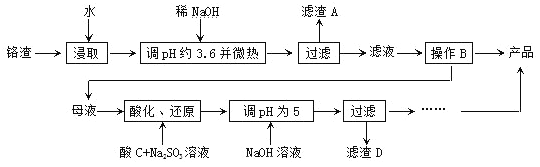
已知:常温时,Fe3+、Cr3+完全沉淀(c≤1.0×10-5mol·L-1)时pH分别为3.6和5。
(1)“微热”的作用是__________________。(填写两点);滤渣A为_____(填化学式)。
(2)根据溶解度(S)-温度(T)曲线,操作B为___________。

(3)酸C为_________(填化学式),“酸化、还原”步骤反应的离子方程式为__________。
(4)常温时,Cr(OH)3的溶度积常数Ksp[Cr(OH)3]=_______。
(5)某工厂采用电解法处理含铬废水,用铁作阴阳极,槽中盛放含铬废水,原理示意图如下。
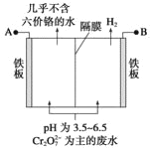
阴极放出氢气,阳极区发生的反应有_________,___________。不考虑气体的溶解,当收集到6.72L(标准状况)的氢气时,理论上有________molCr2O72-被还原。
查看答案和解析>>
科目: 来源: 题型:
【题目】CO2和甲烷催化合成CO和H2是CO2资源化利用的有效途径。主要反应为
Ⅰ:CH4(g)+CO2(g) ![]() 2CO(g)+2H2(g) △H=+247kJ/mol
2CO(g)+2H2(g) △H=+247kJ/mol
(1)已知CH4(g)+H2O(g) ![]() CO(g)+H2(g) △H=+206kJ/mol
CO(g)+H2(g) △H=+206kJ/mol
写出CH4和水蒸气反应生成CO2的热化学方程式_________。
(2)在恒温、恒容的密闭容器中发生反应I,下列选项能够说明反应I达到平衡状态的是______。
A.混合气体的密度不变
B.混合气体的总压强不变
C.CH4、CO2、CO、H2的物质的量之比为1:1:2:2
D.3V正(H2)=V逆(CH4)
E.混合气体的平均相对分子质量不变
(3)催化合成的温度通常维持在550-750℃之间,从反应速率角度分析其主要原因可能是_________。
(4)将CH4与CO2各1mol充入某密闭容器中,发生反应I。100Kpa时,反应I到达平衡时CO2的体积分数与温度的关系曲线如图所示。

①图中A、B、C三点表示不同温度、压强下达到平衡时CO2的体积分数,则______点对应的平衡常数最小,判断依据是________;__________点对应的压强最大。
②300℃,100Kpa下,该容器中反应I经过40min达到平衡,计算反应在0-40min内的平均反应速率为v(CO2)=_________mol/min(结果保留两位有效数字),该温度下的压强平衡常数Kp=________。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列试剂的保存方法错误的是( )
A. 实验室少量的钠保存在煤油中 B. 新制的氯水保存在棕色玻璃瓶中
C. 氢氟酸(HF)保存在无色的玻璃瓶中 D. 氢氧化钠溶液保存在带橡皮塞的玻璃瓶中
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列说法正确的是
A.50 mL 12 mol·L1的盐酸与足量MnO2共热,转移的电子数为0.3NA
B.电解精炼铜时,若转移6.02×1023个电子,阳极溶解32 g铜
C.标准状况下,22.4 L 14CO2与44 g 14CO2所含分子数均为NA
D.2 L 0.2 mol·L1硝酸与适量铁恰好完全反应(还原产物为NO),生成NO的分子数为0.1NA
查看答案和解析>>
科目: 来源: 题型:
【题目】某厂排出的废液主要含Zn(NO3)2和AgNO3,为了从中回收金属银和硝酸锌,某中学化学课外活动小组设计了以下的实验步骤
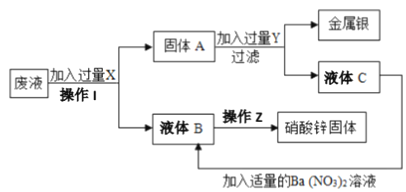
(1)操作I________ (名称)
(2)滤液B的主要成分是______________。(写化学式)
(3)请写出A到C的方程式 _________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】石英沙(主要成分为SiO2)是一种常用的工业原料,其中常混有少量碳酸钙。要除去石英沙中的少量碳酸钙,应采用的方法是( )
A. 用水溶解后过滤分离 B. 用酒精灯加热
C. 用稀硫酸溶解后过滤分离 D. 用稀盐酸溶解后过滤分离
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com