
科目: 来源: 题型:
【题目】有机化合物与我们的生活息息相关,下列说法正确的是( )
A.甲苯的硝化、油脂的皂化均可看作取代反应
B.蛋白质水解生成葡萄糖放出热量,提供生命活动的能量
C.石油裂解的目的是为了提高轻质液体燃料的产量和质量
D.棉花和合成纤维的主要成分是纤维素
查看答案和解析>>
科目: 来源: 题型:
【题目】0.5mol Na2SO4中
A. 含0.5个Na2SO4分子 B. 含3.01×1023个SO42-
C. 含0.5molNa+ D. 含1mol氧原子
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:体积为VmL质量分数为a%的硫酸,密度为ρg·mL-1,摩尔质量为Mg·mol-1,物质的量浓度为cmol·L-1,则下列关系式正确的是
A. ![]() B.
B. ![]() C. M=ρ·V·a% D.
C. M=ρ·V·a% D. ![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W、U五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为54。X的激发态原子电子排布式为2p1,Y原子的基态原子有3个不同的能级,且各能级中电子数相等,Z的基态原子中有3个未成对电子,W的电离能如下表所示,U原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态。
元素 | 第一电离能 | 第二电离能 | 第三电离能 |
W | 495.8 | 4562 | 6910.3 |
(1)U原子电子排布式为_______________。
(2)X与Z 形成的化合物Z2X4,Z原子采取的杂化轨道类型为_______,Y的最高价氧化物的水化物的正盐的阴离子的空间构型为_______;
(3)W的氯化物和Mg的氯化物中,熔点较高的是________(填化学式),原因是_______。
(4)I4O9由一种阳离子和一种阴离子按物质的量比1:3构成,阴离子的空间构型为三角锥形,中心原子杂化类型为sp3杂化,写出I4O9的电离方程式______。
(5)Nb(黑球)和I(白球)能形成一种线性的无机高分子化合物,其结构是许多八面体通过棱边而联结起来的长链,如下图所示。则该化合物中Nb和I的原子个数比为______。
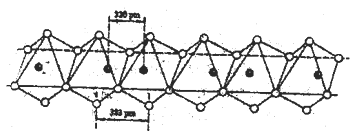
查看答案和解析>>
科目: 来源: 题型:
【题目】下列与有机物的结构、性质有关的叙述正确的是( )
A.苯不能使酸性高锰酸钾溶液褪色,所以苯不能发生氧化反应
B.石油的主要成分是烃,煤经过分馏可制得焦炭、煤焦油等产品
C.丙烯分子中所有原子不可能在同一平面上
D.淀粉、纤维素都是天然高分子有机物,其链节中都含有葡萄糖
查看答案和解析>>
科目: 来源: 题型:
【题目】某一元弱酸HA的相对分子质量为M。在t℃时,将a g HA完全溶解于水中,得V mL饱和溶液,测得该溶液的密度为ρ g/cm3,其中n(A)为b mol。下列叙述中,错误的是
A.溶液中:c(H+)=[1000b+c(OH)V]/V mol/L
B.t℃时,HA的溶解度:S=(100a/ρ)V g
C.物质的量浓度:c(HA)=(1000a/MV) mol/L
D.HA的质量分数:ω(HA)=(a/ρV)×100%
查看答案和解析>>
科目: 来源: 题型:
【题目】已知CuS和Cu2S均为黑色,常温下都不溶于稀盐酸,在氧气中加热,最后都转化为CuO和SO2。某黑色固体样品的成分可能是CuO、CuS和Cu2S的一种或几种。某课外研究小组为探究其成分,设计以下实验测定该样品与氧气反应前后的质量变化,同时检测其气体产物。
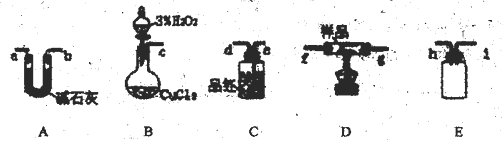
(1)获得氧气的反应方程式为__________。硫化亚铜与氧气反应的方程式为__________。
(2)利用上述装置(可重复使用)进行实验,气流经导管的顺序为__________。
(3)实验测得样品质量为m1,与氧气充分反应后的固体质量为m2,m1 =m2,且C装置中品红褪色,则样品的成分(写出所有可能情况)_________。
(4)该实验小组为了控制实验中氧气的产生速率,设计了如下图所示的实验装置继续探究不同的催化剂对H2O2分解的催化效率。
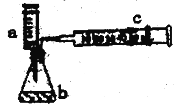
①实验时可以通过测量_________来体现H2O2的分解速率的大小。
②请设计实验比较Fe3+含 Cu2+对H2O2分解的催化效率(完成以下实验方案):_______,最后,比较两个实验的氧气的体积。(试剂仪器不限,装置用上图)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是
A.已知P(s,白磷)![]() P(s,红磷) ΔH<0,则白磷比红磷稳定
P(s,红磷) ΔH<0,则白磷比红磷稳定
B.已知2H2(g)+O2(g)![]() 2H2O(g) ΔH=483.6 kJ·mol1,则氢气的燃烧热为 241.8 kJ·mol1
2H2O(g) ΔH=483.6 kJ·mol1,则氢气的燃烧热为 241.8 kJ·mol1
C.已知2C(s)+2O2(g)![]() 2CO2(g) ΔH=a 2C(s)+O2(g)
2CO2(g) ΔH=a 2C(s)+O2(g)![]() 2CO(g) ΔH=b,则 a>b
2CO(g) ΔH=b,则 a>b
D.已知 NaOH(aq)+HCl(aq)![]() NaCl(aq)+H2O(l) ΔH=57.3 kJ·mol1,则含 40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ 的热量
NaCl(aq)+H2O(l) ΔH=57.3 kJ·mol1,则含 40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ 的热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com