
科目: 来源: 题型:
【题目】自然界中存在大量的金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用。回答下列问题:
(1)CuSO4和Cu(NO3)2中阳离子核外电子排布式为_________,S、O、N三种元素的电负性由大到小的顺序为_________。
(2)在硫酸铜溶液中加入过量KCN能生成配离子[Cu(CN)4]2,CN中提供孤电子对的原子是______,1 mol CN中含有的π键的数目为_________。与CN互为等电子体的离子有_________ (写出一种即可)。
(3)已知AlCl3的蒸气是缔合的双分子(Al2Cl6),更高温度下Al2Cl6则离解生成AlCl3单分子。单分子AlCl3的立体构型是________,缔合双分子Al2Cl6中Al原子的杂化轨道类型为_________。
(4)NaCl和MgO都属离子化合物,NaCl的熔点为801.3℃,MgO的熔点高达2800℃。造成两种晶体熔点差距的主要原因是_____。
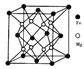
(5)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。则铁镁合金的化学式为________,若该晶胞的参数为d nm,则该合金的密度为____________ g/cm3 (不必化简,用NA表示阿伏加德罗常数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某双原子分子构成的气体,其摩尔质量为M g/mol,该气体质量为m g,阿伏加德罗常数为NA,则:
(1)该气体的物质的量为_______________________。
(2)该气体在标准状况下的体积为______________L。
(3)该气体在标准状况下的密度为____________g/L。
(4)该气体所含原子总数为___________________个。
(5)该气体的一个分子的质量为_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】铁是目前世界上用量最大的金属材料,有关铁及其化合物的说法正确的是( )
A. 磁铁矿的成分是Fe2O3
B. Fe2+遇KSCN溶液显红色
C. Fe可被冷的浓HNO3钝化
D. Fe2+可被还原剂还原为Fe3+
查看答案和解析>>
科目: 来源: 题型:
【题目】砷元素广泛存在于自然界,砷与其化合物被运用在农药、除草剂、杀虫剂等。
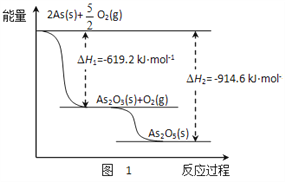
(1)砷的常见氧化物有As2O3和As2O5,其中As2O5热稳定性差。根据图1写出As2O5分解为As2O3的热化学方程式_________________。
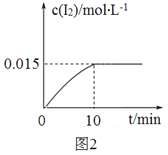
(2)砷酸钠具有氧化性,298 K时,在100 mL烧杯中加入10 mL 0.1 mol/L Na3AsO4溶液、20 mL 0.1 mol/L KI溶液和20 mL 0.05 mol/L硫酸溶液,发生下列反应:AsO43-(无色)+2I-+2H+![]() AsO33-(无色)+I2(浅黄色)+H2O ΔH。测得溶液中c(I2)与时间(t)的关系如图2所示(溶液体积变化忽略不计)。
AsO33-(无色)+I2(浅黄色)+H2O ΔH。测得溶液中c(I2)与时间(t)的关系如图2所示(溶液体积变化忽略不计)。
①下列情况表明上述可逆反应达到平衡状态的是_______(填字母代号)。
a.溶液颜色保持不再变化 b.c(AsO33-)+c(AsO43-)不再变化
c.AsO43-的生成速率等于I2的生成速率 d. 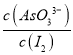 保持不再变化
保持不再变化
②0~10 min内,I的反应速率v(I)=_______。
③在该条件下,上述反应的平衡常数K=______。
④升高温度,溶液中AsO43-的平衡转化率减小,则该反应的 ΔH______0(填“大于”“小于”或“等于”)。
(3)利用(2)中反应可测定含As2O3和As2O5的试样中的各组分含量(所含杂质对测定无影响),过程如下:
①将试样0.2000 g溶于NaOH溶液,得到含AsO33-和AsO43-的混合溶液。
②上述混合液用0.02500 molL-1的I2溶液滴定,用____ 做指示剂进行滴定。重复滴定2次,平均消耗I2溶液40.00 mL。则试样中As2O5的质量分数是______。
(4)雄黄(As4S4)在空气中加热至300℃时会生成两种氧化物,其中一种氧化物为剧毒的砒霜(As2O3),另一种氧化物为______(填化学式),可用双氧水将As2O3氧化为H3AsO4而除去,写出该反应的化学方程式_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E五种化合物均含有某种常见短周期元素,它们的转化关系如图所示,其中A为澄清溶液,C为难溶的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)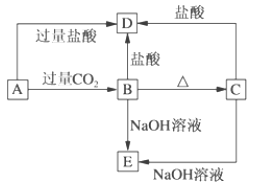
(1)写出化学式:A__________, C___________。
(2)写出下列反应的离子方程式:
A→B:_________________________________________
A→D:__________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中不正确的是
A.常温下pH=7的溶液中:Fe3+、Mg2+、![]() 、Cl能大量共存
、Cl能大量共存
B.在含有0.1 mol·L1 Fe3+的溶液中:SCN、Cl、K+不能大量共存
C.在含有![]() 、
、![]() 、S2、CH3COO四种阴离子的溶液中加入足量的Na2O2固体后,CH3COO浓度变化最小
、S2、CH3COO四种阴离子的溶液中加入足量的Na2O2固体后,CH3COO浓度变化最小
D.常温下,水电离出c(H+)=1010的溶液中:Na+、ClO、S2、![]() 不能大量共存
不能大量共存
查看答案和解析>>
科目: 来源: 题型:
【题目】化合价是学习氧化还原反应的基础。下列化合物中,加点元素的化合价错误的是:
A. CaCO3 (+4) B. H2C2O4 (+3)
C. Na2O2 (-2) D. NH4NO3 (-3)
查看答案和解析>>
科目: 来源: 题型:
【题目】我国空气质量预报的内容主要包括三个方面:二氧化硫、氮氧化物(NOx)、悬浮颗粒物等三种大气污染物的浓度。
(1)与氮氧化物有关的全球或区域性大气环境问题有___________(填字母序号)。
a.酸雨 b.沙尘暴 c.光化学烟雾 d.温室效应
(2)为了降低汽车尾气对大气的污染,目前最有效的方法是给汽车安装尾气净化装置。它能将尾气中的一氧化碳和NO在催化剂作用下,发生反应转化为无害气体,其反应的化学方程式为__________________________。
(3)①实验室也可用下图所示装置制取氨气。烧瓶内固体可选用________(选填选项的代号)。
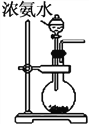
a.碱石灰 b.生石灰 c.二氧化硅 d.五氧化二磷
②催化剂存在下,NH3也可用来消除NOx的污染,生成两种对环境无害的物质,请写出NH3与NO2反应的化学方程式为______________________,该反应中每生成0.5molN2转移____________mol电子(保留至小数点之后一位数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com